МикроРНК способствует реактивации «спящего» герпесвируса
Одна из проблем лечения инфекции вируса герпеса — его незаметность для иммунной системы в скрытом состоянии. При реактивации герпесвирус сначала вырабатывает микроРНК miR-aU14, которая нарушает процессирование микроРНК семейства miR-30. Это, в свою очередь, увеличивает экспрессию p53 и DRP1, а также способствует фрагментации хромосом. В результате снижается уровень интерферонов, и герпесвирус может быть реактивирован. Авторы рассматривают возможность разработки терапии, направленной на miR-aU14.
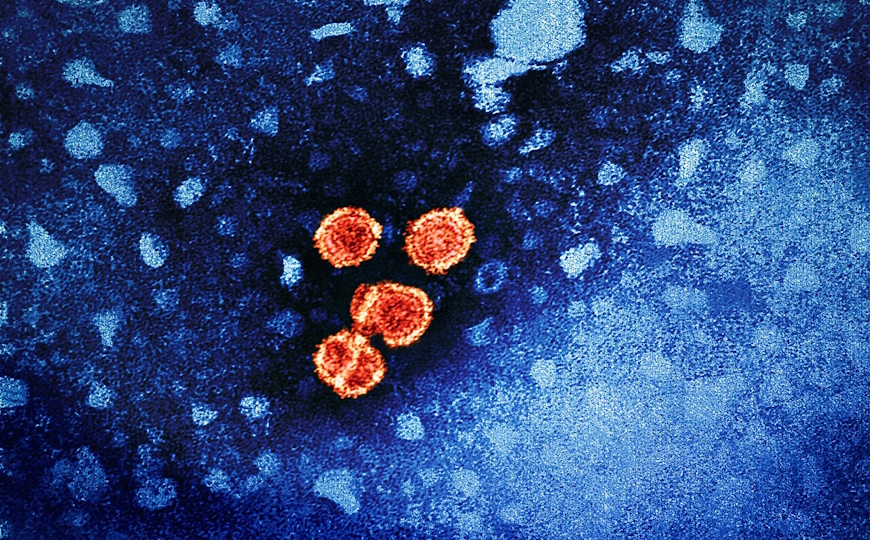
Более 90% всех людей заражено вирусом герпеса человека типа 6A (ВГЧ-6A). Большую часть времени вирус проводит в скрытом состоянии, интегрировав в теломерную область хромосомы. Не до конца понятен механизм реактивации ВГЧ-6A. Ученые из Германии продемонстрировали, что основную роль в этом процессе играет микроРНК.
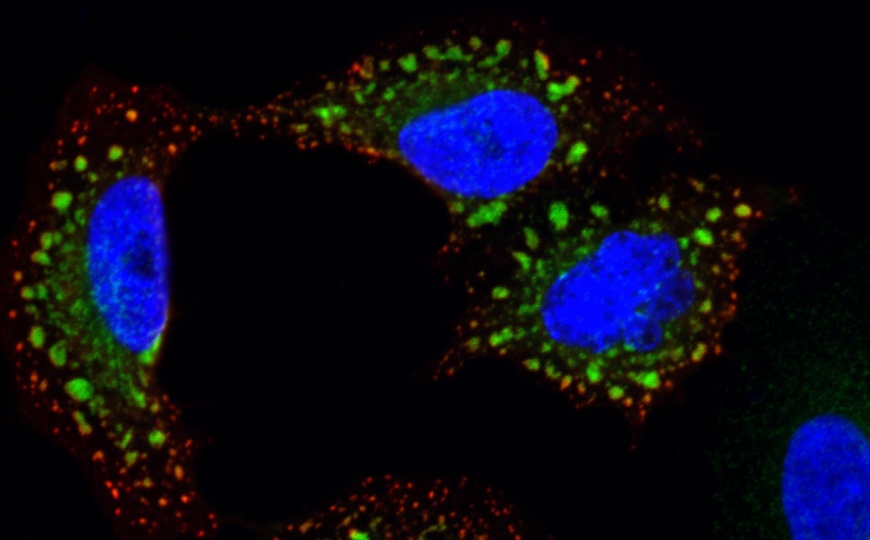
Сначала авторы показали, как ВГЧ-6A действует на митохондрии. Они заражали HUVEC вирусом герпеса. В этих клетках экспрессировался GFP, таргетирующий митохондрии, поэтому их можно было визуализировать. Через 24 часа после инфекции была отмечена фрагментация митохондрий. Схожий эффект был показан и в клетках U2OS при индуцированной реактивации ВГЧ-6A. Фрагментация была связана с увеличением экспрессии белка DRP1, который формирует кольцо вокруг митохондрий при их делении. Также увеличивалась экспрессии белка p53, который контролирует экспрессию DRP1 на уровне транскрипции.
Деление и слияние митохондрий регулируются микроРНК семейства miR-30. Они таргетируют p53 и DRP1. Ученые показали, что при заражении ВГЧ-6A нарушается процессирование этих микроРНК.
Во время реактивации вируса герпеса в клетках U2OS он сначала не реплицируется, но производит некоторые микроРНК и мРНК. Авторы проверили, есть ли среди них микроРНК, которые могли бы нарушать процессирование микроРНК семейства miR-30. Оказалось, что вирусная miR-aU14 комплементарна пре-miR-30a, пре-miR-30d и пре-miR-30c. Эта вирусная микроРНК экспрессируется на высоком уровне при заражении и реактивации.
Одной miR-aU14 достаточно, чтобы привести к фрагментации митохондрий через ось p53–DRP1; ее присутствие также необходимо. Это доказали на мутантном miR-aU14, который не индуцировал экспрессию p53 и DRP1, а также с помощью мимика и мутантного вирусного генома, несущего замены в miR-aU14. На клетках HeLa ученые показали, что miR-aU14 напрямую взаимодействует с пре-miR-30c в районе шпильки.
Митохондрии играют важную роль во врожденном иммунитете. Они участвуют в регулировке выработки интерферонов 1 типа. Фрагментация митохондрий приводит к снижению уровней интерферонов. Так, miR-aU14 снижал выработку IFNβ. В отсутствие интерферонов герпесвирус может быть реактивирован. Интересно, что эктопическая экспрессия miR-aU14 может индуцировать вирусную реактивацию.
Пока неясно, как конкретно вирусные микроРНК участвуют в реактивации вируса. Авторы предполагают, что другие герпесвирусы используют схожие механизмы при реактивации. Понимание этих механизмов может привести к разработке терапии, позволяющей подавить реактивацию вируса герпеса или, наоборот, реактивировать вирус по команде для элиминации зараженных клеток.
Источник
Hennig T., et al. Selective inhibition of miRNA processing by a herpesvirus-encoded miRNA // Nature (2022), published May 04, 2022, DOI: 10.1038/s41586-022-04667-4


 Меню
Меню





 Все темы
Все темы




 0
0