Блокировка некроптоза защищает легкие от повреждения при гриппе
Заражение вирусом гриппа А может индуцировать некроптоз клеток легких. Авторы статьи в Nature показали на мышах, что ингибитор протеинкиназы RIPK3, ответственной за развитие некроптоза при вирусных инфекциях, уменьшает воспалительные процессы в тканях легких при тяжелом течении гриппа А, снижает риск развития острого респираторного дистресс-синдрома и смерти, не ограничивая при этом иммунные реакции организма, необходимые для борьбы с инфекцией.
При вирусной инфекции активируются процессы уничтожения зараженных клеток: апоптоз и некроптоз, запускаемый ферментом RIPK3. Некроптоз способствует развитию гипервоспаления легких и острого респираторного дистресс-синдрома (ОРДС), для которого на данный момент не существует эффективных способов терапии. Исследования на мышах показали, что препарат UH15–38, ингибирующий RIPK3, блокирует некроптоз в клетках альвеолярного эпителия, тем самым приводя к уменьшению воспаления тканей легких и снижению риска смерти.
Вирусам для репликации необходимы живые клетки, поэтому программируемая гибель зараженных клеток служит наиболее эффективным методом борьбы организма с вирусной инфекцией. Существует два основных механизма уничтожения инфицированных вирусом клеток: апоптоз (активируется ферментами каспазами и приводит к образованию апоптотических телец, которые быстро поглощаются макрофагами) и некроптоз (активируется киназой RIPK3 и приводит к разрушению клетки и запуску воспалительного процесса). Некроптоз сопровождается существенно более выраженным иммунным ответом, чем апоптоз, и приводит к большему повреждению тканей, а при тяжелом течении заболевания — к цитокиновому шторму и, как следствие, к ОРДС. То есть, для инфицированного организма апоптоз безопаснее — он ограничивает размножение вируса и при этом обеспечивает адекватный иммунный ответ.
В ходе эволюции некоторые вирусы научились активировать некроптоз — именно так поступает вирус гриппа А. При заражении им белок инфицированной клетки-хозяина ZBP1 связывается с вирусной Z-РНК и активирует фермент RIPK3, который фосфорилирует и активирует киназу MLKL, повреждающую плазматическую мембрану. В результате развивается некроптоз, вызывающий некроз легочных тканей, патологическое рекрутирование нейтрофилов и воспаление легких. Активированный при вирусной инфекции RIPK3 параллельно запускает и каспаза-8-зависимый апоптоз, которого достаточно, чтобы справиться с вирусом гриппа без таких разрушительных последствий. При этом запуск апоптоза возможен и по механизмам, не задействующим RIPK3, а для некроптоза этот белок необходим — это делает его привлекательной терапевтической мишенью.
В качестве потенциального ингибитора RIPK3 ученые выбрали UH15-38 — малую молекулу, которая взаимодействует с АТФ-связывающим карманом киназы RIPK3 и мыши, и человека и тем самым блокирует ее работу.
Эксперименты проводились на клеточных культурах (мышиные эмбриональные фибробласты и человеческие клетки HeLa, в которых экспрессировали RIPK3) и на мышах. Для заражения авторы статьи использовали вирус гриппа А/Puerto Rico/8/1934 (H1N1). На начальном этапе исследования они показали, что у мышей, лишенных гена, кодирующего фермент MLKL (линия Mlkl-/-), не развивался RIPK3-индуцированный некроптоз, что позволяло смоделировать ситуацию ингибирования киназы RIPK3 при тяжелом заболевании гриппом А in vivo.
Опыты на клетках показали, что UH15-38 полностью ингибировал активацию RIPK3, фосфорилирование MLKL и последующий некроптоз. Апоптоз он при этом не индуцировал даже в дозе 50 × IC50.
Для проверки терапевтических качеств UH15-38 мышей дикого типа заражали летальной дозой (6000 × EID50 — средней инфицирующей дозы для куриного эмбриона) вируса гриппа А. UH15–38 вводился внутрибрюшинно, начиная с первого дня после инфекции раз в день; и авторы оценивали выживаемость и скорость потери веса. Ученые протестировали дозы от 7,5 до 50 мг/кг. Согласно полученным данным, всего 7,5 мг/кг UH15–38 в день обеспечивали выживание 40 % зараженных мышей; максимальная выживаемость (80 %) наблюдалась при использовании дозы 30 мг/кг. При отсроченном на два или три дня после инфицирования введении эта доза также снижала потерю веса и смертность. При уменьшении количества вводимого вируса (до дозы, убивающей 60% зараженных животных) UH15–38 защищал от гибели всех инфицированных мышей даже при низких дозах препарата и отсрочке начала терапии до пяти дней с момента введения вируса.
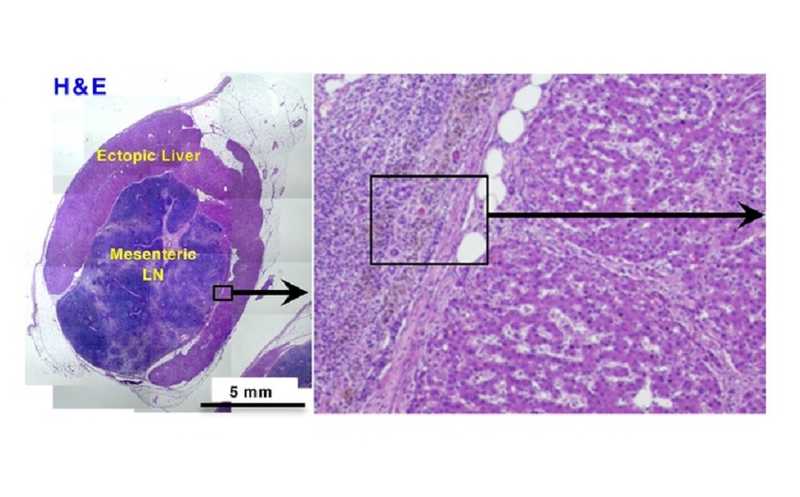
Анализ тканей легких показал, что UH15-38 практически не влияет на количество инфицированных клеток, подвергающихся апоптозу, но при этом предотвращает выброс провоспалительных цитокинов и хемокинов (IL-1β, IL-6, IL-18, TNF) и уменьшает степень фиброзного поражения легких. Однако авторы отмечают, что UH15-38 эффективен при гриппозных инфекциях и при поражениях легких иной природы, но не при заражении SARS-CoV-2.
Таким образом, RIPK3-зависимый некроптоз не является необходимым для борьбы с вирусной инфекцией и даже вреден при летальных дозах вируса гриппа А. Ингибитор RIPK3 UH15–38 в низких дозах избирательно блокирует некроптоз, не воздействуя на пути апоптоза; он также не влияет на другие сигнальные пути, связанные с воспалением и не ингибирует другие, родственные RIPK3 киназы. Эффект UH15-38 наблюдается при введении его в период до 5 дней после заражения, чем он выгодно отличается от осельтамивира и занамивира, применять которые следует в первые 48 часов инфекции.
Ежегодно заражение вирусами сезонного гриппа А приводит к тяжелому течению болезни в 5 млн случаев и становится причиной 650 тыс. смертей во всем мире. Вирусы гриппа А вызывают сезонные эпидемии и обладают существенным пандемическим потенциалом. В то же время существующие вакцины и многие противовирусные препараты недостаточно эффективны. Возможность контролировать гибель зараженных клеток, ограничивая процесс размножения вируса и поражения окружающих тканей, способна стать действенным средством для терапии не только в случае инфицирования вирусом гриппа А, но и при других поражениях легких. Авторы работы в настоящее время создают компанию Vaayu Therapeutics, чтобы разработать аналоги UH15–38, пригодные для применения на людях.


 Меню
Меню





 Все темы
Все темы





 0
0