Сочетание ингибитора нейраминидазы с нейтрализующими антителами оказалось эффективнее любой монотерапии гриппа
Канадские исследователи из Университета Макмастера в экспериментах на мышах доказали эффективность комбинированной терапии гриппа bNab-NA. Она включает противовирусный препарат, ингибитор нейраминидазы, и нейтрализующие антитела, нацеленные на стеблевой домен гемагглютинина. Комбинация bNab-NA оказалась эффективнее любой монотерапии гриппа и может быть полезна как для лечения, так для и профилактики инфекции.

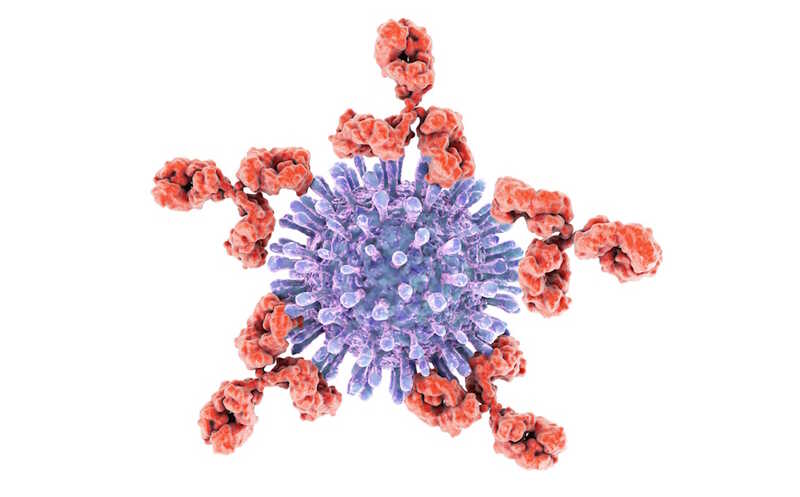
Ежегодно в мире заражаются гриппом 3–5 миллионов человек, из которых около полумиллиона погибают. Существующие вакцины обычно нацелены на головной домен гемагглютинина (HA) — гликопротеина, который расположен на поверхности липопротеиновой оболочки вируса. Из-за антигенного дрейфа головной домен HA постоянно меняется, возникают новые штаммы вируса гриппа, поэтому противогриппозные вакцины необходимо ежегодно обновлять. В новых разработках предлагается использовать более стабильный стеблевой домен HA, против которого будут вырабатываться нейтрализующие антитела широкого спектра (bNAbs). Они действуют, связываясь своим Fc-фрагментом с рецепторами на эффекторных иммунных клетках, а Fab-фрагментом со стеблевым доменом HA. Это взаимодействие называется антителозависимой клеточной цитотоксичностью (ADCC). Для оптимальной работы этих антител необходимо дополнительное связывание остатков сиаловой кислоты на эффекторных клетках с головным доменом HA.
Другой гликопротеин на поверхности вируса — нейраминидаза (NA) — может разрывать связь между сиаловой кислотой и головным доменом, что препятствует эффективной ADCC. Таким образом, ингибирование NA с помощью таких препаратов, как осельтамивир, может усиливать эффект ADCC, вызванный антителами широкого спектра.
Канадские ученые под руководством Мэттью Миллера из Университета Макмастера проанализировали взаимное влияние препаратов — ингибиторов NA и bNAbs —на стеблевой домен HA и в экспериментах на мышах доказали эффективность их совместного применения.
Исследователи смоделировали процесс активации и дегрануляции NK-клеток по пути ADCC. Для этого они использовали Т-клеточную линию человека Jukat и мышиные антитела bNAb 6F12. Т-клетки предварительно модифицировали — экспрессировали в них мышиный Fc-рецептор и фермент, вызывающий биолюминесценцию при активации ADCC. На этой клеточной линии они изучили степень ADCC, возникающей при применении мышиных bNAbs отдельно и в сочетании с осельтамивиром. Результаты показали повышенные уровни клеточной цитотоксичности при применении осельтамивира, коррелирующие с дозой препарата. Интересно, что степень повышения цитотоксичности зависела от штамма вируса и использованных антител. Тот же опыт, но проведенный с мутантными антителами, не позволявшими связываться Fc-фрагменту с его рецептором, показал полное отсутствие активации эффекторных клеток. Это доказывает, что эффект от осельтамивира достигается не из-за суммации действий ингибитора и bNAbs, а именно вследствие их совместной перекрестной активации ADCC.
Дальнейшее переливание зараженным гриппом мышам сыворотки людей с высоким и низким содержанием bNAbs и применение осельтамивира показали, что эффективность препарата была прямо пропорциональна титру антител.
Таким образом, ученым удалось на мышах показать эффективность совместного использования ингибиторов нейраминидазы и нейтрализующих антител широкого спектра, направленных на стеблевой домен гемагглютинина. Осталось провести клинические испытания на людях, необходимые для подтверждения терапевтической пользы такой комбинации для эффективного лечения больных гриппом. Исследователи надеются, что ее использование сможет продлить срок действия современных противовирусных препаратов, потому что вирусы вряд ли выработают к ним устойчивость из-за сочетания с антителами.
Источник
Zhang A., et al. Hemagglutinin stalk-binding antibodies enhance effectiveness of neuraminidase inhibitors against influenza via Fc-dependent effector functions // Cell Reports Medicine, Volume 3, Issue 8, 100718. Published on August 16, 2022. DOI: 10.1016/j.xcrm.2022.100718


 Меню
Меню





 Все темы
Все темы




 0
0