Аутоиммунное заболевание мозга вызывается противоопухолевым иммунитетом
Энцефалит, вызванный антителами к NMDA-рецепторам клеток мозга, часто встречается у молодых женщин и может заканчиваться как быстрой ремиссией, так и летальным исходом. Его развитие может провоцироваться онкологическим заболеванием, если опухоль экспрессирует NMDA-рецепторы и против нее развивается иммунный ответ. В лаборатории Колд-Спринг-Харбор детально изучили иммунологические механизмы, которые связывают опухоли молочной железы, экспрессирующие этот белок, и энцефалит. Они показали, в частности, что не все антитела к рецептору способствуют развитию неврологической патологии.
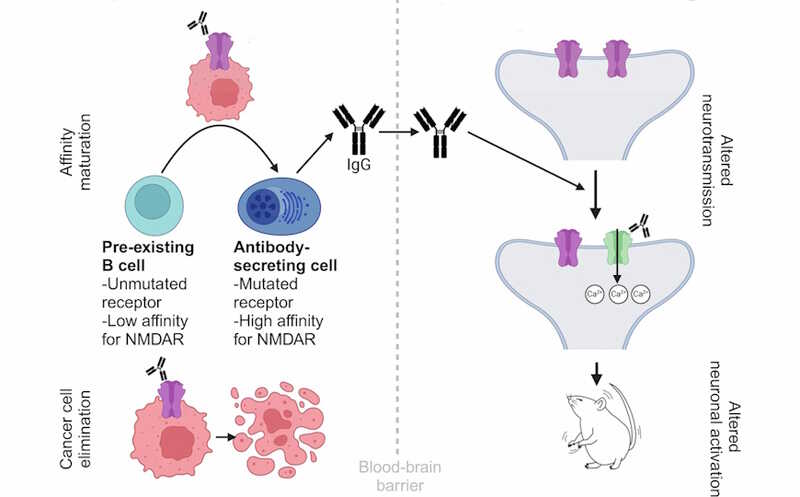
Если опухоль экспрессирует NMDAR, противоопухолевое антитело может вызвать энцефалит
Credit:
Nature. 2026. DOI: 10.1038/s41586-026-10278-0 | CC BY-NC-ND 4.0
Анти-NMDA-рецепторный энцефалит (Anti-NMDA receptor encephalitis, ANRE), — одна из самых распространенных форм аутоиммунного энцефалита. Он встречается главным образом у молодых женщин и вызывает психоз, резкие изменения личности, нарушения памяти, судороги и дисфункцию вегетативной нервной системы, в тяжелых случаях возможен летальный исход. Причиной ANRE часто бывает опухоль, локализованная вне мозга, которая экспрессирует NMDA-рецепторы (NMDAR). У здоровых людей эти рецепторы экспрессируются в головном мозге и контролируют синаптическую пластичность. Предполагается, что против NMDAR, экспрессируемого опухолью, развивается системный иммунный ответ, который вызывает ANRE. У пациентов с этой формой энцефалита были обнаружены антитела к NMDAR, а хирургическое удаление опухоли и иммуносупрессия могут излечить ANRE.
Для лечения ANRE предлагается также блокировать участки на субъединице NMDA-рецептора, с которыми взаимодействуют аутоантитела. (Одну из таких работ мы упоминали в недавнем выпуске «Утреннего кофе».) Однако иммунологические механизмы, связывающие противораковый иммунитет с аутоиммунной реакцией, — в частности, появление антител, вызывающих заболевания, и структура комплексов NMDAR-антитело, — еще недостаточно изучены.
Сотрудники лаборатории Колд-Спринг-Харбор (США) с коллегами из других научных центров детально исследовали эти механизмы. Они подтвердили, что клетки трижды негативного рака молочной железы (ТНРМЖ) человека экспрессируют NMDAR, как методами РНК-секвенирования и пространственной транскриптомики, так и с помощью иммунофлуоресцентного анализа. Затем они создали модель ТНРМЖ у мышей с возможностью индуцировать в опухоли экспрессию NMDAR. Это позволяло изучать иммунный ответ в реальном времени.
При развитии специфического иммунного ответа определенная подгруппа B-клеток, имеющих рецепторы к антигену, начинает вырабатывать антитела против этого антигена. Авторы выделили B-клетки, связывающиеся с NMDAR, из опухолей мышей и близлежащих лимфатических узлов, и реконструировали их эволюционную историю. В ходе процесса, называемого созреванием аффинности, в генах иммунных клеток, кодирующих рецепторы и антитела, возникают мутации, и появляются клеточные клоны, способные прочнее связывать антиген, чем исходные клетки. Секвенирование соответствующих участков генов в единичных клетках позволяет реконструировать этот процесс.
NMDAR в опухолях мышей привлекал В-клетки и индуцировал созревание аффинности. Примечательно, что у мышей с самыми высокими уровнями антител опухоли регрессировали быстрее. Авторы также подтвердили появление у них высокоаффинных антител, происходящих от низкоаффинных.
Взаимодействие антител с NMDAR на атомном уровне исследовали методом криоэлектронной микроскопии. Все исследованные антитела взаимодействовали с внеклеточным N-концевым доменом NMDAR, причем сайты связывания мышиных антител и антител, полученных от пациентов, перекрывались. Взаимодействие с антителами по-разному влияло на свойства рецептора — его активность могла повыситься или снизиться, в зависимости от вызванных конкретным антителом конформационных изменений.
Также авторы проверили, могут ли очищенные антитела против NMDAR, введенные в мозг мыши, вызвать неврологические заболевания. Когда антитело, усиливающее действие рецептора, ввели в желудочки головного мозга, это вызывало у животных вегетативную дисрегуляцию, повышение температуры тела, возрастал риск эпилептических припадков.
Таким образом, аутоиммунные заболевания могут быть прямым следствием противоракового иммунного надзора. Одна и та же субпопуляция B-клеток, распознающих NMDAR, вырабатывает антитела, которые замедляют рост опухоли, но в то же время вызывают неврологические заболевания. Авторы предполагают, что аутоиммунные патологии, опосредованные этим механизмом, могут возникать у людей, чьи опухоли были уничтожены иммунной системой. «У пациентов с аутоиммунными заболеваниями часто это состояние возникает внезапно, — говорит первый автор статьи Сэм Клеман. — Оно может быть связано с раком, о существовании которого вы даже не подозревали».
Понятно, что реальная клиническая ситуация может быть сложнее. В эксперименте антитела вводили в мозг мышей напрямую, но в реальности они должны были преодолеть гематоэнцефалический барьер, чем-то нарушенный. Авторы использовали только одну линию опухолевых клеток, модифицированных для экспрессии NMDAR, тогда как человеческие опухоли отличаются высоким разнообразием. Кроме того, изучался лишь один вариант антител, и выборка пациентов была ограничена.
Исследователи также обнаружили, что 8 из 53 (15%) пациенток с ТНРМЖ в крови обнаруживаются антитела к NMDAR в количестве выше нормы. Интересно, что их присутствие коррелировало с благоприятными клиническими исходами: ни у одной из этих пациенток онкозаболевание не прогрессировало несколько лет.
В дальнейшем авторы планируют исследовать роль нарушения ГЭБ в развитии ANRE, детальнее охарактеризовать гуморальный ответ при этом состоянии и наметить стратегии лечения неврологических иммунных заболеваний, которые не снижали бы противоопухолевый иммунитет.
«Один и тот же иммунный ответ против опухоли может производить антитела с совершенно противоположным воздействием на мозг, — объясняет один из руководителей работы Хиро Фурукава, проводивший исследования методом криоэлектронной микроскопии. — Понимание того, какие антитела вредны, а какие защищают, в итоге может помочь нам разработать методы лечения, которые сохранят способность иммунной системы бороться с раком, предотвращая при этом неврологические повреждения».
Польза кетогенной диеты при эпилепсии может быть связана с изменением транскриптома гиппокампа
Источники
Kleeman, S.O., et al. Ectopic NMDAR expression in cancer unmasks germline-encoded autoimmunity // Nature. 2026. DOI: 10.1038/s41586-026-10278-0
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы
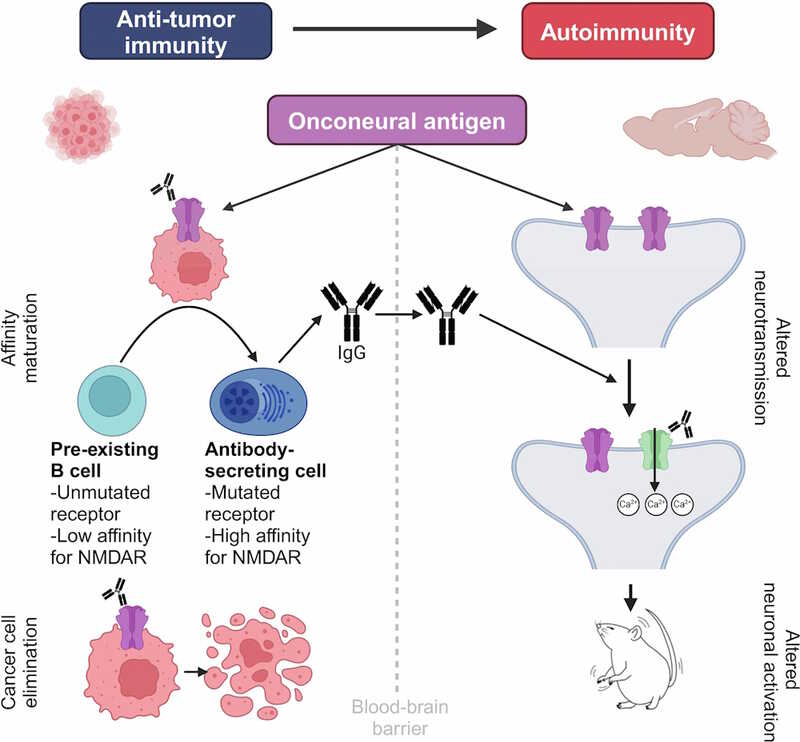 Credit: Nature. 2026. DOI:
Credit: Nature. 2026. DOI:



 0
0