Гипервирулентному штамму M. tuberculosis помогает адаптироваться к антибиотикотерапии отключение фермента, синтезирующего триацилглицериды
Исследование ученых из Санкт-Петербурга показало, что во время многомесячного лечения мышей, зараженных гипервирулентным штаммом Mycobacterium tuberculosis, произошел отбор микобактерий с мутацией, инактивирующей ген tgs3. Ген связан с липидным обменом и способствует дормантности (переходу в состояние покоя), что обеспечивает персистенцию патогена, а его отключение, напротив, приводит к усилению роста микобактерий. Уже после двух месяцев лечения новыми антибиотиками доля мутантного аллеля выросла с 10 до 70%.
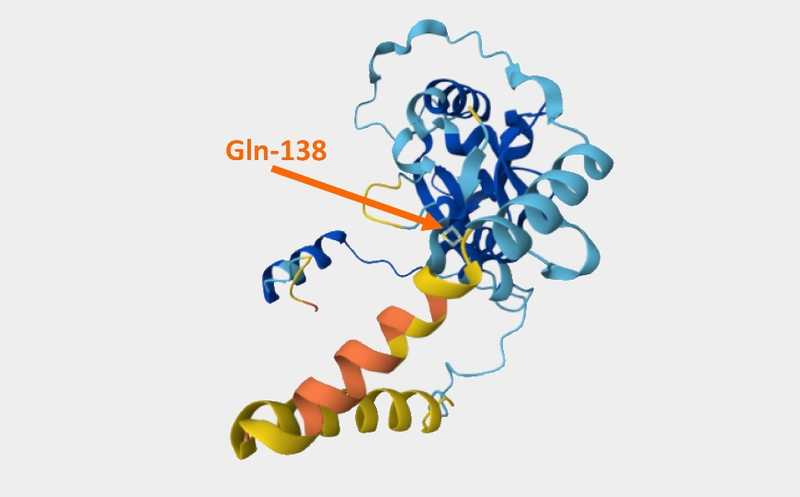
Триацилглицеролсинтаза Tgs3 M. tuberculosis. Стрелкой показан кодон 138 (глутамин). В результате мутации он заменяется стоп-кодоном, что приводит к продукции укороченного варианта белка
Источник:
Репертуар факторов вирулентности и способы адаптации к человеческому организму отличаются у филогенетически различных штаммов M. tuberculosis. Это было продемонстрировано в моделях in vivo и на макрофагах. Внутривенное инфицирование резистентных мышей C57BL/6 — хорошая модель для изучения как бактериальной вирулентности, так и длительного лечения лекарственно-устойчивого туберкулеза. При этом в условиях иммунного ответа организма-хозяина разные штаммы используют различные стратегии адаптации, что может привести к отбору полезных мутаций в генах, не имеющих прямого отношения к резистентности.
Ученые из Санкт-Петербурга исследовали адаптации значимых штаммов M. tuberculosis к химиотерапии в мышиной модели (линия C57BL/6). Изучались патогенные свойства хорошо охарактеризованных мультирезистентных штаммов M. tuberculosis, принадлежащих к генотипам Beijing и LAM. Контрольные группы животных не получали лечения, экспериментальные получали адекватную химиотерапию препаратами нового поколения. После 2 и 5,5 месяцев лечения мышей подвергали эвтаназии и исследовали на наличие патологических изменений, бактериальную нагрузку и биохимические показатели поражения печени. Для изолятов, выделенных из легких, выполняли полногеномное секвенирование.
В ходе этого исследования у мышиных изолятов M. tuberculosis ранее были выявлены мутации лекарственной устойчивости (подробнее на PCR.NEWS). Мутаций устойчивости к применяемым препаратам нового поколения не возникло, поскольку лечение было адекватным и непрерывным. Новый анализ был направлен на детальное изучение всего массива геномных данных.
При сравнении с геномами исходных штаммов новых мутаций было найдено очень мало, и тем больший интерес они представляют. Наиболее примечательной оказалась мутация в гене tgs3 (кодон 138 Gln>Stop), выявленная во всех изолятах из легких мышей, зараженных гипервирулентным штаммом Beijing 396 («бурятский субтип») и получавших химиотерапию. Эта мутация приводит к образованию наполовину укороченного и нефункционального белка. Однако tgs3 не был инактивирован полностью: мутантные аллели обнаружены в среднем в 65% ридов. Эта мутация уже была в геноме родительского штамма, но только в 9% клеток. Ее доля выросла до 59–100% (в среднем 68%) в мышиных изолятах после двух месяцев лечения, но несколько снизилась (до 38–79%, в среднем 63%) после 5,5 месяцев лечения (P = 0,04). Это очевидно отражает нелинейную динамику адаптации микроба.
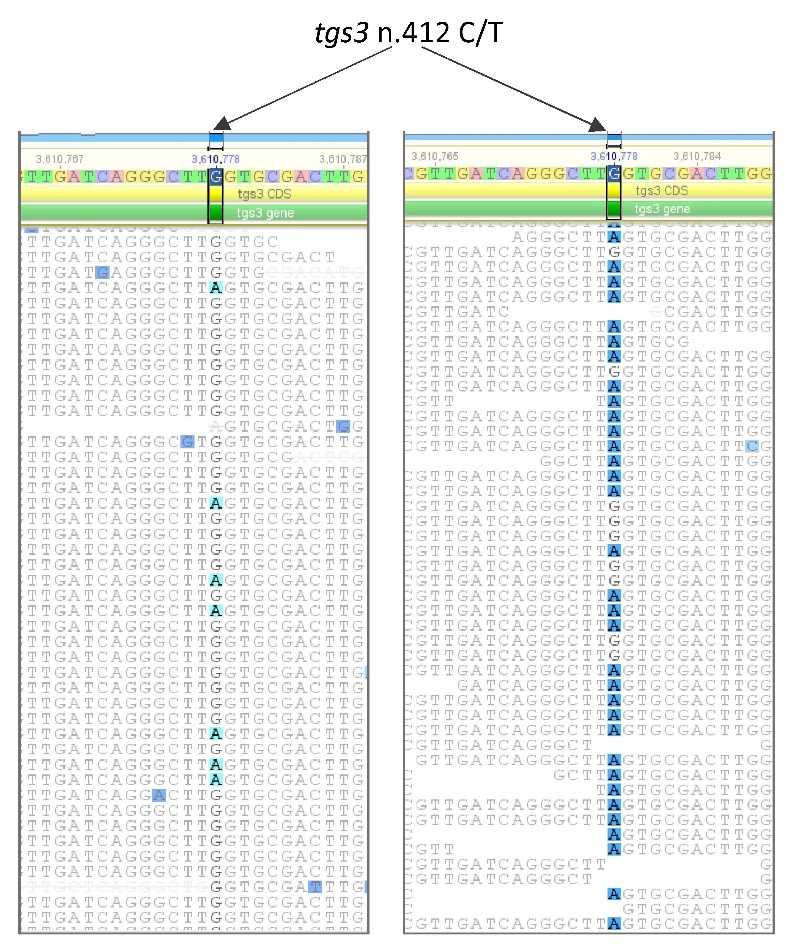 Картирование коротких нуклеотидных прочтений полногеномного секвенирования на геном референс-штамма H37Rv. Показан фрагмент последовательности гена tgs3 с мутацией в кодоне 138 Gln>Stop (CAA>TAA) (мутантная позиция в геноме 3610778 G>A показана стрелками). Слева исходный штамм 396, справа изолят из легких мыши после 5,5 месяцев лечения. Credit: Игорь Мокроусов
Картирование коротких нуклеотидных прочтений полногеномного секвенирования на геном референс-штамма H37Rv. Показан фрагмент последовательности гена tgs3 с мутацией в кодоне 138 Gln>Stop (CAA>TAA) (мутантная позиция в геноме 3610778 G>A показана стрелками). Слева исходный штамм 396, справа изолят из легких мыши после 5,5 месяцев лечения. Credit: Игорь Мокроусов
Ген tgs3, кодирующий фермент триацилглицеролсинтазу, регулирует липидный обмен, накопление энергии и адаптацию к стрессу. Повышенная продукция триацилглицеридов, видимо, способствует адаптации и персистенции M. tuberculosis через дормантность (состояние покоя).
По мнению руководителя проекта д.б.н. И.В. Мокроусова (Институт им. Пастера), снижение экспрессии tgs3 в изолятах от мышей, зараженных гипервирулентным и высоколетальным штаммом Beijing 396 и получавших химиотерапию, может отражать особенности адаптивной стратегии этого штамма, основанной на усилении роста, особенно в первые месяцы селективного давления антибиотикотерапии. Малого (9%), но не ничтожного количества мутантных клеток в исходном штамме было достаточно для классического положительного отбора. Имея мутацию, благоприятную для выживания, бактериальная субпопуляция с нефункционирующим Tgs3 значимо увеличила свою долю у всех животных, зараженных штаммом 396. Вероятно, мутация tgs3 138 Gln>Stop усиливала рост этого штамма у инфицированных животных в условиях химиотерапии новыми антибиотиками. Точная роль этой и других мутаций, выявленных в исследуемых штаммах, требует дальнейшего изучения в экспериментах с заменой аллелей и нокаут-мутантов.
Работа выполнена при поддержке РНФ (грант 24-44-00004, руководитель проекта — д.б.н. И.В. Мокроусов (Санкт-Петербургский НИИ эпидемиологии и микробиологии имени Пастера).
Источник
Vinogradova T., et al. Long-term chemotherapy of C57BL/6 mice infected with epidemiologically important Mycobacterium tuberculosis strains and molecular insight into host-pathogen interplay // Microbial Pathogenesis. 2025; 207: 107919. DOI: 10.1016/j.micpath.2025.107919


 Меню
Меню





 Все темы
Все темы



 0
0