Альвеолярные макрофаги, пересаженные мыши после длительного культивирования, восстанавливают свои характеристики
Ученые из Франции и Германии показали, что при длительном культивировании ex vivo альвеолярные макрофаги сохраняют экспрессию ключевых генов. Изменения, произошедшие с клетками в культуре, обратимы при пересадке клеток обратно в легкие мыши. Авторы считают, что это свойство позволит разработать новые подходы в клеточной терапии.
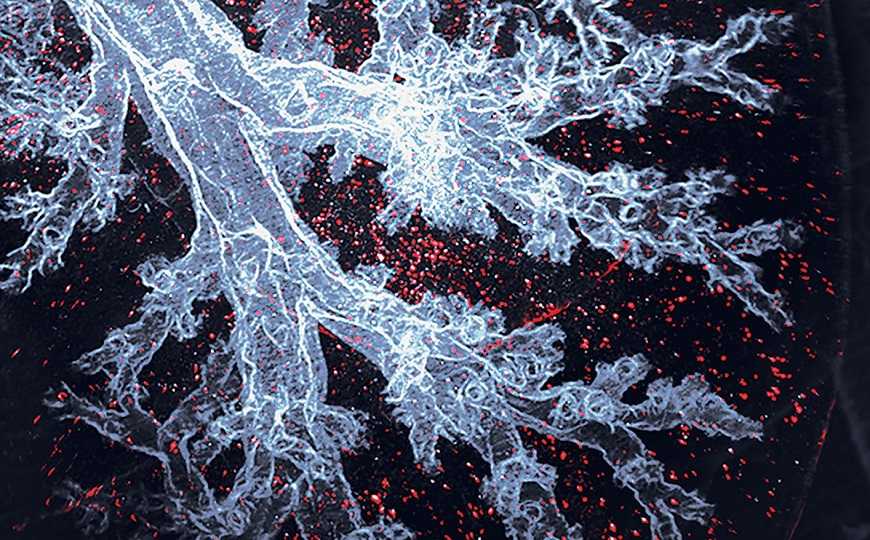
Альвеолярные макрофаги (красные) в легких мыши.
Credit:
Sara Gholamhosseinian Najjar and Michaela Burkon | Пресс-релиз
Резидентные (тканевые) макрофаги можно обнаружить во всех тканях тела; они выполняют разнообразные функции, связанные с поддержанием гомеостаза, иммунным ответом и самообновлением организма. В различных органах макрофаги образуют популяции, которые фенотипически отличаются друг от друга. Известно, что пересадка макрофагов из других тканей в легкие меняет их фенотип, а при культивировании ex vivo альвеолярные макрофагы теряют экспрессию тканеспецифических генов. Вероятно, это связано с потерей сигналов окружающей среды. Остается неизвестным, обратимы ли эти изменения, и сохраняют ли макрофаги чувствительность к специфичным сигналам внешней среды после длительного культивирования. Ответы на эти вопросы получили исследователи из Франции и Германии.
В настоящее время макрофаги при культивируют в основном получают при дифференцировке из клеток-предшественников, при этом формируются гетерогенные популяции клеток, которые можно использовать в течение короткого промежутка времени. Авторы выращивали мышиные макрофаги, полученные при бронхоскопии, ex vivo в среде, содержащей колониестимулирующие факторы для гранулоцитов и макрофагов. Им удалось культивировать клетки на протяжении десяти месяцев. Кроме того, эти макрофаги выдерживали несколько циклов заморозки и разморозки.
Затем ученые проверили фенотипические характеристики и функции культивируемых макрофагов. Они продемонстрировали характерные для этих клеток особенности, например, способность к фагоцитозу и формированию подкисленных лизосом. Кроме того, симуляция инфекции — добавление в культуру липидосахаридов Escherichia coli — приводила к повышенной выработке активных форм кислорода.
РНК-секвенирование показало, что некоторые ключевые гены, специфичные для альвеолярных макрофагов, экспрессировались как у свежевыделенных клеток, так и у культивируемых. Тем не менее, профиль экспрессии специфичных генов все же изменялся в ответ на изменение условий окружающей среды. Например, культивация повлияла на гены, связанные с липидным метаболизмом, адгезией и аутокринной передачей сигнала для самообновления популяции.
Затем ученые проверили, восстанавливают ли альвеолярные макрофаги свои характерные особенности при пересадке обратно в легкие мыши. Они обнаружили, что после длительного культивирования (два месяца) альвеолярные макрофаги способны стабильно заселять ткани животных как минимум на протяжении четырех месяцев, составляя 5–15% от всех макрофагов. При этом экспрессия тех генов, которые отличают их от других популяций резидентных макрофагов, полностью восстанавливалась после трансплантации в легкие мыши. Это означает, что адаптация клеток к условиям длительного культивирования обратима. Этот вывод также подтвердил анализ доступности хроматина: большинство участков после трансплантации вернулись в изначальное состояние.
Наконец, пересадка таких макрофагов мышам с нокаутом гена Csf2rb, у которых отсутствуют собственные альвеолярные макрофаги, оказалась крайне эффективной: спустя восемь месяцев в легких мышей было почти столько же макрофагов, сколько и у мышей дикого типа. Кроме того, микроскопическое исследование показало, что количество накопленных из-за отсутствия макрофагов слизи и клеточных остатков в альвеолярной жидкости у этих животных также сократилось.
Таким образом, авторы продемонстрировали, что эпигенетические изменения в культуре альвеолярных макрофагов обратимы после трансплантации обратно в организм. Также обратимы и остальные признаки адаптации клеток к культивации, такие как изменения в клеточной адгезии, миграции и особенностях метаболизма. Авторы считают, что выращивание макрофагов позволит создать новый подход к клеточной терапии: в отличие от Т-клеточной терапии, которая больше подходит для лечения онкологических заболеваний крови, макрофаги могли бы помочь при лечении солидных опухолей.
Источник
Subramanian, S. et al. Long-term culture-expanded alveolar macrophages restore their full epigenetic identity after transfer in vivo. // Nature Immunology (2022), published February 24, 2022. DOI: 10.1038/s41590-022-01146-w


 Меню
Меню





 Все темы
Все темы





 0
0











