Антибиотики Novltex преодолевают множественную лекарственную устойчивость
Международная группа ученых разработала Novltex — новый класс антибиотиков, эффективный против патогенов со множественной лекарственной устойчивостью. Антибиотики Novltex представляют собой модифицированные соединения недавно открытого класса Novo29 из β-протеобактерий. Авторы значительно повысили выход продукта и использовали для синтеза доступный треонин вместо дорогостоящего D-гидроксиаспарагина, что решает проблему масштабирования производства новых антибиотиков. Значения минимальной ингибирующей концентрации (МИК) Novltex были сопоставимы с МИК используемых в клинике антибиотиков.
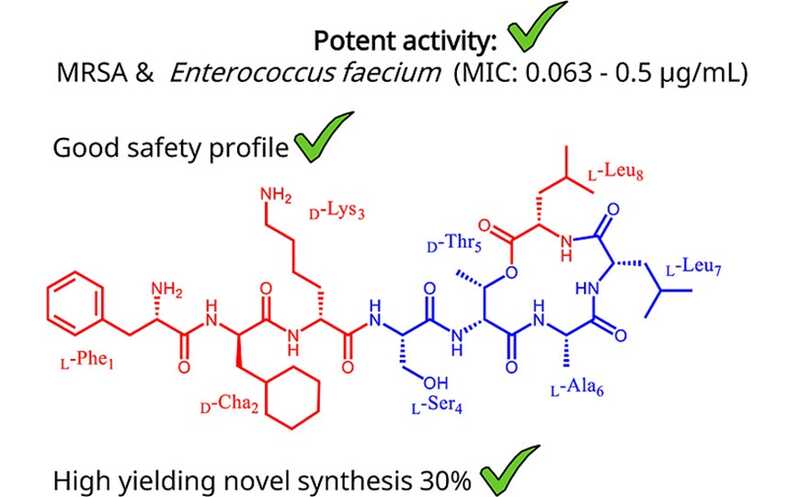
Credit:
Esra Malkawi, et al. // Journal of Medicinal Chemistry Article ASAP, DOI: 10.1021/acs.jmedchem.5c01193 || CC BY 4.0
Растущая устойчивость бактерий к существующим антибиотикам — одна из главных проблем мирового здравоохранения. Ведутся поиски новых противомикробных препаратов. Международная группа ученых разработала новый класс антибиотиков, эффективный против патогенов со множественной лекарственной устойчивостью (МЛУ).
Отправной точкой для разработки новых антибиотиков послужил относительно недавно открытый класс антибиотиков Novo29 (также известный как кловибактин) из β-протеобактерий, который продемонстрировал высокую антимикробную активность. Макроциклическое кольцо Novo29 структурно похоже на Leu10-тейксобактин. Антибактериальная активность Novo29 обусловлена одновременным воздействием на пирофосфатные части нескольких предшественников пептидогликана (C55-PP, Lipid II и Lipid III) — мишеней, которые консервативны у бактерий, но отсутствуют в клетках млекопитающих.
Однако практическое использование Novo29 ограничено двумя серьезными проблемами: его синтез крайне сложен, имеет низкий выход (около 1%), также он требует включения дорогостоящего и не доступного коммерчески D-гидроксиаспарагина (D-Hyn5), что значительно увеличивает затраты на производство и масштабирование.
Чтобы решить эти проблемы, ученые выдвинули гипотезу, что объединение макроцикла Leu10-тейксобактина (при синтезе которого используется доступный и недорогой треонин вместо сложного D-Hyn5) с N-концевым «хвостом» Novo29 позволит создать новое вещество с антимикробными свойствами. Полученные гибридные антибиотики назвали Novltex.
Авторы разработали эффективную и высокопроизводительную методологию синтеза аналогов Novltex. Исследователи применили метод твердофазного пептидного синтеза (SPPS) с использованием коммерчески доступных компонентов и быстрого микроволнового связывания.
Новая платформа позволила заменить дорогой D-Hyn5 на недорогой треонин, при этом обеспечив значительно более высокий выход — от 25% до 30%, что делает процесс экономичным и подходящим для масштабирования. Время циклов связывания удалось сократить примерно до 10 минут.
Ученые синтезировали и протестировали библиотеку из 16 аналогов Novltex, чтобы систематически изучить влияние конфигурации аминокислот на антибактериальную активность.
Сначала исследователи синтезировали десять аналогов для изучения роли стереохимии в макроцикле и N-концевом «хвосте». В результате был выявлен Аналог 4 (D-Leu2) как наиболее перспективный. Он использовал конфигурацию макроцикла Leu10-тейксобактина и продемонстрировал многообещающую активность против метициллинрезистентного золотистого стафилококка (MRSA) с минимальной ингибирующей концентрацией (МИК) 2–4 мкг/мл, что было сопоставимо с действием антибиотика ванкомицина. Эти данные подтвердили, что правильное конформационное расположение аминокислот, особенно гидрофобных остатков (Phe1 и Leu2), имеет решающее значение, вероятно, для улучшения мембранных взаимодействий.
Обнаружив, что боковая цепь в позиции Leu2, предположительно, взаимодействует с бактериальной мембраной, ученые перешли к рациональной оптимизации структуры. Они выдвинули гипотезу, что замена Leu2 на гидрофобные остатки может усилить мембранное взаимодействие. Для этого была синтезирована новая серия аналогов (11–16), где Leu2 заменялся аминокислотами с циклическими гидрофобными боковыми цепями, например, циклогексилаланином (Cha). Этот целенаправленный дизайн привел к открытию Аналога 12 (Leu2Cha–Novltex), который показал самую высокую активность (МИК 0,25 мкг/мл). Интересно, что Аналог 12 оказался в 32 раза активнее, чем Аналог 11 (с более короткой цепью), что указывает, что необходима определенная гибкость и протяженности боковой цепи для эффективного взаимодействия с мембраной.
Аналог 12 был дополнительно протестирован против клинических штаммов МЛУ-патогенов, являющихся приоритетными для Всемирной организации здравоохранения (ВОЗ), включая MRSA и Enterococcus faecium. Он показал высокую эффективность (МИК 0,063–0,5 мкг/мл) против обоих типов МЛУ-штаммов. Его МИК были значительно ниже или сопоставимы с показателями используемых в клинике антибиотиков. В частности, против штаммов МЛУ E. faecium, устойчивых к ванкомицину, даптомицину, цефотаксиму, левофлоксацину и ампициллину, Аналог 12 проявил мощную ингибирующую активность (МИК 0,125–0,5 мкг/мл).
Особенно примечательна скорость действия нового соединения — оно способно значительно сокращать популяцию бактерий всего за 6 часов даже при относительно низкой концентрации. Для сравнения, ванкомицину требуется вчетверо больше времени и более высокая дозировка для достижения аналогичного эффекта. Важным преимуществом Аналога 12 является также отсутствие формирования устойчивых мутантов у бактерий при воздействии препарата.
Механизм действия нового антибиотика сохраняет принцип работы исходного соединения — он связывается с ключевым компонентом бактериальной стенки Lipid II, нарушая жизненно важные процессы клетки. Дополнительные исследования показали, что препарат вызывает деполяризацию цитоплазматической мембраны MRSA, что может объяснить его мощное бактерицидное действие.
Аналог 12 демонстрирует хороший профиль безопасности. Тестирование на различных типах человеческих клеток показало отсутствие токсического эффекта даже при концентрациях, значительно превышающих терапевтические дозы. Препарат также проявил низкую гемолитическую активность, что делает его потенциально пригодным для инъекционного введения.
По мнению авторов, аналоги Novltex могут лечь в основу разработки нового поколения антибиотиков. Синтез с использованием недорогих и коммерчески доступных компонентов решает ключевые проблемы масштабирования новых лекарств.
Из ранее не культивируемой бактерии выделен новый антибиотик
Источник:
Esra Malkawi, et al. Novltex: A New Class of Antibiotics with Potent Activity against Multidrug-Resistant Bacterial Pathogens─Design, Synthesis, and Biological Evaluation // Journal of Medicinal Chemistry Article ASAP, DOI: 10.1021/acs.jmedchem.5c01193


 Меню
Меню





 Все темы
Все темы




 0
0










