Автономный сенсор измеряет уровень кишечных метаболитов в реальном времени
Ученые из США разработали прототип проглатываемого прибора для измерения концентрации кишечных метаболитов. Прибор не требует батареи и генерирует электричество за счет реакций окисления глюкозы и восстановления кислорода. Полученное напряжение затем преобразуется в магнитный сигнал, частота которого зависит от концентрации глюкозы. Систему проверили на свиньях. В будущем возможно оснащение прибора дополнительными сенсорами, определяющими, например, pH или лекарственные препараты.
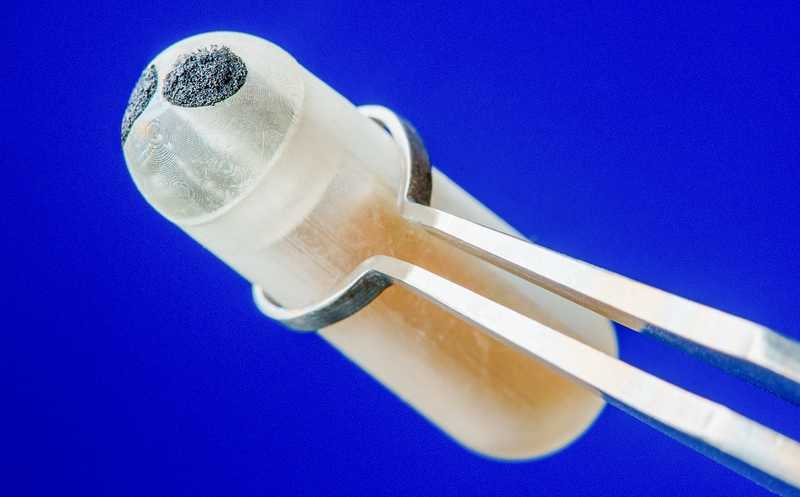
Один из пяти человек в течение жизни страдает тем или иным расстройством пищеварительного тракта. Метаболиты кишечных бактерий играют важную роль в развитии подобных заболеваний и, как следствие, являются одним из ключевых диагностических критериев. При этом существующие методы мониторинга кишечных метаболитов либо инвазивны, либо отсрочены по времени (например, анализ стула). Группа ученых из США представила концепт прибора, позволяющего автономно и в реальном времени измерять уровень кишечных метаболитов.
Проглатываемые устройства — один из наиболее перспективных методов мониторинга кишечных метаболитов, так как они позволяют измерять целый спектр параметров непосредственно в интересующей части организма в реальном времени. Одним из основных камней преткновения в их разработке является необходимость в источнике питания для обеспечения довольно высоких потребностей устройств беспроводной передачи сигнала. Большинство разработанных ранее приборов использовали батареи в качестве источника питания, однако подобное решение влечет за собой ряд проблем, включая большой размер устройства и риск отравлениями веществами, содержащимися в батарее, при нарушении герметичности.
В новой работе ученые представили концепт устройства, совмещающего процесс измерения уровня метаболитов с получением необходимого для передачи сигнала электричества. Для подтверждения функциональности системы ученые выбрали измерение уровня глюкозы в тонком кишечнике.
Устройство оснащено катодом и анодом, представляющими собой никелевую пену, покрытую углеродными нанотрубками. Оба электрода покрыты специфичными катализаторами. На аноде происходит окисление глюкозы с образованием глюконовой кислоты. На катоде восстанавливается кислород с образованием воды. Полученное в результате реакций напряжение передается на специально созданный чип, который преобразует его в магнитный сигнал, частота которого затем измеряется внешним прибором. Такой метод позволяет обеспечить гораздо лучшее проникновение сигнала сквозь ткани тела по сравнению с использованием электрического поля. Частота генерируемого системой сигнала зависит от напряжения, которое, в свою очередь, зависит от уровня глюкозы в окружающей среде, что позволяет напрямую переводить замеренные частоты в значение концентрации глюкозы.
Для прохождения кислой среды желудка устройство заключено в специальную капсулу, которая затем распадается в нейтральной среде кишечника. Электрические элементы системы изолированы при помощи покрытия из силикона и полиуретана. Устройство в защитной капсуле имеет длину 2,6 см и радиус 0,9 см.
Ученые протестировали систему в условиях, имитирующих пищеварительный тракт. В рамках данных экспериментов они оптимизировали толщину защитной капсулы и провели калибровку устройства при разных концентрациях глюкозы, кислорода и в различных температурах. Авторы также показали, что система генерирует необходимое для работы напряжение даже в отсутствии глюкозы, что может объясняться естественно возникающим между электродами напряжением, а также протеканием реакции восстановления кислорода.
In situ эксперименты проводились на свиной модели. Перед введением системы животных содержали на жидкой диете, а потом не кормили в течение 14 часов. Успешную доставку устройства в тонкий кишечник подтверждали рентгеновским снимком. В качестве контроля использовали анализы содержания глюкозы в крови с интервалом в 20 минут.
Животных напоили 360 мл физраствора, содержащими 60 ммоль/литр глюкозы, после чего кишечный уровень глюкозы (IGL) быстро повышался, пока не выходил на плато в 20–22 ммоль/литр, а также повышалось содержание глюкозы в крови (BGL), свидетельствующее о поглощении глюкозы из кишечника. Значения IGL были меньше, чем концентрация во вводимом растворе, что можно объяснить разбавлением раствора содержимым кишечника или же задержкой глюкозы в желудке.
При последовательном введении двух доз раствора наблюдался выход IGL сначала на одно плато, затем на второе, более высокое, в то время как BGL показывал стабильное повышение с небольшой задержкой.
Животным давали раствор глюкозы, а потом — равный объем раствора, не содержащего глюкозу. В результате IGL сначала выходил на плато, а потом резко снижался после введения «пустого» раствора, однако это снижение быстро сглаживалось. В то же время BGL показывал неравномерное, но стабильное повышение.
Ученые также продемонстрировали, что система может функционировать и без раствора глюкозы даже в голодавшем животном, вероятнее всего за счет кишечного сока, небольшое количество которого присутствует в кишечнике даже у голодающих животных.
Таким образом, ученые представили работающий прототип системы для автономного измерения кишечных метаболитов в реальном времени. Несмотря на то, что функциональность прототипа ограничена измерением уровня глюкозы, авторы отмечают, что на чип можно установить дополнительные сенсоры, включая системы измерения pH, уровня кислорода, и лекарственных препаратов.
Робокапсулу для пероральной доставки инсулина проверили на свиньях
Источник:
Ernesto De la Paz, et al. A self-powered ingestible wireless biosensing system for real-time in situ monitoring of gastrointestinal tract metabolites. // Nature Communications 13, 7405, published November 17, 2022. DOI: 10.1038/s41467-022-35074-y


 Меню
Меню





 Все темы
Все темы




 0
0