DUX4 вызывает отсутствие носа
Потеря функции гена SMCHD1 связана с врожденным отсутствием носа. В экспериментах in vitro ученые из США показали, что при выключении SMCHD1 активируется транскрипционный фактор DUX4. Это приводит к апоптозу при дифференцировке эмбриональных клеток в клетки эпидермальных плакод — предшественников обонятельного эпителия.
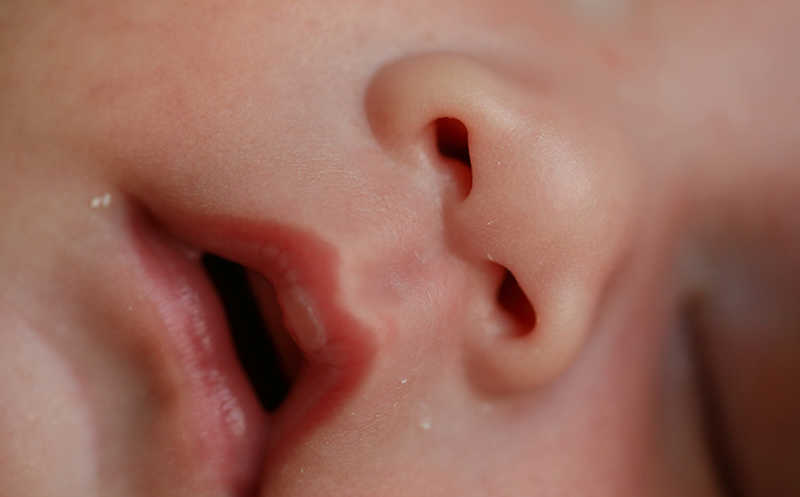
Врожденное отсутствие носа (ариния) — крайне редкий дефект, в течение последнего века было зарегистрировано меньше ста случаев. Ранее ученые из США описали роль мутаций гена SMCHD1 в развитии аринии. В новой работе эта же группа продемонстрировала влияние экспрессии транскрипционного фактора DUX4 на формирование дефекта.
Идентификация SMCHD1 как драйвера аринии стала неожиданностью, так как мутации в этом гене также приводят к развитию плече-лопаточно-лицевой мышечной дистрофии второго типа (facioscapulohumeral muscular dystrophy type 2, FSHD2). При FSHD2 потеря функции SMCHD1 приводит к гипометилированию региона субтеломерных макросателлитных повторов D4Z4 — участка ДНК, кодирующего фактор транскрипции DUX4. Гипометилирование запускает экспрессию DUX4, который индуцирует набор генов, связанных с оксидативным стрессом, повреждением ДНК и врожденным иммунитетом. Их совокупная экспрессия запускает апоптоз.
В новой работе ученые использовали культуры человеческих эмбриональных клеток линии H9. В клетках нокаутировали SMCHD1, а затем индуцировали их дифференциацию в клетки эпидермальных плакод — предшественников различных структур в голове эмбриона, в том числе обонятельного эпителия. Клетки H9 дикого типа (WT) развивались нормально. В то же время популяция нокаутных клеток стремительно снижалась на 3–4 день после дифференциации в клетки плакод. При этом в среде повышалось содержание лактатдегидрогеназы, что служит признаком апоптоза.
При более подробном изучении клеток с нокаутом SMCHD1 оказалось, что они не группируются, как нормальные клетки плакод. Иммунохимическое окрашивание маркеров межклеточной адгезии выявило изменения в морфологии клеток. Иммунофлуоресцентый анализ каспазы-3 подтвердил, что клеточная смерть вызвана апоптозом. Примечательно, что при индукции дифференциации SMCHD1 KO клеток в клетки нервного гребня они формировали нормальный фенотип без видимых дефектов морфологии, пролиферации и миграции.
РНК-секвенирование плакоидных клеток с нокаутом SMCHD1 в момент первых морфологических изменений выявило 1 061 генов с пониженной и 2 676 генов с повышенной экспрессией по сравнению с WT. В группе с наиболее выраженным повышением экспрессии преобладали гены-мишени DUX4. Дальнейший анализ мРНК показал увеличенные уровни DUX4 и его мишеней в SMCHD1 KO клетках. При этом ученые обнаружили, что гипометилирование D4Z4 не может считаться единственной причиной индукции DUX4, так как гипометилирование без экспрессии DUX4 наблюдалось в нокаутных клетках до дифференциации в плакоидные клетки и при дифференциации в клетки нервного гребня.
Восстановление экспрессии SMCHD1 в нокаутных клетках возвращало им нормальный фенотип. Такой же эффект наблюдался при ингибировании экспрессии DUX4 короткими РНК, образующими шпильки, или фармакологическими ингибиторами (ip300w).
На следующем этапе исследователи также провели эксперименты с индуцированными стволовыми клетками, полученными от пациентов с аринией, FSHD2 и здоровых контролей. При индукции дифференциации в плакоиды стволовые клетки пациентов с аринией демонстрировали экспрессию DUX4 и/или его генов-мишеней, чего не наблюдалось в контроле. Примечательно, что уровни экспрессии DUX4 варьировались и были ниже, чем в клеточных линиях SMCHD1 KO. Это соответствует данным о неодинаковой пенетрации мутаций SMCHD1, которые могут вызывать крайне широкий спектр симптомов — от отсутствия морфологических проявлений до аринии или тяжелых случаев FSHD2.
Наконец, ученые постарались установить хотя бы некоторые внешние факторы, влияющие на экспрессию DUX4. Ранее было показано, что ее индуцирует герпесвируса человека типа 1. И действительно, заражение клеток H9 герпесвирусом приводило к экспрессии DUX4, при этом в SMCHD1 KO клетках уровень экспрессии был выше.
Таким образом, исследователи получили новые данные о механизме, который связывает мутации в SMCHD1, индукцию экспрессии DUX4 и дефекты развития. Авторы отмечают, что необходимы дальнейшие исследования для установления факторов, регулирующих экспрессию DUX4.
Источник
Inoue, et al. DUX4 double whammy: The transcription factor that causes a rare muscular dystrophy also kills the precursors of the human nose // Science Advances? 9, eabq7744, published February 17, 2023. DOI: 10.1126/sciadv.abq7744


 Меню
Меню





 Все темы
Все темы




 0
0











