Как запретить иммунной системе атаковать бета-клетки при диабете
При диабете первого типа клетки иммунной системы атакуют и разрушают бета-клетки поджелудочной железы, вырабатывающие инсулин. Системное угнетение иммунитета может замедлить этот процесс, но опасно для здоровья. Авторы статьи в Science Advances разработали защитный препарат, нацеленный на сами бета-клетки. Эта белковая молекула связывается с пептидом, который присутствует на бета-клетках, но не на клетках других типов, а ее свободный конец взаимодействует с рецептором PD-1 на поверхности Т-клетки и подавляет ее активность.
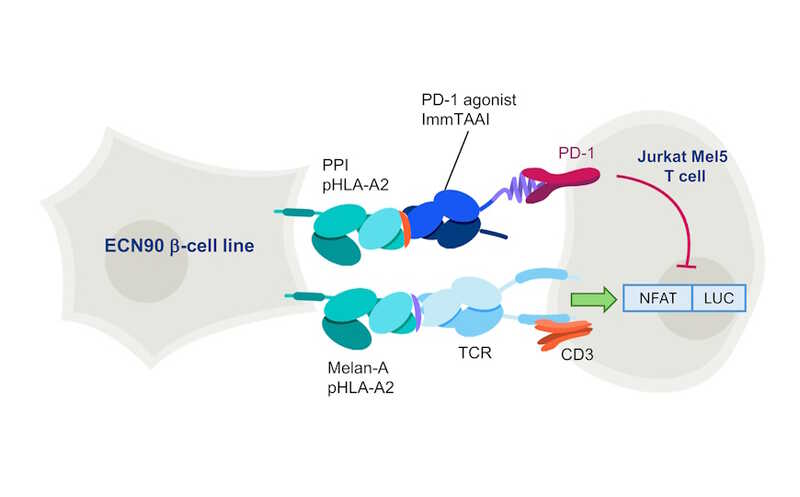
Разработанная авторами молекула (синий и сиреневый) садится на бета-клетку и ждет атаки Т-клетки, чтобы выключить ее
Credit:
Science Advances. 2026. DOI: 10.1126/sciadv.aec9029 | CC BY 4.0
Сахарный диабет первого типа — аутоиммунное заболевание, вызванное атакой Т-клеток на производящие инсулин бета-клетки поджелудочной железы. Системная иммуносупрессия может замедлить этот процесс, но она опасна для здоровья, и с этой точки зрения перспективнее стимулировать только местную толерантность в пораженном органе. Однако аутоиммунный ответ при диабете сложно регулировать в том числе потому, что он поликлонален — на момент постановки диагноза в организме присутствуют Т- и В-клетки, распознающие разные эпитопы островковых клеток. Один из возможных путей формирования иммунной толерантность в островках Лангерганса поджелудочной железы — воздействие на мишень, то есть на бета-клетки. В этом случае не обязательно определять все антигены бета-клеток или подавлять действие иммунной системы во всех тканях.
Уже проходят клинические исследования при аутоиммунных заболеваниях агонисты ингибиторных рецепторов иммунных клеток, в том числе агонисты рецептора клеточной смерти PD-1. Известно, что моноклональное антитело, нарушающее взаимодействие PD-1 с его лигандом PD-L1, ускоряет развитие диабета 1 типа у мышей. Подобные осложнения у людей вызывают противораковые антитела с аналогичным действием, а маркеры истощения Т-клеток, в том числе PD-1, коррелируют с положительными результатами лечения диабета.
Авторы статьи в Science Advances ранее разработали биспецифический агонист PD-1, который назвали ImmTAAI (immune modulating monoclonal TCR against autoimmunity — иммуномодулирующий моноклональный Т-клеточный рецептор против аутоиммунитета). Его таргетный, то есть распознающий клетку-мишень конец — это растворимый Т-клеточный рецептор, высокоспецифичный к пептиду препроинсулина PPI15–24. Препроинсулин — неактивный предшественник инсулина длиной 110 аминокислот, а его пептидные фрагменты презентируются на поверхности бета клеток (как и фрагменты всех белков, синтезируемых в клетке). В частности, PPI15–24 для презентации взаимодействует с HLA-A*02:01 (HLA-A2). Также у ImmTAAI есть эффекторный конец — наноантитело, которое является агонистом (активатором) PD-1.
Таким образом, молекула ImmTAAI связывается с бета-клеткой и «поджидает» аутоиммунный лимфоцит, распознающий любой антиген бета-клетки. Когда он пытается атаковать, эффекторный конец ImmTAAI взаимодействует с PD-1.
Ранее авторы показали, что ImmTAAI — мощные ингибиторы эффекторных Т-клеток in vitro, причем ингибирование происходило только тогда, когда ImmTAAI связаны с клетками-мишенями, но не когда находятся в растворе. Теперь они исследовали взаимодействие терапевтической молекулы с тканями поджелудочной железы человека.
Поскольку наноантитело-агонист PD-1 и домен ImmTAAI, нацеленный на T-клеточный рецептор, специфичны для человека, на мышах эти исследования провести невозможно. Для исследования взяли тонкие (около 120 мкм) срезы живой ткани донорских органов трансплантационного качества, помещенные в агарозу и поддерживаемые в функциональном состоянии. Каждый срез содержал островковые участки, способные к распознаванию глюкозы и секреции инсулина.
Исследователи получили меченные флуоресцентным красителем молекулы ImmTAAI. Молекулы с флуоресцентной меткой так же успешно связывались с бета-клетками в культуре и ингибировали активные Т-клетки линии Jurkat NFL Mel5, как и молекулы без метки. При этом с клетками, не презентирующими PPI15–24, они не связывались.
Инкубация срезов с молекулами ImmTAAI и последующее микроскопическое исследование показали, что и в ткани поджелудочной железы ImmTAAI специфически связывается с поверхностью бета-клеток. Связывание также оказалось HLA-специфичным (молекулы были нацелены на PPI15–24, представленный в контексте HLA-A2). Подтвердилось и ингибирующее действие на Т-клетки. Интересно, что у одного из доноров недавно был диагностирован диабет 1 типа, и в этих срезах инкубация с ImmTAAI увеличила подвижность инфильтрированных в островки Т-клеток.
Механизм ингибирования авторы детально изучили на модифицированных Т-клетках, которые назвали «аватарами (первичные человеческие Т-клетки, в которых с помощью лентивирусной доставки генов экспрессировали специфичные к определенными антигену Т-клеточные рецепторы). Они показали напрямую, что ImmTAAI снижает специфический лизис бета-клеток и частично восстанавливает секрецию инсулина в образцах, моделирующих диабет.
Авторы подчеркивают, что подобные биспецифические препараты хорошо себя показали в терапии рака, что свидетельствует в пользу нового препарата. Следующим шагом может быть исследование эффективности, безопасности и дозировки ImmTAAI, необходимой для сохранения эндогенной массы бета-клеток при диабете 1 типа.
Женщина с диабетом не нуждается в инсулине после трансплантации островков из ее собственных клеток
Источник
Matthew W. Becker, et al. Beta cell-targeted PD-1 agonist inhibits cell-mediated autoimmunity in pancreas tissue slices // Science Advances. 1 Apr 2026. Vol 12, Issue 14. DOI: 10.1126/sciadv.aec9029


 Меню
Меню





 Все темы
Все темы
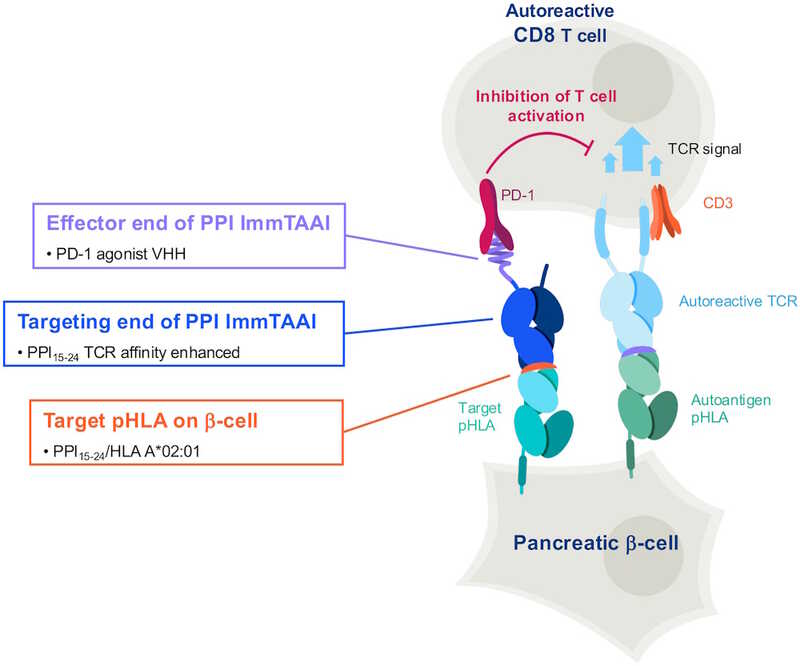 Credit: Science Advances. 2026. DOI:
Credit: Science Advances. 2026. DOI:




 0
0