Контрольная точка иммунитета играет неиммунную роль в клетках глиобластомы
Ученые из Австралии обнаружили неожиданную роль CD47 — одной из иммунных контрольных точек — в клетках глиобластомы, агрессивного рака мозга. Известно, что этот белок защищает клетки от фагоцитоза макрофагами, однако исследователи выяснили, что при глиобластоме он также регулирует пролиферацию и миграцию раковых клеток. Этот механизм не зависит от макрофагов. Его «внутренняя» функция объясняет, почему антитела к CD47 оказывались малоэффективны при лечении глиобластомы, однако понимание этого механизма, вероятно, позволит создать более точный метод терапевтического вмешательства.
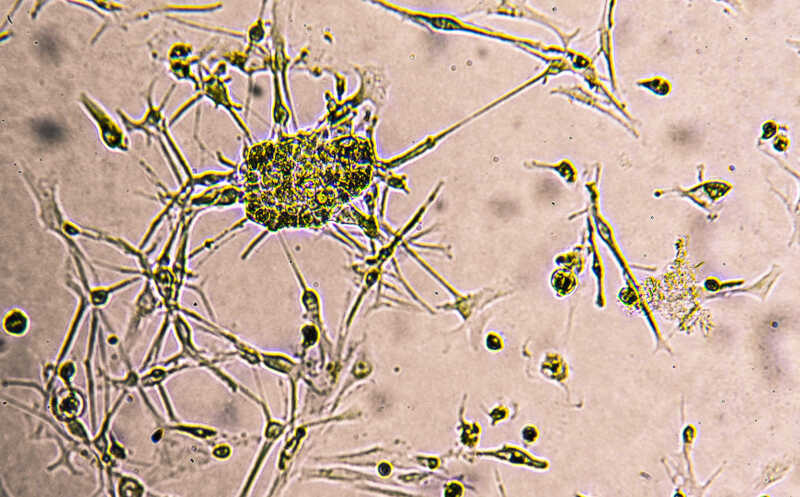
Клетки глиобластомы в культуре.
Credit:
123rf.com
Глиобластома — самая распространенная и агрессивная опухоль мозга. Выживаемость после постановки диагноза не превышает 14-15 месяцев, а радио- и химиотерапия после хирургического удаления опухоли лишь незначительно продлевают жизнь пациентов. Австралийские ученые обнаружили ключевой механизм роста и распространения глиобластомы, который может стать потенциальной мишенью для терапии. Им оказался белок CD47.
CD47 — одна из контрольных точек врожденного иммунитета, которая ограничивает фагоцитоз миелоидными клетками. Уже известно, что этот белок способствует уклонению опухоли от иммунной системы, однако препараты антител против CD47 малоэффективны при лечении глиобластомы, и причина этой низкой эффективности до сих пор неясна. Ученые показали, что в клетках глиобластомы у него есть иная роль, не связанная с подавлением иммунитета.
Проанализировав транскриптомные данные пациентов с глиобластомой, авторы работы обнаружили, что в опухоли повышена экспрессия CD47 по сравнению с нормальными тканями мозга. При этом в инвазивном фронте был низкий уровень маркера макрофагов CD68, поэтому ученые предположили, что эти клетки вряд ли являются основной мишенью CD47 — по-видимому, белок выполняет и не зависящую от макрофагов функцию.
Дальнейший анализ показал, что CD47 регулирует клеточную пластичность глиобластомы. В клетках этого типа рака, нокаутных по CD47, снижалась активность пролиферации и способность к миграции.
Результаты опытов in vitro исследователи подтвердили на мышиной модели. Мышам линии C57BL/6 внутричерепно вводили клетки высокоагрессивной линии мышиной глиобластомы, экспрессирующие люциферазу — дикого типа или с нокаутом CD47. У мышей, которым подсадили нокаутную глиобластому, опухоль росла намного медленнее, а срок выживаемости увеличился почти вдвое. Гистологический анализ подтвердил снижение опухолевой нагрузки при нокауте CD47, причем на рекрутирование миелоидных клеток или макрофагов нокаут не повлиял.
Чтобы выявить молекулярный механизм CD47-зависимой клеточной пластичности, авторы провели секвенирование РНК глиобластомы с нокаутом CD47 и без. Анализ дифференциальной экспрессии показал, что гены сигнального пути ROBO/SLIT в основном были подавлены при нокауте CD47. Уже было показано, что активация ROBO2 его лигандом SLIT2 регулирует пролиферацию, адгезию, миграцию и дифференцировку клеток. Ученые подтвердили его активацию и накопление в клетках глиобластомы дикого типа, а также установили, что CD47 предотвращает убиквитинзависимую деградацию ROBO2, связывая E3-убиквитинлигазу ITCH.
Работа демонстрирует, что белок CD47 регулирует пластичность клеток глиобластомы через сигнальный путь ROBO2 как in vitro, так и in vivo. Полученные результаты указывают на ось CD47–ROBO2 как на потенциальную мишень для терапии глиобластомы.
Ингибирование Wnt-сигналинга в глиобластоме повысило ее чувствительность к иммунотерапии
Источник
R. Polara, et al. CD47 stabilizes ROBO2 to regulate glioblastoma progression by preventing ITCH-mediated ubiquitination. // Proc. Natl. Acad. Sci. U.S.A. 123 (13) e2602460123 (2026). DOI: 10.1073/pnas.2602460123


 Меню
Меню





 Все темы
Все темы




 0
0












