Крупные внеклеточные везикулы лучше подходят для доставки груза между клетками
Есть два основных типа внеклеточных везикул (ВВ): образующиеся из эндосом (экзосомы) и образующиеся из выпячиваний плазматической мембраны (эктосомы). При выделении из сыворотки или культуральной жидкости фракция крупных ВВ обогащена эктосомами, а малых — экзосомами. Экзосомы изучены лучше, но исследователи из Японии показали, что именно крупные ВВ лучше подходят для доставки в клетки полезного груза. Например, упакованный в крупные ВВ белок Cas12f эффективнее редактировал геном клеток-реципиентов. В образовании и поглощении ВВ клетками важную роль играют белки MIM и CIP4.
Клетки секретируют внеклеточные везикулы (ВВ), чтобы облегчить перенос несекретирующих компонентов, включая белки, РНК, липиды и другие клеточные материалы, в клетки-реципиенты. Считается, что есть два основных типа ВВ: образующиеся из эндосом (экзосомы) и образующиеся из выпячиваний плазматической мембраны (эктосомы). Современные способы выделения ВВ не позволяют разделить эти типы. Тем не менее, фракция крупных ВВ обогащена эктосомами, а малых — экзосомами.
Были попытки использовать ВВ для доставки белков. Однако для этого в основном использовалась фракция малых ВВ, а эффективность доставки была довольно низкой. Исследователи из Японии использовали другую фракцию ВВ, происходящую из выпячиваний плазматической мембраны.
Внутриклеточная сигнальная ГТФаза Rac1 способствует клеточной миграции. Ее обнаруживали в ВВ из плазмы. Авторы выяснили, как содержащие Rac1 ВВ проникают в клетку и какие функции выполняют.
ВВ проникают в клетку с помощью эндоцитоза, после чего перемещаются в эндосомы. В деформации плазматической мембраны во время эндоцитоза главную роль играют белки с доменом BAR. Напротив, белки с инвертирванным доменом BAR, такие как MIM, кооперируют с малыми ГТФазами, чтобы управлять формированием выпячиваний. Образованные в результате таких выпячиваний ВВ содержат Rac1. Однако не было обнаружено свидетельств того, что Rac1 доставляется в клетки-реципиенты.
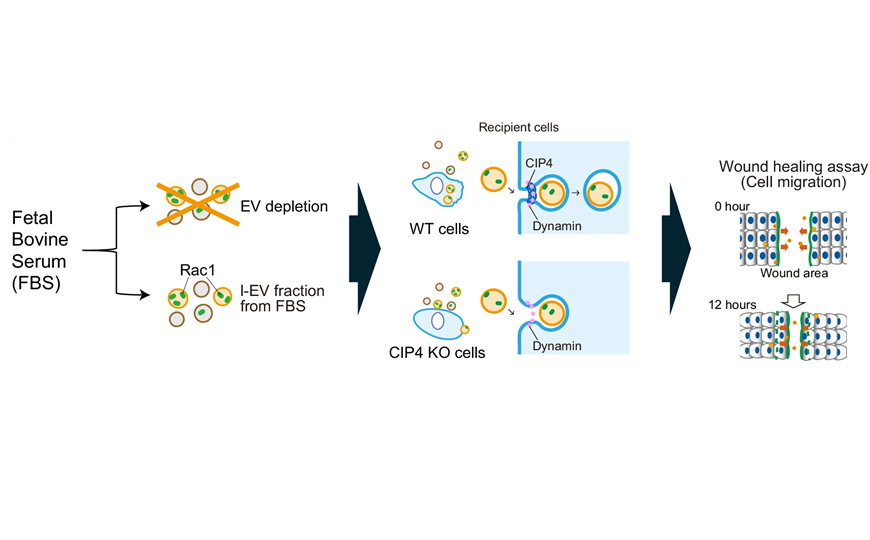
Один из F-BAR-содержащих белков — CIP4 — играет важную роль в эндоцитозе. При его нокауте клетки PANC-1 хуже перемещались под влиянием ВВ из сыворотки. То же происходит, если из сыворотки удалить ВВ. Напротив, изолированные крупные ВВ активировали миграцию клеток. Интересно, что малые ВВ таким эффектом не обладали.
Далее авторы собрали крупные ВВ из клеток HEK293, экспрессирующих MIM. Клетки PANC-1 в ответ на эти сигналы перемещались активнее, то есть эти ВВ имели такой же эффект, как и ВВ сыворотки. В этих ВВ также обнаруживался белок Rac1; его не было в фракции малых ВВ. Авторы подтвердили, что Rac1 влияет на миграцию клеток.
В клетке-реципиенте крупные ВВ, содержащие Rac1, сначала попадают в ранние эндосомы и постепенно перемещаются в поздние. После этого Rac1 выходит в цитозоль и активирует клеточную миграцию. Авторы также определили количество молекул Rac1, попадающих в клетку и содержащихся в ВВ.
Тогда авторы проверили, могут ли ВВ доставлять полезный ученым груз — белки для редактирования генома Cas12f. Повысить количество Cas12f в ВВ можно, используя связывание FKBP и FRB под действием рапамицина. Тогда MIM-FKBP и Cas12f-Halo-FRB будут взаимодействовать, Cas12f попадет в ВВ, при этом образование ВВ не изменится. Такие ВВ доставляли Cas12f в репортерные клетки, где восстанавливали свечение GFP. Дальнейшие опыты подтвердили, что для доставки Cas12f нужны MIM и CIP4, как и для доставки Rac1.
Если содержащие Cas12f ВВ инкубировать при 4°C, 37°C или даже 56 °C в течение 30 минут, то активность Cas12f сохраняется. Заморозка при −80 °C также не влияла на активность белка.
Среднее количество молекул Cas12f на крупную ВВ — 1,2 без рапамицина и 4,3 с ним. Включение последовательности T2A позволило повысить это количество до 11,2. CD63 — маркер ВВ, образованных эндосомами. CD63 помогает упаковать в крупную ВВ еще больше полезного груза (до 55,3 молекул), однако малые ВВ получают мало молекул Cas12f.
Однако эффективность редактрования генома напрямую не коррелировала с количеством молекул Cas12f в ВВ. Крупные ВВ из MIM-экспрессирующих клеток помогали редактировать геном лучше, чем ВВ из CD63-экспрессирующих клеток или малые ВВ из любых клеток.
Таким образом, ВВ, образованные из выпячиваний плазматической мембраны под действием MIM, лучше подходят для доставки полезного груза, чем эндосомальные ВВ.
Внеклеточные везикулы с мРНК разгладили морщины у мышей
Источник:
Toshifumi Fujioka,, et al. Efficient cellular transformation via protein delivery through the protrusion-derived extracellular vesicles // Nature Communications (2025), 08 December 2025, DOI: 10.1038/s41467-025-66351-1


 Меню
Меню





 Все темы
Все темы




 0
0











