Макрофаги утилизируют митохондрии с помощью микроаутофагии
Митофагия (переваривание митохондрий) — один из механизмов, связанных с активацией макрофагов. Ученые из Японии показали, что макрофаги используют для утилизации своих митохондрий не «классический» механизм аутофагии (макроаутофагию), а микроаутофагию — особый механизм, требующий специализированных везикул достаточно крупного размера. Этот процесс оказался важным для переключения фенотипа макрофагов под действием провоспалительных сигналов.
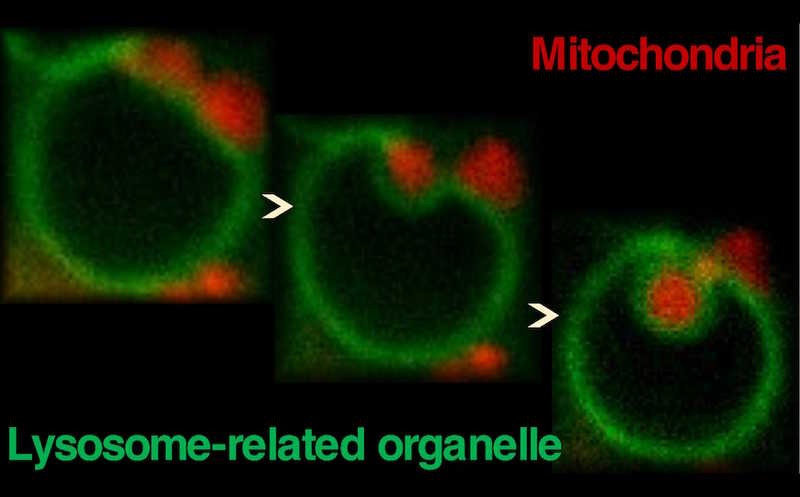
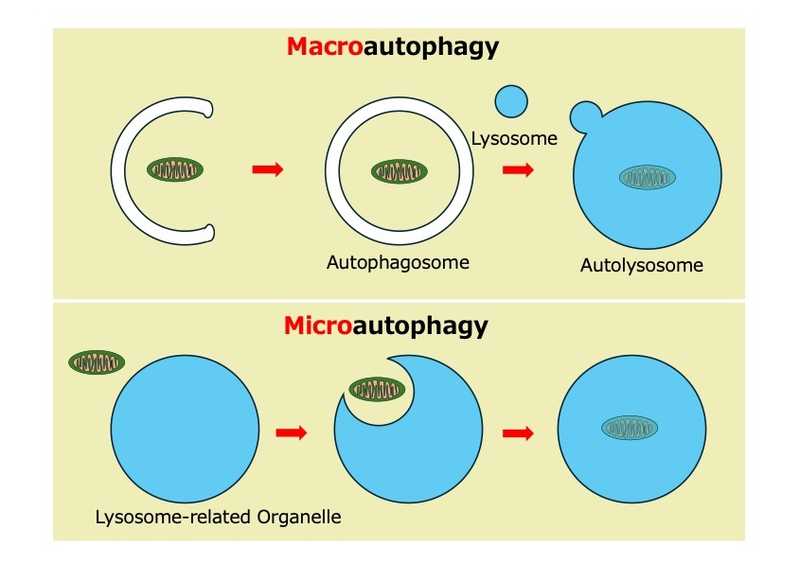
Клетки обладают различными механизмами поддержания гомеостаза, одним из которых является аутофагия. Данный механизм (в частности, аутофагия митохондрий) задействован в том числе в активации и поляризации макрофагов. Помимо «классической» макроаутофагии — она подразумевает формирование двумембранных аутофагосом, которые доставляют подлежащие разрушению компоненты к лизосомам, —внимание ученых в последнее время привлекает микроаутофагия. При ней приспособленные для деградации одномембранные органеллы «всасывают» субстраты внутрь через инвагинации мембраны. При этом долгое время оставалось неясным, как подобный механизм может быть реализован в клетках млекопитающих, поскольку их лизосомы (основные кандидаты на роль везикул для микроаутофагии) меньше большинства органелл.
 Credit:
Пресс-релиз
Credit:
Пресс-релиз
Ученые из Японии описали в мышиных макрофагах костномозгового происхождения и остеокластах специализированные лизосомоподобные органеллы (lysosome-related organelles, LRO), характеризующиеся наличием малых ГТФаз Rab32 и Rab38. Эти одномембранные органеллы имеют общие черты с лизосомами — наличие мембранного белка Lamp1 и закисление внутренней среды с помощью V-АТФазы, — однако они значительно крупнее (около 2000 нм против 100 нм у обычных лизосом). Эти характеристики позволяют рассматривать LRO в качестве органелл, участвующих в микроаутофагии.
Сначала исследователи с помощью световой и электронной микроскопии показали, что Rab32+-LRO способны захватывать внутриклеточные мембранные структуры, включая эндосомы. Характерные для эндосом белки Rab5A и Rab7 обнаруживались внутри Rab32+-LRO, а ингибирование протонной помпы бафиломицином A1 подавляло деструкцию захваченных структур и способствовало накоплению внутри LRO различных мембранных органелл, в том числе эндосом.
Помимо маркеров эндосом в Rab32+-LRO также обнаруживался митохондриальный маркер Tomm20, — это указывает на способность Rab32+-LRO захватывать митохондрии. Их поглощение усиливалось при обработке клеток токсичными для митохондрий препаратами олигомицином A и антимицином A (OA). С помощью флуоресцентного реагента Mtphagy Dye, разработанного специально для визуализации митофагии, исследователи показали, что транспорт митохондрий в Rab32+-LRO связан именно с их селективной аутофагией. В макрофагах костномозгового происхождения двойной нокаут Rab32/38 ослаблял этот сигнал как при действии OA, так и при обработке другим повреждающим митохондрии веществом — карбонилцианид м-хлорфенилгидразоном (CCCP). С помощью световой и электронной микроскопии и трехмерных реконструкций ученые визуализировали процесс поглощения митохондрий Rab32+-LRO.
Ученые также продемонстрировали, что для макрофагов микроаутофагия является преобладающим путем деструкции митохондрий. В отличие от клеток HeLa, где при повреждении митохондрий проявлялась макроаутофагия, в макрофагах преобладали структуры Lamp1+-митохондрий, но не ассоциированных с аутофагосомами LC3+ — это признаки микроаутофагии. Кроме того, нокаут генов, кодирующих ключевые для макроаутофагии белки Atg7 и Rb1cc1, не приводил к ослаблению сигнала Mtphagy Dye в макрофагах.
Ключевым компонентом Rab32-зависимой микроаутофагии является фосфатидилинозитол (3,5)-бифосфонат (PtdIns(3,5)P2). При обработке клеток апилимодом, ингибитором фосфатидилинозитол фосфат киназы PIKfyve, в мембране Rab32+-LRO переставали формироваться характерные для микроаутофагии инвагинации. Эффект сохранялся даже при конститутивной активации Rab32. При этом ученые не выявили ассоциации между Rab32+-LRO и белками комплекса ESCRT, задействованного в микроаутофагии в других клетках.
Решающим сигналом для отправки поврежденных митохондрий на деградацию выступает убиквитинирование. Подавление этого процесса при помощи TAK243 — ингибитора E1-лигазы (она участвует в присоединении убиквитиновой метки) — приводило к нарушению импорта митохондрий в Rab32+-LRO несмотря на продолжающееся формирование инвагинаций в мембранах. Также для процесса оказался важен адаптер убиквитина p62/SQSTM127, который рекрутировался к поврежденным митохондриям и «сопровождал» их в LRO. Его нокдаун снижал интенсивность митофагии. При этом не было показано влияния на митофагию в макрофагах ранее описанных для нейронов и клеток HeLa молекулярных сигналов «съешь меня» — кардиолипина и гетеродимера NIPSNAP1/2. Это свидетельствует о наличии в макрофагах особого пути инициации микроаутофагии поврежденных митохондрий.
Известно, что под действием липополисахарида (LPS) и сигналов от T-хелперов 1 типа (в частности, IFN-γ) происходит активация макрофагов по «классическому» пути и приобретение ими провоспалительного M1-фенотипа. Это сопровождается переходом от окислительного фосфорилирования к гликолизу, что требует утилизации «лишних» митохондрий с помощью митофагии. Исследователи показали, что воздействие LPS и IFN-γ приводит к убиквитинированию и фрагментации митохондрий, а затем их перемещению в LRO, причем полный процесс разрушения занимает около 24 часов. Кроме того, под действием LPS и IFN-γ отмечалось усиление выработки маркеров M1-фенотипа IL-6, IL-1β и TNF-α. В клетках с двойным нокаутом Rab32/38 выработка этих цитокинов была нарушена, а уровень митохондриального дыхания оставался неизменным, что свидетельствует о нарушении перехода к гликолизу.
Авторы исследования подчеркивают, что микроаутофагия и, в частности, микромитофагия имеет большое значение в поддержании гомеостаза в макрофагах и представляет собой энергоэкономичный путь утилизации органелл, что важно для этих клеток, подверженных динамическим изменениям. Полученные данные расширяют представления о механизмах деградации органелл и их роли в иммунном ответе.
Источник
Lu, S.L., et al. Evidence that mitochondria in macrophages are destroyed by microautophagy // Nature Communications (2025). DOI: 10.1038/s41467-025-63531-x


 Меню
Меню





 Все темы
Все темы




 0
0










