Метилирование мРНК регулирует формирование переднего мозга у мышей
Эпитранскриптомная регуляция крайне важна для формирования мозга в эмбриогенезе — авторы статьи в Science Advances показали это на мышах. Они установили, что белок VIRMA, участвующий в посттранскрипционном m6А-метилировании мРНК, играет ключевую роль в развитии переднего мозга. Нокаут VIRMA в клетках-предшественниках нейронов нарушал биогенез рибосом, тормозил пролиферацию и усиливал апоптоз, результате чего мыши рождались с недоразвитым мозгом и рано погибали.
Формирование головного мозга требует высокоточного контроля экспрессии генов. Особенно в его развитии важна активность нейральных клеток-предшественников (НПК), которая зависит от сбалансированной работы механизмов транскрипции, посттранскрипционных модификаций РНК (эпитранскриптомного профиля) и трансляции. Одной из ключевых эпитранскриптомных меток является m6А — метилирование мРНК, регулирующее её стабильность и трансляцию. Белок VIRMA, входящий в состав m6А-метилтрансферазного комплекса, ранее связывали с развитием рака, но его роль в нормальном эмбриональном развитии оставалась неясной. Коллектив ученых из Китая показал на мышах, что VIRMA необходим для биогенеза рибосом в НПК, а от него, в свою очередь, зависит формирование переднего мозга.
Исследователи проанализировали динамику экспрессии VIRMA в клетках переднего мозга мышей. Вестерн-блот показал, что уровни этого белка были значительно выше на эмбриональных стадиях развития мозга и снижалась во взрослом возрасте. Жидкостная хроматография с тандемной масс-спектрометрией показала повышенное содержание меток m6А в мРНК на эмбриональных стадиях развития мозга.
Затем ученые с помощью Cre-рекомбиназы получили мышей с условным нокаутом гена Virma в НПК переднего мозга. Такие животные весили вполовину меньше мышей дикого типа и преждевременно умирали. Иммуногистохимический анализ выявил значительные изменения структуры переднего мозга у мышей с нокаутом Virma. Нейральные прогениторные клетки таких животных хуже пролиферировали и уходили в апоптоз, что, предположительно, и привело к нарушению структуры переднего мозга.
Иммуноцитохимическое окрашивание НПК показало, что белок VIRMA колокализован с ядерными спеклами — тельцами в ядре, отвечающими за регуляцию сплайсинга и модификации РНК. При нокауте Virma снижался уровень белков, вносящих m6А-метки в РНК. Содержание m6А в мРНК также было понижено, хотя общее количество этой метки в тотальной РНК не изменилось по сравнению с клетками мышей дикого типа. Это показывает, что VIRMA поддерживает необходимый уровень m6А на мРНК в клетках-предшественниках нейронов развивающегося эмбрионального мозга. Примечательно, что транскрипты, содержащие два или более сайта m6А-метилирования, имели сравнительно короткое время полужизни, однако при нокауте Virma в НПК оно значительно удлинялось.
Проанализировав гены, в мРНК которых снижалось метилирование по m6А-сайту при нокауте Virma, авторы выяснили, что большинство таких генов относятся к пути биогенеза рибосом. Иммунопреципитация метилированных РНК и количественная ПЦР с обратной транскрипцией выявили, что в норме мРНК соответствующих генов обогащена меткой m6А, а при дефиците VIRMA уровень такого метилирования снижался. Среди мРНК с VIRMA-зависимым m6А-метилированием 43% связываются белком YTHDF2 — медиатором деградации мРНК. Это подтверждает роль VIRMA в стабилизации мРНК. При этом VIRMA не был локализован непосредственно в участках биогенеза рибосом, что свидетельствует об m6А-опосредованном механизме вмешательства на этот процесс.
При нокауте VIRMA в клетках снижался уровень рибосомальных белков, хотя уровень кодирующих их мРНК оставался в норме. Их недостаток приводит к рибосомальной дисфункции — одной из причин, по которым клетка может уйти в апоптоз, опосредованный белком p53. Однако в ответ на стрессовые состояния клетки этот белок способен накапливаться и функционировать как транскрипционный фактор. Снижение уровня VIRMA усиливало экспрессию генов-мишеней p53 и замедляло его деградацию, что указывает на активацию этого белка. Однако мРНК p53 не содержит сайтов m6А метилирования — отсутствие таких меток означает, что его экспрессия не зависит от метилирования напрямую. Прошлые исследования показали, что при рибосомальной дисфункции тормозится деградация p53, способствуя апоптозу. С помощью вестерн-блоттинга и иммунопреципитации авторы статьи подтвердили, что дефицит VIRMA усиливает взаимодействие рибосомальных белков RPL5 и RPL11 с E3-убиквитинлигазой MDM2. Такое связывание снижает активность MDM2 и препятствует деградации p53 — это объясняет усиление апоптоза НПК при нокауте VIRMA.
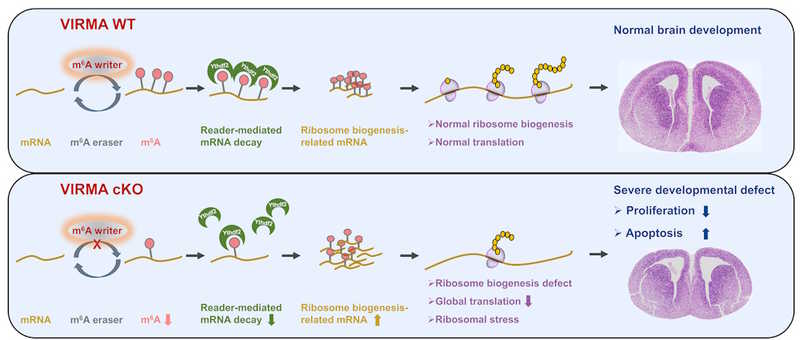 Изменения m6А метилирования при нокауте VIRMA нарушают биогенез рибосом, который способствует уходу клетки в апоптоз. Из-за этого дефицит VIRMA в НПК переднего мозга приводил к нарушению его развития.
Изменения m6А метилирования при нокауте VIRMA нарушают биогенез рибосом, который способствует уходу клетки в апоптоз. Из-за этого дефицит VIRMA в НПК переднего мозга приводил к нарушению его развития.Credit:
Science Advances (2025). DOI: 10.1126/sciadv.adq9643 | CC BY
Наконец, ученые оценили влияние VIRMA на пролиферацию опухолевых клеток. Биоинформатический анализ выявил значительную корреляцию между VIRMA и генами, участвующими в рибосомальном биогенезе. Когда ученые провели нокдаун VIRMA при помощи РНК-интерференции в клетках линии MCF7 (рак молочной железы) и HeLa (рак шейки матки), в них снизился общий уровень трансляции, нарушился синтез рибосом, замедлилась пролиферация и усилился апоптоз.
Исследование демонстрирует, что VIRMA критически важен для развития переднего мозга из-за его роли в биогенезе рибосом. Эпитранскриптомная регуляция при участии этого белка играет ключевую роль в контроле роста и деления нейрональных клеток в эмбриогенезе. Кроме того, описанный механизм справедлив и для опухолевых клеток.
Дрозофилы с врожденной бессонницей лучше обучаются, но меньше живут
Источник
Min Wu et al. VIRMA-mediated m6A modification regulates forebrain formation through modulating ribosome biogenesis // Sci. Adv. 11(26). Published online 27 June 2025. DOI: 10.1126/sciadv.adq9643


 Меню
Меню





 Все темы
Все темы




 0
0










