Описаны функции гена FAAH-OUT, мутация в котором снижает боль и тревожность
Авторы статьи в Brain исследовали механизмы работы гена длинной некодирующей РНК FAAH-OUT. Микроделеция в этом гене сформировала необычный фенотип: пациентку отличали нечувствительность к боли, повышенная способность к регенерации и сниженная тревожность. FAAH-OUT регулирует активность промотора гена FAAH, важного компонента эндоканнабиноидной системы.
Авторы новой статьи в Brain исследовали молекулярные механизмы, благодаря которым редкая мутация в гене микроРНК снижает болевую чувствительность и тревожность и ускоряет регенерацию.
Боль — естественный и необходимый стимул, уберегающий человека от опасностей и травм. Однако иногда сложные пути ноцицепции оказываются нарушены — как в случае жительницы Шотландии Джо Кэмерон (Jo Cameron). Внимание медиков и генетиков Джо привлекла десять лет назад, уже будучи в пожилом возрасте — она не чувствовала боль во время серьезной операции. Помимо этого, у женщины притуплены чувства страха и тревоги, быстро заживают раны.
Ученым удалось обнаружить в геноме Джо Кэмерон гетерозиготную микроделецию в гене длинной некодирующей РНК (lncRNA) FAAH-OUT, который экспрессируется в головном мозге и спинальных ганглиях. FAAH-OUT регулирует активность расположенного неподалеку от него гена FAAH, который кодирует фермент — гидролазу амидов жирных кислот, осуществляющую деградацию анандамида (anandamide-degrading fatty acid amide hydrolase). FAAH входит в эндоканнабиноидную систему, контролирующую болевые ощущения, эмоциональное состояние человека и т.д.
Теперь та же команда исследователей раскрыла молекулярные механизмы, за счет которых ген FAAH-OUT регулирует экспрессию FAAH. С помощью CRISPR-Cas9 ученые отредактировали геном эмбриональных клеток почки человека (HEK293), чтобы получить линию клеток с такой же микроделецией, как у Джо Кэмерон. В стабильной клеточной линии наличие делеции подтвердили с помощью ПЦР, а затем количественная ПЦР с обратной транскрипцией указала на значительное снижение экспрессии обоих генов — FAAH-OUT и FAAH.
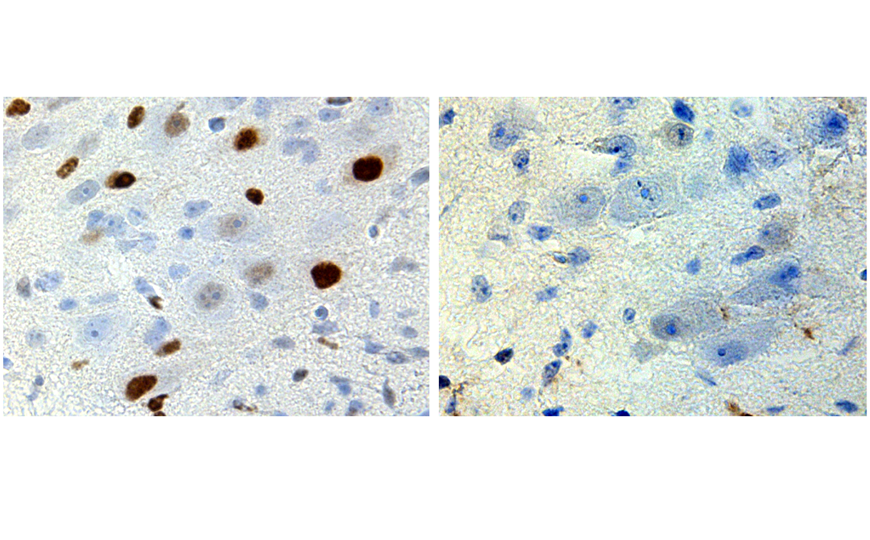
Используя высокочувствительную гибридизацию in situ и конфокальтую микроскопию, авторы установили, что в образцах человеческой ткани транскрипт FAAH-OUT находится преимущественно в ядре, тогда как транскрипт FAAH — в цитоплазме. Воздействие на транскрипцию FAAH-OUT влияло и на FAAH. Авторы выявили консервативный участок в интроне FAAH-OUT (FAAH-AMP), по-видимому, имеющий важное регуляторное значение. Данные по модификации гистонов и иммунопреципитации хроматина (ChIP-qPCR) подтвердили, что этот участок может функционировать как энхансер, и действительно, его делеция снижала экспрессию FAAH.
Анализ метилирования ДНК и иммунопреципитация хроматина (ChIP-qPCR) показали, что нарушение транскрипции lncRNA FAAH-OUT приводит к зависимому от ДНК-метилтрансфераз семейства DNMT1 метилированию промоторной области FAAH.
Кроме того, авторы выполнили транскриптомный анализ фибробластов Джо Кэмерон и четырех здоровых не родственных ей женщин, чтобы описать сеть генов, регуляция которых нарушается при изменениях взаимодействия FAAH-OUT с FAAH. Это позволило установить молекулярные механизмы в основе уникального фенотипа «человека без боли». Выделены, в частности, группы генных продуктов, которые принимают участие в WNT-индуцированной передаче сигналов, а также в сигнальных путях заживления ран, связанных с мозговым нейротрофическим фактором BDNF. Еще один ген, экспрессия которого значительно снижена в клеточной линии, полученной от Джо, кодирует атипичный хемокиновый рецептор ACKR3. Он действует как scavenger receptor опиоидов, то есть связывает опиоидные пептиды, «отнимая» их у классических опиоидных рецепторов, тем самым эффективность опиоидов в его присутствии уменьшается.
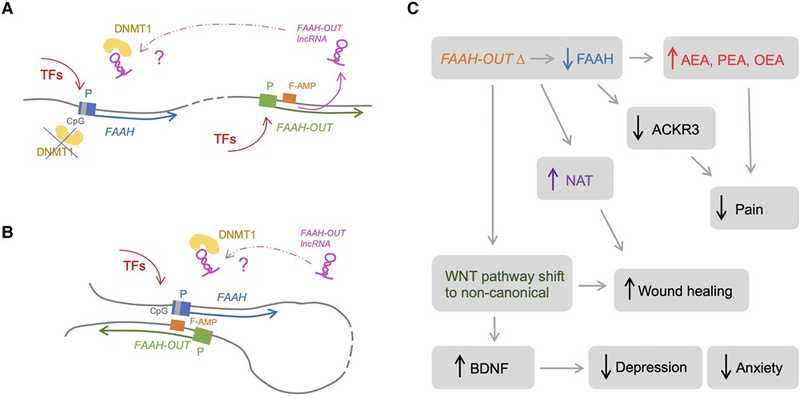 Схема регуляторных взаимодействий между FAAH-OUT и FAAH, а также изменения активности генов, ассоциированных с фенотипом Джо Кэмерон. Credit: Brain 2023. DOI:
10.1093/brain/awad098 | CC BY
Схема регуляторных взаимодействий между FAAH-OUT и FAAH, а также изменения активности генов, ассоциированных с фенотипом Джо Кэмерон. Credit: Brain 2023. DOI:
10.1093/brain/awad098 | CC BY
Таким образом, FAAH — перспективая мишень терапии хронической боли, тревожности, депрессии и других заболеваний. Понимание регуляторной роли гена FAAH-OUT может обеспечить платформу для новых методов генной терапии и терапии на основе малых молекул.
Болевой порог у рыжих повышен из-за активности опиоидных рецепторов
Источник
Hajar M., et al. Molecular basis of FAAH-OUT-associated human pain insensitivity // Brain. Published online 24 May 2023. DOI: 10.1093/brain/awad098


 Меню
Меню





 Все темы
Все темы




 0
0