Полногеномное нанопоровое секвенирование адаптировано для клинической диагностики
Новый метод быстрого полногеномного секвенирования (rWGS) для диагностики генетических заболеваний сочетает в себе оптимизированный протокол секвенирования Oxford Nanopore, облачную биоинформатику и индивидуальный подход к отбору вариантов. Кратчайшее время тестирования, на данный момент рекордное — 7 ч 18 мин. Но метод не лишен недостатков, которые могут осложнить его применение в клинической практике.

Быстрая диагностика генетических заболеваний может ускорить назначение лечения, улучшить прогноз пациентов, находящихся в критическом состоянии, и снизить расходы. Большинство решений по оказанию неотложной помощи должны приниматься в течение нескольких часов, при этом для традиционного тестирования требуются недели, а для экспресс-тестирования — дни. Монополия на быстрое клиническое полногеномное секвенирование (rapid whole-genome sequencing, rWGS) остается у Illumina. Однако нанопоровое секвенирование уже способно конкурировать с ней и на этом поле. Исследователи из Стэнфорда вместе с коллабораторами из других научных центров продемонстрировали, что с помощью секвенирования генома на платформе Oxford Nanopore можно точно и быстро диагностировать тяжелые генетические заболевания.
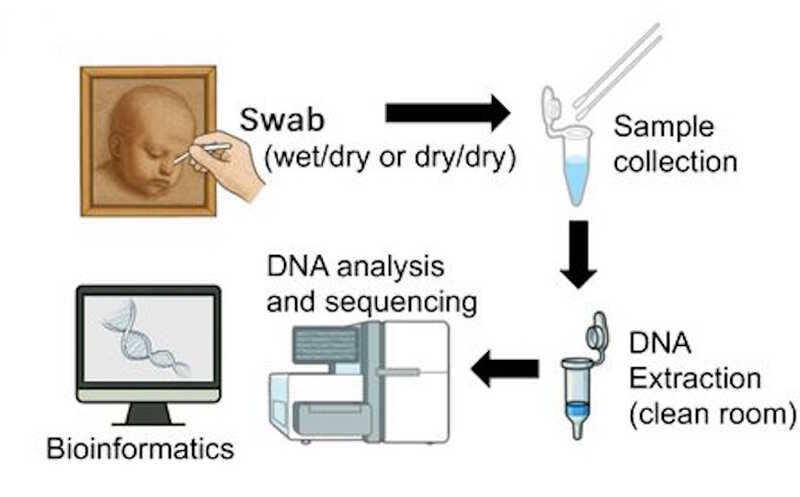
Ученые тестировали метод в двух больницах Стэнфорда. С декабря 2020 года по май 2021-го на участие в исследовании зарегистрировали 12 пациентов. Выборка была репрезентативной в отношении рас, этнических групп и пола. Чтобы максимально сократить время анализа, ученые оптимизировали протоколы пробоподготовки и секвенирования, а также использовали облачное вычисление.
Исследователи отказались от лигирования ДНК с баркодами для создания геномной библиотеки, что ускорило пробоподготовку на 37 мин, уменьшив ее продолжительность до 2,5 ч. Это также позволило загружать в каждую проточную ячейку в два раза больше ДНК. Выигрыш во времени давало и одновременное секвенирование в 48 проточных ячейках. Также ячейки промывали и повторно использовали, чтобы снизить стоимость секвенирования.
Терабайты необработанных сигналов секвенатора передавались в облачное хранилище в режиме реального времени. Данные распределили между несколькими облачными компьютерами, чтобы практически мгновенно производить идентификацию нуклеотидов и выравнивание прочтений с референсным геномом человека GRCh37. Это позволило сократить время обработки данных на 93%, с 7 ч 21 мин до 34 мин. Идентичность выравнивания составила 94%, покрытие — 46-64 на аутосомах. Медиана количества найденных однонуклеотидных вариаций, небольших вставок и делеций составила около 4,5 млн. Настраиваемая пользователем фильтрация и приоритизация снижала число вариаций-кандидатов для обзора вручную до медианы 29 для коротких вариаций и 22 для структурных вариаций.
Кратчайшее время от поступления образца крови в лабораторию до постановки первичного диагноза составило 7 часов 18 минут, диагноз получили 42% пациентов. Каждый первичный диагноз немедленно рассматривали врачи-исследователи и клиницисты, чтобы определить, является ли конкретная вариация основной причиной заболевания пациента. Результаты были подтверждены лабораторией, сертифицированной в соответствии с Clinical Laboratory Improvement Amendments (CLIA), и учитывались при корректировке лечения пяти пациентов.
Младшим из пациентов был трехмесячный доношенный младенец с эпилепсией. У него идентифицировали патогенный гетерозиготный вариант гена CSNK2B и поставили окончательный диагноз: синдром Пуарье-Бьенвеню. Это позволило не продолжать тестирование и начать лечение противосудорожными препаратами. Результат был получен за 8 часов 25 минут, что сильно контрастирует с типичными «диагностическими одиссеями» при редких генетических заболеваниях.
Стивен Кингсмор, директор и CEO Института геномной медицины Ради Чилдрен в Сан-Диего, один из инициаторов использования rWGS для диагностики заболеваний, поздравил авторов работы с достижением, однако дал критическую оценку перспективам применения метода в клинике. По его словам, распространение секвенирования для диагностики «больше зависит от масштабируемости и стоимости, чем от скорости». Заявленная в статье стоимость $4971-7318 на пациента пока что в несколько раз превышает стоимость rWGS, выполняемого командой Кингсмора на платформе Illumina NovaSeq (около $1500). При этом результат секвенирования в Ради Чилдрен можно получить за 18 ч, что Кингсмор считает приемлемой скоростью для постановки диагноза пациентам в критическом состоянии. Он также отметил, что в статье не указан уровень ошибок, который остается проблемой нанопорового секвенирования.
Руководитель работы Юэн Эшли, профессор медицины, генетики и биомедицинской науки о данных в Стэнфорде, отказался говорить об уровне ошибок, однако сообщил, что в следующем месяце ожидается публикация более подробной технической статьи, где будут все необходимые данные.
Источник
Gorzynski, J. E. et al. Ultrarapid Nanopore Genome Sequencing in a Critical Care Setting. // New England Journal of Medicine, January 2022. DOI: 10.1056/NEJMc2112090


 Меню
Меню





 Все темы
Все темы



 0
0