Секвенирование длинных фрагментов ДНК из почвы обнаружило новые таксоны бактерий и биоактивные молекулы
Нанопоровое секвенирование позволяет получать длинные прочтения, что облегчает сборку геномов ранее не исследованных организмов. Это могло бы помочь в изучении некультивируемых бактерий, однако ДНК, выделенная из почвы обычными методами, сильно фрагментирована. Исследователи из Рокфеллеровского университета разработали метод выделения высокомолекулярной ДНК из образцов почвы, собрали и проанализировали беспрецедентный объем генетической информации (около 2,5 терабаз из одного образца). Они также предсказали структуру нерибосомных антимикробных пептидов, которые могут синтезировать микроорганизмы, на основе кластеров биосинтетических генов, обнаруженных в их геномах.

Метагеномика (секвенирование ДНК, выделенной из целых микробных сообществ) позволяет исследовать геномы некультивируемых микроорганизмов. Этому способствует секвенирование длинных прочтений, например, нанопоровое. Длинные риды упрощают сборку полноразмерных последовательностей геномов. Однако для использования преимуществ длинных прочтений необходима высококачественная нефрагментированная ДНК. Исследователи из лаборатории генетически кодируемых малых молекул в Рокфеллеровском университете (Нью-Йорк, США) предлагают метод, позволяющий получать протяженные фрагменты метагеномной ДНК из образцов почвы для последующего нанопорового секвенирования. Таким способом авторы прочитали сотни полных кольцевых геномов из одного образца почвы и в них идентифицировали новые пути синтеза антибиотиков.
Обычно при исследовании метагеномов можно получить представление об их разнообразии, секвенируя ампликоны участков генов 16S рибосомной РНК. Также можно получить протяженные последовательности геномов путем сборки из коротких фрагментов (metagenome-assembled genome, MAG). Однако сборка может быть неполной и неточной, что затрудняет исследование генетического потенциала микроорганизмов. Например, кластеры биосинтетических генов (BGC — компактно расположенные гены ферментов, необходимых для синтеза одного метаболита) могут иметь длину в десятки или сотни тысяч пар оснований, и их сложно собирать из 150-нуклеотидных ридов.
Авторы нового исследования разработали пайплайн для выделения ДНК из почвы и подготовки образца для секвенирования, который позволяет получать риды длиной в десятки и сотни тысяч пар оснований (медианная длина N50 превышает 30 т. п. н.). Это дает возможность собирать последовательности длиной в миллионы пар нуклеотидов, иначе говоря, полные кольцевые геномы бактерий.
Щадящий метод очистки включает отделение бактерий от частиц почвы с помощью центрифугирования, а затем промывку обезжиренным молоком. Полученный продукт визуально напоминал лабораторную бактериальную культуру. После этого авторы использовали коммерческие наборы для экстракции ДНК с высокой молекулярной массой. Этот подход позволил извлечь существенно больше генетической информации из образца лесной почвы (2,5 терабаз).
Проведя 16S-профилирование, авторы обнаружили более 4500 уникальных видов, в том числе некультивируемые. В геномах четырех семейств — UBA5704, Pseudonocardiaceae, Streptomycetaceae и UBA11063 — встречалось более трех BGC на 1 Mb нуклеотидной последовательности. UBA — «некультивируемые бактерии или археи (uncultured bacteria or archaea); этот термин был введен для MAG, которые оказались первым примером бактериальной или архейной линии. UBA5704 — это семейство порядка Multivoradales типа Acidobacteriota, UBA11063 — семейство порядка Burkholderiales типа Pseudomonadota. Интересно, что среди BGC преобладали синтазы нерибосомных пептидов — соединений, среди которых есть антибиотики, цитостатики, иммуносупрессоры и другие биологически активные вещества.
Нерибосомные пептиды синтезируются мультиферментными системами, каждый модуль которых присоединяет очередную аминокислоту. Поэтому по информации о последовательности BGC, кодирующих синтазы нерибосомных пептидов, можно предсказать строение пептида. Авторы выполнили сборку этих BGC и для 20 из них предсказали разные варианты продуктов — линейных или циклических пептидов.
Для всех синтезированных пептидов провели скрининг биоактивности против грамположительных модельных микроорганизмов Bacillus subtilis и Staphylococcus aureus, а также грамотрицательной Escherichia coli. Пять наиболее перспективных затем проверили на активность против патогенов ESKAPE (Enterococcus faecium, S. aureus, Klebsiella pneumoniae, Acetobacter baumannii, Pseudomonas aeruginosa и Enterobacter cloacae), а также на токсичность для клеток человека.
Внимание исследователей привлекли два соединения. Одно из них, SynBNP 25, было мощным антибиотиком широкого спектра действия и не обладало цитотоксичностью. Его назвали «эрутацидин», от латинского erutus — «выкопанный». Второе, SynBNP 27, которое проявило мощную активность против золотистого стафилококка S. aureus (минимальная ингибирующая концентрация 2 мкг/мл), получило название тригинтамицин, так как его активность была обнаружена при 30 градусах.
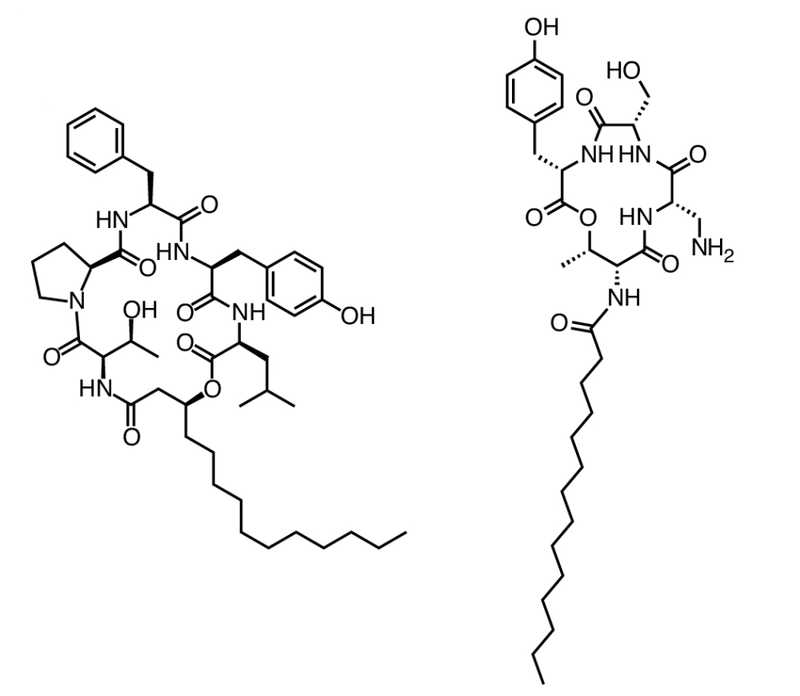 Тригинтамицин (слева), эрутацидин (справа). Credit: Nat Biotechnol (2025). DOI:
10.1038/s41587-025-02810-w |
CC BY-NC-ND 4.0
Тригинтамицин (слева), эрутацидин (справа). Credit: Nat Biotechnol (2025). DOI:
10.1038/s41587-025-02810-w |
CC BY-NC-ND 4.0
Исследование механизмов действия показало, что тригинтамицин нацелен на АТФазу ClpX, которая не является необходимой для многих бактерий, а эрутацидин взаимодействует с кардиолипином и может также взаимодействовать с другими родственными липидными структурами. Это редкий механизм действия, не представленный среди используемых в клинике антибиотиков, поэтому можно надеяться, что эрутацидин будет активен против против патогенов с множественной лекарственной устойчивостью.
Предложенный подход расширяет возможности метагеномики по изучению огромного генетического разнообразия некультивируемых бактерий и поиску биоактивных молекул, которые они могут синтезировать.
Новый внехромосомный элемент Inocle обнаружен в бактериях ротовой полости
Источник
Burian, J., et al. Bioactive molecules unearthed by terabase-scale long-read sequencing of a soil metagenome // Nature Biotechnology (2025). DOI: 10.1038/s41587-025-02810-w


 Меню
Меню





 Все темы
Все темы
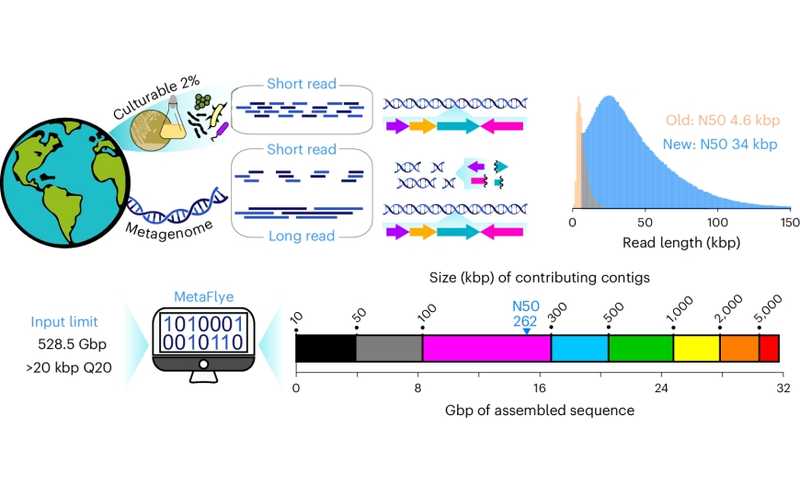 Credit: Nat Biotechnol (2025). DOI:
Credit: Nat Biotechnol (2025). DOI:



 0
0