Цифровой мост между головным и спинным мозгом восстановил способность ходить после травмы позвоночника
Новая разработка Грегуара Куртина с коллегами вернула способность ходить человеку с травмой шейного отдела позвоночника. Имплантаты считывают сигналы от нейронов коры, алгоритм генерирует стимулирующие сигналы, которые еще один имплантат передает в спинной мозг ниже участка травмы. Ходьба стала более естественной, чем в предыдущих экспериментах.
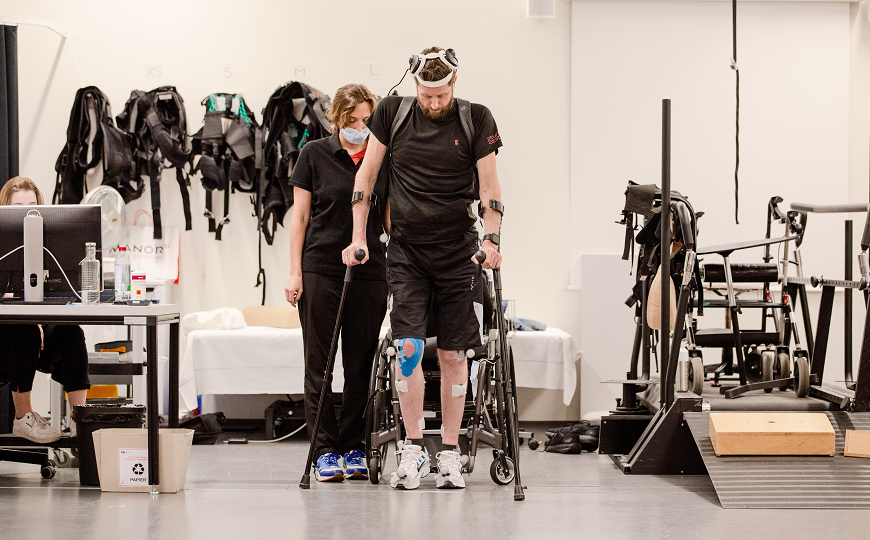
Пациент и исследователь в госпитале университета Лозанны.
Credit:
Jimmy Ravier
Повреждения спинного мозга разрывают нейронные пути, необходимые для связи с головным мозгом. Следствием может быть потеря способности двигать ногами и руками, чувствительности и других физиологических функций. По оценкам Всемирной организации здравоохранения (ВОЗ), от 250 000 до 500 000 человек ежегодно получают подобные травмы. Предлагаются различные стратегии восстановления нейронных связей, как биологические (активация роста аксонов нейронов, трансплантация клеток нейроглии, поддерживающих рост, и т.п.), так и технологические. Однако пока что ни одна стратегия не признана достаточно эффективной и безопасной.
Международная группа ученых под руководством Грегуара Куртина, Джослин Блох (Университет Лозанны, Швейцария) и Гийома Шарве (Университет Гренобль-Альпы, Франция) опубликовала в Nature отчет об испытании на человеке цифрового моста, или BSI (интерфейса между головным и спинным мозгом). Подобную конструкцию они исследовали на обезьянах еще в прошлом десятилетии. Имплантированный чип в головном мозге получал сигналы от нейронов моторной коры, контролирующих движения задних лап, и с помощью беспроводного интерфейса передавал декодированные сигналы на другой имплантат, расположенный ниже повреждения спинного мозга (эпидуральная электростимуляция). В результате животные снова смогли ходить.
В новой работе представлены результаты эксперимента, в котором участвовал человек с травмой спинного мозга. Два беспроводных регистратора, каждый из которых содержит 64 электрода, в ходе операции были размещены на твердой мозговой оболочке (одна из трех оболочек, покрывающих мозг, самая внешняя), над областями, которые участвуют в контроле движений ног. (Такой метод отведения потенциалов, при котором электроды располагаются на мозге, называется электрокортикографией, или ЭКоГ; потенциалы имеют большую амплитуду и разрешение, чем при ЭЭГ.) Участки, сильнее всего реагирующие на намерение пошевелить ногами, выбрали с помощью компьютерной томографии и магнитоэнцефалографии. В имплантате также есть две антенны: одна питает его за счет индуктивной связи, а другая, сверхвысокочастотная, транслирует сигналы ЭкоГ в режиме реального времени на портативную базовую станцию (ее пока приходится носить в рюкзаке).
Третью многоэлектродную решетку имплантировали в твердую оболочку спинного мозга, чтобы сигналы поступали на входные зоны задних корешков. Эти структуры проецируются на сегменты спинного мозга, которые содержат двигательные нейроны, контролирующие мышцы ног. Алгоритм базовой станции декодирует сигналы ЭКоГ и преобразует их в стимулирующие сигналы; они передаются генератору импульсов, он, в свою очередь, стимулирует нейроны спинного мозга, а от них сигналы поступают к мышцам.
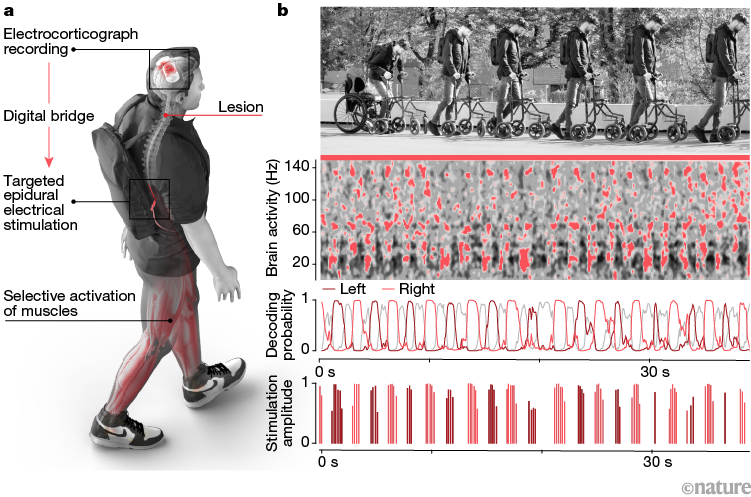 Схема расположения имплантатов и блока обработки в рюкзаке, преобразующего сигналы головного мозга в сигналы для активации мышц; справа хронофотографии участника и параллельные его движениям операции цифрового моста: спектрограмма активности мозга, вероятность движений левой и правой ноги, вычисленная по этим сигналам, и результирующая модуляция амплитуды стимуляции. Credit: Nature. 2023. DOI:
10.1038/s41586-023-06094-5 | CC BY 4.0
Схема расположения имплантатов и блока обработки в рюкзаке, преобразующего сигналы головного мозга в сигналы для активации мышц; справа хронофотографии участника и параллельные его движениям операции цифрового моста: спектрограмма активности мозга, вероятность движений левой и правой ноги, вычисленная по этим сигналам, и результирующая модуляция амплитуды стимуляции. Credit: Nature. 2023. DOI:
10.1038/s41586-023-06094-5 | CC BY 4.0
Цифровой мост имплантировали пока только одному пациенту, который за десять лет до начала клинических испытаний попал в аварию на мотоцикле. Частичный разрыв спинного мозга привел к тетраплегии — потере функции конечностей. Ходить самостоятельно Герт-Ян Оскам не мог, но «верил, что это возможно», как он сказал на пресс-брифинге. Ранее он участвовал в клиническом испытании STIMO, которое включало пятимесячную программу нейрореабилитации с электростимуляцией спинного мозга. Удалось восстановить способность передвигаться с ходунками, но дальнейших улучшений не было.
Установка имплантатов заняла немного времени, после каждой операции пациента выписывали в течение суток, и в последующие 20 месяцев наблюдений требовалась лишь нечастая повторная калибровка. Уже после пятиминутной первичной калибровки BSI поддерживал непрерывный контроль активности мышц-сгибателей бедра (нарушения затронули их в наибольшей степени). Мышечная активность увеличилась в пять раз по сравнению с попытками без BSI. Восстановился интуитивный контроль движений ног: Герт-Ян смог стоять, ходить, подниматься по лестнице и даже пересекать пешком сложные ландшафты.
После программы нейрореабилитации определенные улучшения наблюдались и при выключенном BSI (видео). Улучшились не только двигательные показатели, но и чувствительность к легким прикосновениям. «Эти улучшения без стимуляции трансформировались в значительное повышение качества жизни, например, возможность самостоятельно ходить дома, садиться в машину и выходить из нее или пить напитки с друзьями, стоящими в баре», — отмечают авторы статьи. Можно надеяться, что цифровой мост создает основу для восстановления естественного контроля движений.
В предыдущих исследованиях авторы уже использовали электрическую стимуляцию спинного мозга для восстановления двигательной активности у людей. (И установили в параллельных экспериментах на животных, что движение восстанавливается благодаря интернейронам спинного мозга; подробнее на PCR.NEWS). Отличие нового исследования от предыдущих заключается в том, что здесь авторы декодируют движения по активности мозга, а не по остаточным движениям, которые регистрируют датчики, прикрепленным к телу. Участники предыдущих испытаний сообщали, что им трудно адаптировать движения ног к разным ландшафтам, ходьба не воспринимается как полностью естественная. Цифровой мост, по-видимому, преодолевает эти ограничения.
В дальнейшем авторы планируют подтвердить эти результаты на других пациентах, в том числе с полным разрывом спинного мозга, а также сделать носимые компоненты более компактными. Кроме того, они думают над тем, чтобы аналогичным образом восстановить движения рук после инсульта или при болезни Паркинсона; подобные работы они делали ранее.
Источник
Lorach, A. A., et al. Walking naturally after spinal cord injury using a brain-spine interface // Nature. 2023. DOI: 10.1038/s41586-023-06094-5


 Меню
Меню





 Все темы
Все темы




 0
0











