Вакцина против ВИЧ на основе вирусного вектора прошла первую фазу клинических испытаний
Команда американских ученых протестировала на людях геннотерапевтический препарат против вируса иммунодефицита человека. Суть метода в доставке гена антиВИЧ-антитела широкого спектра с помощью аденоассоциированного вирусного вектора. В первой фазе КИ оценили иммунный ответ на компоненты лекарства и проанализировали последствия от разных доз вектора.
123rf.com
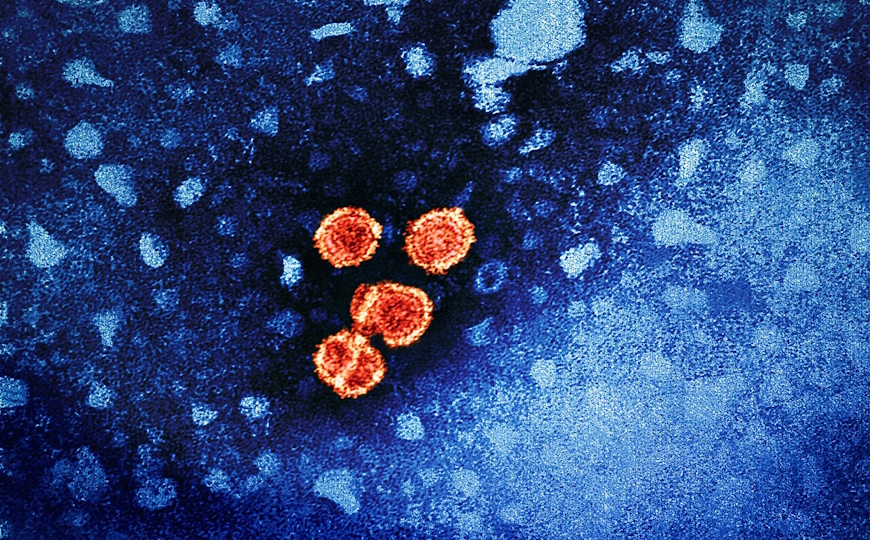
Вирус иммунодефицита человека (ВИЧ) защищает себя от иммунного ответа многими способами. Их общая цель — поменять гликопротеины на поверхности вируса. Обойти эти способы позволяют антитела широкого спектра (bnAb). Они нацелены на консервативные участки капсида вируса и поэтому могут работать против нескольких типов ВИЧ одновременно. Заставить организм вырабатывать такие антитела прямой иммунизацией компонентами вируса сложно по ряду причин.
Ученые из США провели первую фазу клинических испытаний геннотерапевтической вакцины против ВИЧ. На этой фазе оценивают последствия от введения различных доз препарата. Исследователи использовали аденоассоциированный вирус AAV 8 для доставки в клетки гена bnAb VRC07, которое ранее уже исследовалось в качестве активной составляющей вакцины против ВИЧ. Интересно, что генетическая конструкция кодирует легкую и тяжелую цепи в одной рамке считывания. Между генами цепей расположена специальная вставка 2A, благодаря которой во время трансляции происходит сдвиг рибосомы. Это приводит к отдельному синтезу тяжелой и легкой цепей антитела с одной рамки считывания.
Из 97 кандидатов для клинических испытаний в 2018–2019 гг. было отобрано восемь добровольцев: шесть мужчин и две женщины в возрасте от 30 до 60 лет. Все кандидаты были ВИЧ-инфицированы и стабильно получали антиретровирусную терапию. Вектор вводили внутримышечно и оценивали его безопасность, устойчивость, эффективность экспрессии и функциональность антител. Наблюдения продолжались несколько лет.
Участников разделили на группы по два-три человека. Каждая группа получала свою дозу препарата: 5х1010, 5х1011, 2,5х1012 копий вирусного генома на килограмм веса. После введения вектора часть пациентов жаловалась на боль в мышцах и головную боль. Тем не менее серьезных побочных эффектов не наблюдалось — ученые не обнаружили развития гепатита или активации CD4+ Т-лимфоцитов, специфичных к вектору. В то же время после самой низкой дозы у двух участников эксперимента увеличивалась продукция интерферона гамма в CD8+ клетках. Ученые подтвердили, что это был специфичный иммунный ответ на капсид AAV8.
Сывороточный белок VRC07 был обнаружен у всех участников. В случае отсутствия иммунного ответа на само антитело VRC07 его концентрация выходила на плато к 14 неделе после инъекции и в основном варьировалась между 0,1 и 1 мкг/мкл. В одном из случаев экспрессия белка превысила 3 мкг/мкл. У четырех участников концентрация оставалась стабильно высокой продолжительное время (годы).
Ученые проанализировали влияние иммунной системы на работу VRC07. Эксперимент был устроен следующим образом. Исследователи проверяли образцы на наличие VRC07-связывающих белков и определяли их аффинность к антителу. В конце ученые in vitro оценивали, насколько эти белки будут мешать правильной работе антитела. Последний тест не показал какого-либо влияния иммунной системы. Это значит, что анти-VRC07 антитела связываются с его Fab-фрагментом и не взаимодействуют с идиотипной частью. Такие антитела были обнаружены у трех из восьми участников, у двух из них, по-видимому, это привело к снижению концентрации целевого белка.
Нейтрализирующая способность (IC50) VRC07 in vivo снижалась меньше чем в два раза по сравнению с экспериментами in vitro. Тем не менее in vivo значение IC50 лежало в пределах двух стандартных отклонений от среднего in vitro C50.
Ученые предполагают, что их препарат уменьшит резервуар вируса в организме. В то же время они подчеркивают, что результаты эксперимента не дают повода быть уверенными в этом. Также это исследование открывает новые цели для разработки будущих препаратов: увеличение продукции антител и уменьшение IC50.
Таким образом, исследователи показали возможность использовать аденоассоциированный вектора для продукции bnAb и показали, что эффект трансфекции сохраняется со временем.
Источник
Casazza, J.P., et al. Safety and tolerability of AAV8 delivery of a broadly neutralizing antibody in adults living with HIV: a phase 1, dose-escalation trial. // Nature Medicine (2022). DOI: 10.1038/s41591-022-01762-x


 Меню
Меню





 Все темы
Все темы




 0
0