Визуализирующая масс-цитометрия для молекулярного типирования рака
Ученые использовали масс-цитометрию для выделения фенотипических кластеров единичных опухолевых клеток. Такой подход к типированию опухолей повышает точность прогноза и может служить базой для разработки терапевтических стратегий.
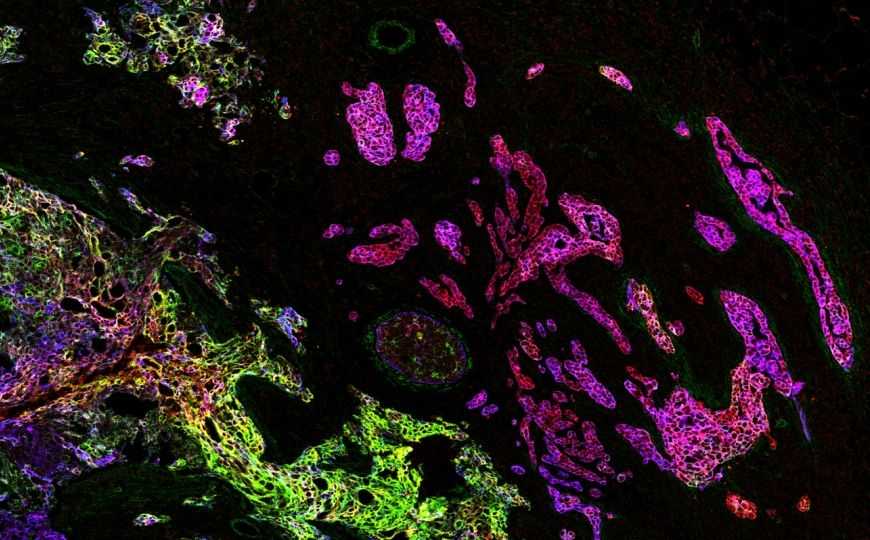
Credit:
Bernd Bodenmiller, Цюрихский университет | Пресс-релиз
В основе диагностики рака и подбора лечения лежат гистологические и фенотипические различия опухолей. Однако даже при одинаковых типах опухоли прогноз сильно варьирует из-за сложной архитектуры опухолевой ткани. Гетерогенность опухоли может стать препятствием для верной оценки тяжести заболевания. Молекулярное типирование имеет диагностическую ценность, однако к нему обращаются не всегда. Кроме того, подтип рака молочной железы определяется только в тех случаях, если более 1% опухолевых клеток содержат рецепторы гормонов или более 10% клеток демонстрируют высокий уровень экспрессии белка HER2. В результате большая часть клеток остается неохарактеризованной.
В новой работе ученые из Цюрихского университета с коллабораторами продемонстрировали значимость молекулярного типирования опухолей молочной железы на основе данных о единичных клетках, используя визуализирующую масс-цитометрию (Imaging Mass Cytometry, IMC). Анализ проводился с помощью платформы Hyperion Imaging System от компании Fluidigm, сочетающей иммуногистохимическое окрашивание с масс-спектрометрической детекцией сигнала. В качестве меток используются изотопы тяжелых металлов, индивидуальные для каждого антитела. Сигнал обрабатывается специальной компьютерной программой, после чего формируется изображение с разрешением на уровне единичных клеток.
Авторы создали панель из 35 белковых биомаркеров, в число которых вошли мишени с известной клинической значимостью (рецепторы эстрогена, прогестерона и HER2), а также фактор пролиферации Ki-67, маркеры эпителиальной, мезенхимальной, иммунной и эндотелиальной клеточных линий, онкогены и белки — участники некоторых сигнальных путей. После обработки образцов опухолей молочной железы от 352 пациентов, для 281 из которых были доступны данные о клиническом исходе, было получено 720 изображений. По изображениям ученые подсчитали экспрессию маркеров в единичных клетках и разбили клетки на фенотипические кластеры. Всего было определено 14 метакластеров, включающих известные клеточные подтипы. Кроме этого, авторы выделили 18 новых подгрупп единичных клеток, ассоциированных с патологией (single-cell pathology subgroup, SCP). Эти подгруппы отличались от классических клинических подтипов и характеризовались различными клиническими исходами. Например, SCP1 соответствовала хорошему прогнозу для пациента, а прогноз для пациента с SCP3 был хуже. Как сообщается в статье, определение фенотипических групп единичных клеток повышает точность предсказания выживаемости по сравнению с традиционными клиническими подходами.
Ученые дополнительно проанализировали образцы от 73 пациентов и выявили те же метакластеры и SCP, но в других соотношениях. Это может быть обусловлено разными принципами формирования когорт испытуемых для двух экспериментов.
В результате исследования была получена детальная пространственная карта фенотипов единичных клеток и взаимного расположения клеточных сообществ в опухолевых тканях. Президент и исполнительный директор Fluidigm Крис Линтвейт считает, что данная работа простимулирует использование IMC в клинических испытаниях, повысит точность прогнозов и качество персонализированной медицины.Источники
Imaging Mass Cytometry Uncovers Novel Breast Cancer Subgroups Associated With Outcomes


 Меню
Меню





 Все темы
Все темы




 0
0