Вырабатываемый при инфекции простагландин вызывает не только лихорадку, но и озноб
При развитии инфекции у млекопитающих поднимается температура тела, за что отвечают два механизма. В клетках сосудов головного мозга вырабатывается медиатор простагландин Е2 (PGE2), который действует на экспрессирующие его рецептор EP3R нейроны преоптической области, гипоталамического центра терморегуляции, вызывая лихорадку. Исследователи из Японии показали, что PGE2 действует таже на экспрессирующие EP3R нейроны латерального парабрахиального ядра, которые передают сенсорные сигналы в центральное миндалевидное ядро, регулирующее эмоции, в том числе дискомфорт и страх. При инфекции передача холодовых сенсорных сигналов даже в термонейтральных условиях усиливается. Из-за этого повышается чувствительность к холоду, что проявляется в виде озноба и вызывает у животных стремление к теплу (в исследовании крысы выбирали нагретую до 39°C пластинку, а не пластинку 28°C).

У млекопитающих выделяют произвольную поведенческую терморегуляцию и непроизвольную вегетативную терморегуляцию. Чтобы помочь организму бороться с инфекцией и поднять внутреннюю температуру тела (Tcore), задействуются оба механизма. Часто больные люди испытывают озноб, который способствует терморегуляторному поведению — они увеличивают количество слоев одежды, включают обогреватель и так далее. Однако механизм роста чувствительности к холоду при инфекции неясен.
Простагландин Е2 (PGE2) является основным медиатором лихорадки. При введении липополисахарида животным было показано, что в эндотелиальных клетках кровеносных сосудов мозга индуцируется экспрессия ферментов биосинтеза PGE2. Образовавшийся PGE2 высвобождается в паренхиму головного мозга, где воздействует на рецепторы простагландина EP3 (EP3R) нейронов преоптической области (POA), гипоталамического центра терморегуляции. Воздействие PGE2 запускает непроизвольные реакции, такие как термогенез бурой жировой ткани (BAT), дрожь и сужение сосудов кожи. Также под действием липополисахарида крысы ищут тепла, но ранние работы показали, что POA при этом может и не быть задействована. Исследователи из Японии выяснили, какие области мозга вовлечены в поведенческую терморегуляцию и реакцию озноба.
Латеральное парабрахиальное ядро (LPB) моста является ключевым интегративным центром, опосредующим восходящий термосенсорный сигналинг от кожных терморецепторов как для автономной, так и для поведенческой терморегуляции. Недавно эта же группа исследователей показала, что два отдельных термосенсорных нейронных пути от LPB к POA и к центральному миндалевидному ядру (CeA) управляют соответственно избеганием тепла и избеганием холода. Рецепторы EP3R (Ptger3) и EP4R (Ptger4) экспрессируются в LPB, а введение липополисахарида активировало более половины Ptger3-экспрессирующих нейронов, но почти не активировало Ptger4-экспрессирующие нейроны. Авторы работы предположили, что PGE2, вырабатываемый во время инфекции, может провоцировать поиск тепла, изменяя термосенсорную передачу посредством воздействия на EP3R в LPB.
Сначала исследователи вводили PGE2 или солевой раствор в LPB крысам дикого типа, а затем позволяли им выбирать между двумя пластинами — нагретой до 28°C (термонейтральная для крыс) и до 39°C (теплая). Крысы, которым ввели солевой раствор, предпочитали термонейтральную пластину, но животные, которым ввели PGE2, больше времени проводили на теплой пластине. Их внутренняя температура постепенно повышалась, при этом инъекции не влияли на общий уровень активности крыс или на TBAT.
С помощью агонистов рецепторов PGE авторы подтвердили, что поиск тепла происходит под действием активации EP3R в LPB. Нейроны LPBEP3R опосредуют передачу сигналов к нескольким участкам переднего мозга, но не к терморегуляторному центру POA. Проекций нейронов LPBEP3R в POA было очень мало.
Нейроны LPB с проекциями в CeA (LPB→CeA) передают сигналы о холоде, необходимые для его избегания. Оказалось, что нейроны LPBEP3R — часть популяции нейронов LPB→CeA. Дополнительные опыты подтвердили, что воздействие PGE2 в LPB не индуцирует термогенез в BAT или ответ со стороны сердечно-сосудистой системы.
Таким образом, сигналы от холодовых рецепторов кожи активируют группу нейронов LPB, экспрессирующих EP3R (нейроны LPBEP3R), которые передают сенсорные сигналы в центральное миндалевидное ядро (CeA). При наличии инфекции PGE2, продуцируемый в сосудах головного мозга, воздействует на EP3R нейронов LPB и тем самым усиливает передачу холодовых сенсорных сигналов в CeA даже в термонейтральных условиях. Из-за этого повышается чувствительность к холоду, что проявляется в виде озноба и вызывает стремление к теплу.
Другая группа нейронов LPB, не экспрессирующая EP3R, также получает сенсорный сигнал о холоде и передает его в преоптическую область (POA), вызывая автономные реакции защиты от холода. Эти реакции опосредуются экспрессирующими EP3R нейронами POA. Во время инфекции PGE2 вызывает автономные реакции (лихорадку), воздействуя на EP3R на нейронах POA.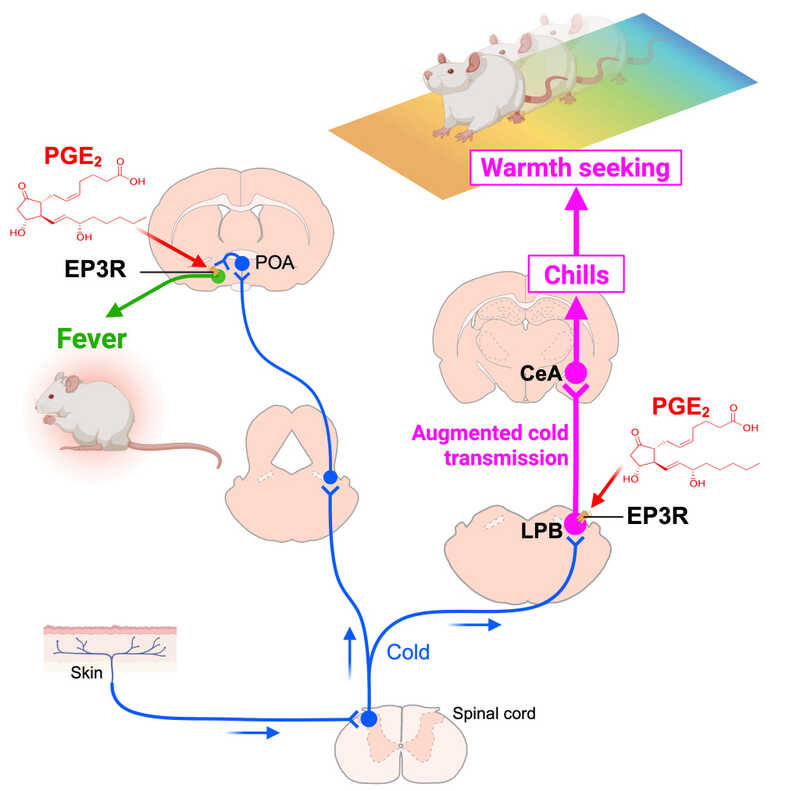 Kazuhiro Nakamura |
Пресс-релиз
Kazuhiro Nakamura |
Пресс-релиз
Воспоминания о холоде вызывают физиологическую реакцию согревания
Источник:
Takaki Yahiro, et al. The pyrogenic mediator prostaglandin E2 elicits warmth seeking via EP3 receptor-expressing parabrachial neurons: a potential mechanism of chills // The Journal of Physiology (2026), published 10 February 2026, DOI: 10.1113/JP289466


 Меню
Меню





 Все темы
Все темы




 0
0











