О геноме человека, бессмертной медузе и волосах царевича Алексея
Широкому кругу читателей Евгений Рогаев известен как ученый, который поставил точку в вопросе об аутентичности останков царской семьи. Он стоял у истоков внедрения анализа ДНК в судебно-медицинскую экспертизу в нашей стране, участвовал в открытии генов, ключевых для болезни Альцгеймера, одним из первых в России начал работать с древней ДНК и секвенировал митохондриальный геном мамонта. А поводом для этого интервью послужило получение самой полной версии генома человека.

Евгений Рогаев — доктор биологических наук, член-корреспондент РАН, заведующий лабораторией эволюционной геномики Института общей генетики РАН, профессор Медицинской школы Университета Массачусетса, директор Научного центра генетики и наук о жизни университета «Сириус».
Самый полный геном человека
Недавно вышла статья в Science: консорциум Telomere-to-telomere (T2T) опубликовал полную версию генома человека. В этой работе участвовали вы и ваши сотрудники. Вы входите в консорциум?
Входим. В самой работе больше всего участвовал Иван Александров, в соавторах публикации консорциума также Лев Уральский, Федор Гусев и я.
Какова ваша роль в этой работе? Что именно из генома человека вы секвенировали?
Роль сотрудников нашей группы — участие в анализе центромерных альфоидных повторов ДНК. Большая часть непрочитанного генома как раз относилась к центромерным участкам, это особые участки хромосом, которые необходимы для деления клеток, и они, как правило, состоят из тандемно повторяющихся единиц последовательности ДНК. Интересно, что моя самая первая научная работа, дипломная, была посвящена как раз клонированию и секвенированию первого фрагмента хромосомы, содержащей эти альфоидные повторы ДНК центромеров. Мы опубликовали статью еще в 1986 году. Несколько лет назад мы в какой-то степени вернулись к этой теме. Центромеры во всех хромосомах считались гомогенными, состоящими из одинаковых повторов. Но оказалось, что они не совсем гомогенны, разные хромосомы по этим доменам друг от друга отличаются. Там довольно сложная структура, и на хромосомах они занимают многие тысячи нуклеотидов. Но как именно они расположены, их последовательность очень трудно было определить. Прошло много времени, а в исходном референсном геноме в этих участках оставались «дырки». По примерной оценке версия ядерного генома человека, которая с 2001 года все время пополнялась и улучшалась, не содержала где-то около 8% геномной последовательности ДНК.
Что входит в эти 8%? Как правило, это участки генома сложной структуры — повторы, инверсии, дупликации и т.д. Когда мы с помощью современных методов секвенирования прочитываем короткие последовательности (short reading), такие участки очень трудно сориентировать.
Пару лет назад мы опубликовали работу по исследованию эпигенетических профилей нейрогенома. В ней мы хотели найти эпигенетические различия в нейронах у разных людей, в том числе больных шизофренией. Мы смотрели, какие участки генома в нейронах коры головного мозга имеют активные промоторы, по специальному хроматиновому маркеру, и таким образом просматривали весь геном. И когда мы начали строить карту этих активных промоторных генов, то обнаружили, что в дополнение к тысячам сигналов на участках известных генов многие сигналы картируются на разные геномные участки, где по референсному геному никаких генов не отмечено. Интегрируя эти данные хроматиновых «сигналов на промоторы» и данные транскриптомики (анализа РНК транскриптов клеток мозга от многих индивидов), мы показали возможность открытия новых генов, которые еще не были аннотированы. По большей части, таким способом мы выявили серию белок-некодирующих генов, но также и некоторые белок-кодирующие. Пока мы два года эту статью делали, в референсную последовательность генома постепенно добавлялись некоторые из таких генов, что подтверждало правомерность нашего подхода.
С 2001 года драфт генома несколько раз обновлялся, в последний раз — в 2019-м?
Да, но все равно оставались кусочки геномных последовательностей ДНК, которые невозможно было «воткнуть» в целую последовательность, в контиг. Теперь таких нет, все на месте. Вы спросите: а что сделали, чтобы так получилось? Прежде всего, появились методы «длинного чтения» (long reading). Оно было обеспечено двумя платформами — Pac Bio (Pacific Bioscience) может прочитать десятки тысяч нуклеотидов, а Oxford Nanopore обеспечивает ультрадлинное чтение, до миллиона нуклеотидов (правда для этого надо еще суметь так выделить ДНК, чтобы она не порвалась). Но у этих платформ был недостаток — большой процент ошибок, в Pac Bio до 13-15 %. Но можно было сделать грубый набросок длинной последовательности, а потом, используя секвенирование методом Illumina, эту последовательность сделать чистой. Но не так давно у Pac Bio появилась технология, которая с помощью многих циклов и многократного прочтения «чистит» последовательность ДНК от ошибок, что и было использовано в работе консорциума.
Геном каких именно клеток секвенировали?
Как описано в статье, была использована специальная гомозиготная клеточная линия человека. Когда мы начинаем собирать полный геном, то гетерозиготность, когда на парных хромосомах находятся разные аллели, очень мешает. Думаю, идеальным было бы взять сперматозоид, с гаплоидным набором. Но в таком случае нужно работать с одиночной клеткой. Другой вариант — взять диплоидную гомозиготу. Для этого использовали особую линию клеток, связанных с редкой патологией при беременности под названием «пузырный занос». При такой патологии в оплодотворенной яйцеклетке материнский набор хромосом элиминируется, а генетический материал сперматозоида дуплицируется. В результате клеточных делений получаются клетки с диплоидным набором хромосом только от папы, в гомозиготном состоянии.
Причем с Х-хромосомой.
С Y хромосомой такие клетки не выживают, можно получить только 46 ХХ. При использовании такой клеточной линии устраняется проблема генетической гетерогенности, становится гораздо проще собирать геномную последовательность. Так как это клеточная линии, которая ведется в лаборатории, возможны некоторые геномные изменения в процессе культивирования клеток, но они незначительные. Только Y-хромосомы в этом геноме нет.
Большая часть вновь секвенируемых участков некодирующие?
Да, большая часть — это центромерные и околоцентромерные хромосомные участки, которые содержат семейства повторов ДНК. Но среди повторов в прицентромерных участках могут содержаться и гены. В прошлой версии генома не хватало нормальной структуры правильно ориентированных рибосомальных генов. Это очень важные гены, активно экспрессирующиеся и, по числу копий, весьма полиморфные среди разных людей. И теперь было четко определено, как они устроены, в новой версии генома в данной клеточной линии имеется около 200 рибосомальных генов. Кроме того, среди новых генов были выделены так называемые паралогичные гены (имеющие копии похожих генов), которые раньше пропускали. Вот, если кратко, то вся история. Эта последовательность теперь может быть использована как последняя версия референсного генома. На самом деле и в нем есть участки, где, скажем так, предполагается возможность ошибки, но таких участков гораздо меньше.
ДНК — проводник в прошлое
Давайте перейдем к вашим работам с древней ДНК. Где вы ее выделяете и секвенируете? И насколько дорого исследовать древний геном?
Вся работа проводится в России. И выделение древней ДНК, и приготовление так называемых геномных библиотек, и геномное секвенирование, и анализ. Головное учреждение в проекте — это «Сириус», у нас там полностью сделана платформа для геномного секвенирования, все работает. В работу вовлечены и московские генетические лаборатории, в которых есть условия для выделения древней ДНК. Конечно, такая работа осуществляется в рамках консорциума, в сотрудничестве с нашими коллегами — археологами и антропологами, которые профессионально описывают и предлагают образцы для исследований.
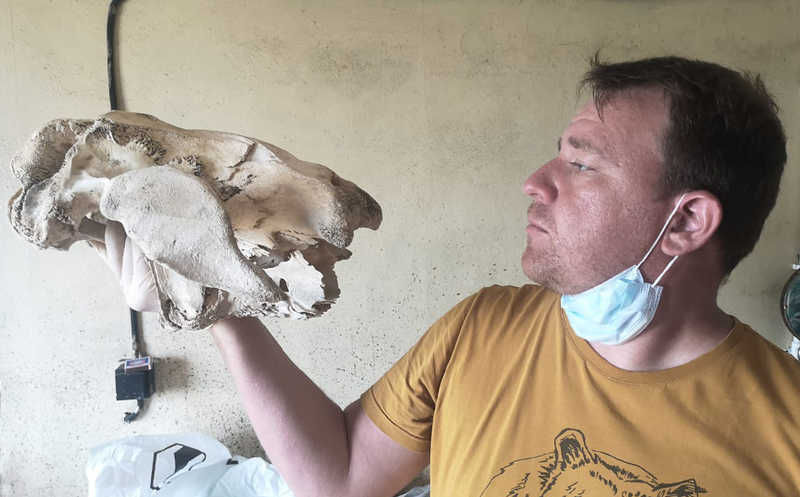
Стоимость секвенирования древнего генома на порядок больше, чем для современного. Знаете, почему? Нет, дело не только в плохой сохранности древней ДНК. И не в необходимости создания особо чистых условий в специальных помещениях лаборатории. Мы знаем, как эффективно контролировать и вычищать возможные загрязнения современной ДНК или ошибки, связанные с повреждениями древней ДНК. Это делается как на уровне экспериментальной работы, так и на уровне биоинформатического анализа. Основные затраты идут не на выделение ДНК или приготовление геномных библиотек, а на химические реагенты, которые используются для определения нуклеотидных последовательностей на современной платформе глубокого секвенирования. При работе с древней ДНК бóльшая часть реагентов тратится не на секвенирование эндогенной ДНК человека, а на ДНК микробов, обильно загрязняющих кость. Раньше считалось, что лучше всего ДНК сохраняется в зубах, но оказалось, что костные фрагменты височных участков черепа, в первую очередь слуховые косточки, намного лучше для этого подходят. Там может содержаться наибольшая пропорция геномной ДНК человека относительно загрязняющей микробной ДНК.
Расскажите про ваш проект исследования генетической истории России. Как я поняла, в этом проекте временные рамки очень широкие, от палеолита до формирования древнерусской общности. С какими образцами вы работаете? Каких археологических культур?
Проект называется «Генетическая история древнего населения Русской равнины». Про результаты сейчас говорить преждевременно, потому что мы еще мало что опубликовали. Сам проект заключается в следующем. Европейскую часть нашей страны занимает Восточно-Европейская, или Русская равнина, простирающаяся от Баренцева и Белого морей на севере до южных морей, а на востоке — до Уральских гор. И в этом обширном географическом ареале, который нас интересует, мы хотели бы исследовать все эпохи, для которых найдены и собраны коллекции антропологических и археологических материалов: от палеолита до средних веков. Чтобы реконструировать историю многочисленных культур и народов, сменявших друг друга или сосуществующих на этой территории на протяжении тысячелетий или столетий. Мы решили начать с исторического периода скифов, начавшегося в раннем железном веке, с одной стороны, и с другой стороны — с периода формирования восточнославянских племен и древнерусской общности в ранние средние века в восточноевропейской части. Вот две условные исторические точки, которые нас сейчас интересуют. Между ними есть промежуток времени, менее тысячи лет. Его тоже надо заполнять, но сначала нужно разобраться с биологическими образцами (костными фрагментами) из погребений скифской культуры и средневековых археологических памятников на этой территории. И мы уже получили геномные данные по большому количеству древних образцов.
Ключевой вопрос проекта — создание древнерусской общности. Сейчас мы исследуем обширные коллекции ранних средних веков вместе с нашими ведущими археологами и антропологами и их сотрудниками. Особый интерес представляют северные захоронения и археологические памятники, связанные с Северной Русью, этим занимается Николай Андреевич Макаров и Институт археологии. У них добыто много образцов, в том числе в ходе недавних раскопок и археологических исследований современными методами, что особенно ценно. Также благодаря сотрудничеству с Александрой Петровной Бужиловой у нас есть возможность исследовать ценные коллекции из НИИ и музея антропологии МГУ. Они включают образцы раннего средневековья и предшествующих эпох, найденные на территории Русской равнины. Генетические исследования древних образцов позволят прояснить историю восточного славянства. А для понимания генетической истории в контексте современных популяций нужно создать хорошую базу данных геномов современных русских, белорусов, украинцев и других народов, проживающих на сопредельных территориях. Таких полноценных данных еще нет, поэтому для нашей страны актуальным был бы запуск отдельного проекта по секвенированию современных геномов народов России.
Особый интерес представляют совсем древние образцы времён палеолита, возраст которых более 20 тысяч лет. Это крайне редкие, единичные находки. К сожалению большая часть таких находок, найденных на нашей территории, уже была передана ранее в западные лаборатории. Мы очень заинтересованы в генетическом исследовании таких образцов, которые и можно и нужно исследовать в России.
У вас недавно вышла статья по геному древнего ярославца времен нашествия Золотой Орды.
Это просто небольшой кусочек работы, показавшей на основе анализа митохондриальной линии его более вероятное европеоидное, а не азиатское происхождение, как можно было бы предположить на основе некоторых антропологических описаний.
Загадка бессмертной медузы
Вы директор Научного центра генетики и наук о жизни Университета «Сириус». Какие геномные проекты там идут?
Если про наши проекты, то есть «столетний геном». Мы секвенируем и анализируем геномы ста столетних людей, жителей России, чтобы найти генетические и эпигенетические варианты, связанные с защитой от болезней пожилого возраста и с долголетием. Заканчивается проект по реконструкции последовательности de novo генома соболя и куницы, там были получены интересные результаты по межвидовому скрещиванию. Ну и проект, связанный с «бессмертной» медузой, самый наш любимый, хотя, наверное, самый трудоемкий.
Это медуза, у которой бесконечный жизненный цикл, потому что она может превращаться обратно в полип? Она вас интересует просто как биологический феномен или есть связь между ее бессмертием и вашим исследованием долгожителей, например?
Что считать бессмертием? Можно считать, что мы все — это продолжение бессмертной зародышевой линии, germline, которая передается из поколения в поколение. А соматические клетки смертны, у животных всегда есть онтогенетически ограниченный период существования. Но мы знаем, что есть механизм, когда с помощью манипуляции транскрипционными факторами in vitro можно дифференцированные соматические клетки превращать обратно в недифференцированные клетки.
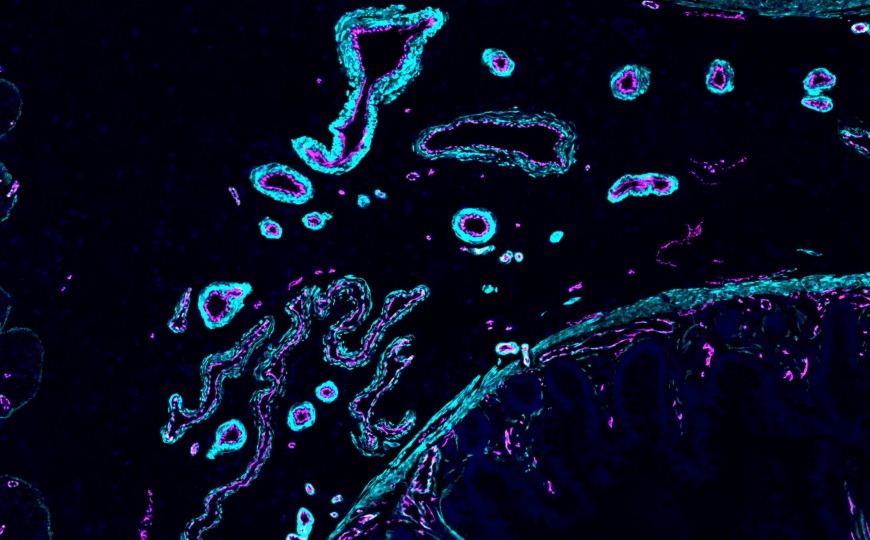
 Слева — «бессмертная» медуза Turritopsis dohrnii, справа — полип, от которого отпочковываются медузы. Из архива лаборатории в ИОГене
Слева — «бессмертная» медуза Turritopsis dohrnii, справа — полип, от которого отпочковываются медузы. Из архива лаборатории в ИОГене
Возвращать плюрипотентность?
Да. In vitro мы можем это сделать, но мы не видим, чтобы это происходило in vivo. Более того клетки кожи — фибробласты можно напрямую с помощью только одного транскрипционного фактора превращать в клетки мышц. Опять же в условиях in vitro. Процесс, который называется трансдифференциацией. Как раз поэтому нас заинтересовали кишечнополостные, в первую очередь, Turritopsis dohrnii. Это уникальный организм, для которого была показана удивительная возможность обратного развития. Как и у всех кишечнополостных, у нее медуза отпочковывается от полипа, но при определенных условиях она может превращаться обратно в полип. Такая трансформация происходит через соматические клетки, половые клетки в этом не участвуют. Вопрос в том, как именно репрограммируется геном и происходит такое возвращение в исходное состояние.
Вы пытаетесь это понять, исследуя ее геном? И откуда вы берете животных?
Мы научились содержать и разводить этих медуз в лаборатории. Это очень большой успех, потому что это весьма трудоемкий процесс. Запуск циклов обратного развития также изучаем в лаборатории. И мы уже получили большой объём геномных и эпигеномных данных.
«Королевская болезнь» и волосы царевича
А что в исследовании бывает самым интересным?
Когда удается решить проблему с помощью успешно найденного, красивого методического приёма. Например, в работе по выявлению гена «королевской болезни крови» — как мы установили, гемофилии формы В, которой страдали члены королевских семей Европы, включая царевича Алексея Романова. Конечно, найти мутацию было само по себе интересно, и тем самым решить историческую загадку. Но вот что не освещалось в медийном пространство и было описано в приложении статьи — так это подход, который мы использовали для доказательства патогенности найденной мутации. Надо было как-то доказать, что мутация, которую мы обнаружили в некодирующем сайте на границе с экзомом, —это не просто безобидный генетический полиморфизм. Сначала мы клонировали геномный участок, содержащий мутантный вариант гена, при этом использовали деградированную геномную ДНК, выделенную из исторического образца. Затем этот участок, содержащий экзон и сайт с мутацией, мы поместили между двумя другими экзонами в специальную плазмиду. После этого трансформировали этой плазмидой культуры клеток хомячка и человека и показали, что найденная мутация влияет на сплайсинг, что доказывает ее патогенный характер.
Получается, что вы нашли механизм, по которому эта мутация ведет к гемофилии?
Да, мы показали, что за счет этой мутации нарушается сплайсинг, возникает сдвиг рамки считывания. И с использованием методов глубокого секвенирования показали, что меняются транскрипты – на клеточных культурах. Это была такая хорошая придумка.
 Царевич Алексей с матерью
Царевич Алексей с матерью
Расскажите про еще одну недавнюю статью, о портрете царевича Алексея.
Это статья про выяснение аутентичности биологического образца в музейном экспонате, с помощью чего определилась музейная ценность портрета. История такая. В Государственном историческом музее хранилась картина, написанная акварелью, очевидно, портрет царевича Алексея, сына последнего российского императора Николая II и его супруги Александры Фёдоровны. В портретную рамку был вмонтирован ларец, в котором содержалось несколько волосков. Нас попросили определить, возможен ли генетический анализ для выяснения их происхождения. Волосики были очень тоненькими, без корней, и казалось маловероятным получить информативный результат по ДНК. Но как-то между делом мы попробовали провести такой анализ. Тем временем мы готовили и последние заключения в Следственный комитет по идентификации царской семьи Романовых. Оказалось, что удается извлечь ДНК из единичного волоса, но в чрезвычайно малом количестве и в виде фракции очень маленьких фрагментов разрушенной ДНК. Размер большинства таких фрагментов был даже меньше минимального, требуемого для геномного анализа древних образцов. Несмотря на это, нам удалось восстановить информативные участки митохондриальной ДНК. Оказалось, что именно этот митохондриальный тип мы ранее выявили у Александры Федоровны и ее детей, включая царевича Алексея. Такой вариант митохондриального генома Александра унаследовала от своей бабушки, британской королевы Виктории. Эта работа стала примером использования генетического подхода для определения музейного статуса экспоната.
«Если есть знание, оно может когда-то выстрелить»
Не могу не спросить про болезнь Альцгеймера. Вы ведь участвовали в самом первом исследовании ее генетической природы, когда открыли гены пресенилинов?
Мы это сделали еще в середине 90-х прошлого столетия, когда работали в составе международного консорциума. В основном эта работа проводилась в Канаде. Пресенилины — это ферменты, расщепляющие белок-предшественник бета-амилоидов, которые образуют амилоидные бляшки в сосудах. Потом, в нашей московской лаборатории, мы нашли целое семейство генов и белков, которые дистанционно гомологичны пресенилинам, но имеют совсем другие функции. Стало ясно что существуют семейства генов особых клеточных ферментов - аспартатных протеаз, которые обладают необычной способностью «разрезать» другие белки, в частности рецепторы, внутри мембран. И тем самым регулировать разные клеточные процессы.
Вы говорили, что молекулярный механизм болезни Альцгеймера сейчас ясен. А почему тогда не удается найти методы лечения? Можете предположить?
Могу только рассуждать об этом. Мы знаем первичный механизм болезни. Ключевой этап — это расщепление амилоидного предшественника ферментами пресенилинами. На самом деле для этого необходимы два фермента: один расщепляет белок-предшественник с внешней поверхности мембраны, другой, а именно пресенилин, расщепляет его внутри мембраны. В результате образуются короткие патогенные бета-пептиды длиной 40-42 аминокислоты, которые формируют амилоидные бляшки. Это при болезни Альцгеймера происходит всегда. Мутации генов пресенилинов усиливают такое расщепление или сдвигают его к более фибрилогенному пептиду. Но даже если нет мутаций, механизм тот же. Возникают еще нейрофибриллярные клубки в нейронах, они связаны не только с болезнью Альцгеймера, но и с другими деменциями, тоже потенциальная мишень. Мы можем разрабатывать лекарство на пресенилины, на сам бета-пептид, или на бляшки, когда они уже возникли. Априори лучше воздействовать на первичный механизм. Ингибиторы пресенилинов есть. Но дело в том, что пресенилины очень важны для других процессов — для расщепления многих других трансмембранных белков, включая клеточные рецепторы. Они расщепляют рецептор, чтобы освободить внутриклеточную сигнальную часть белка. Вообще, открытие пресенилинов важно не только для понимания механизмов болезни Альцгеймера, но и для фундаментальных механизмов клеточной сигнальной трансдукции. Если мы подавим пресенилины, то эта сигнальная трансдукция будет нарушаться, что может приводить к очень негативным эффектам. Поэтому пока существующие ингибиторы пресенилинов не считаются перспективными терапевтическими молекулами.
Было очень много клинических испытаний потенциальных препаратов, воздействующих непосредственно на бета-пептид или амилоидные бляшки, которые ни к чему хорошему не привели. Периодически появляются статьи, в том числе в выдающихся журналах, сообщающих о разработке вариантов моноклональных антител, которые элиминируют бляшки. На мышах такой эффект убедительно показали, но в клинических испытаниях он не особо выражен. Одно из объяснений — то, что у больных Альцгеймером уже началась дегенерация нейронов, и воздействовать поздно. Так что сегодня большинство фармкомпаний и лекарственных агентств уже не поддерживают разработку препаратов против бета-пептида.
Риск болезни Альцгеймера (в научной литературе используется сокращение БА) повышен у носителей варианта гена АРОЕ е4, который встречается в 10% европейской популяции, в том числе в России. Один из подходов, который мы применили с коллегами из Медицинской школы Массачусетского университета, — это разработка малых интерферирующих РНК, подавляющих активность АРОЕ в мозгу. Пока это сделано на моделях животных. Еще мы поучаствовали в работе с коллегами из Национального института здоровья, в которой использовали трансгенные модели БА на мышах. С возрастом возникает хронический воспалительный процесс. Один из вопросов — не играет ли это роль в развитии БА, и можно ли этот процесс как-то подавлять? В эксперименте мы подавляли образование иммунных В-клеток и обнаружили снижение патогенных процессов и улучшение когнитивных способностей у модельных мышей.
В целом, болезнь Альцгеймера — это пример того, что, несмотря на в значительной степени выясненный механизм болезни, подход к разработке лекарства, направленный на первичную мишень, не всегда действует. Но если есть знание, оно может когда-то выстрелить.








 Меню
Меню





 Все темы
Все темы




 0
0