Белок S1 коронавируса проникает через гематоэнцефалический барьер мышей
В ходе экспериментов на мышах ученые показали, что белок S1 коронавируса при внутривенном введении преодолевает гематоэнцефалический барьер за счет абсорбцио-опосредованного трансцитоза. Белок обнаруживался во всех отделах мозга. При интраназальном введении S1 поглощался тканями мозга менее эффективно.
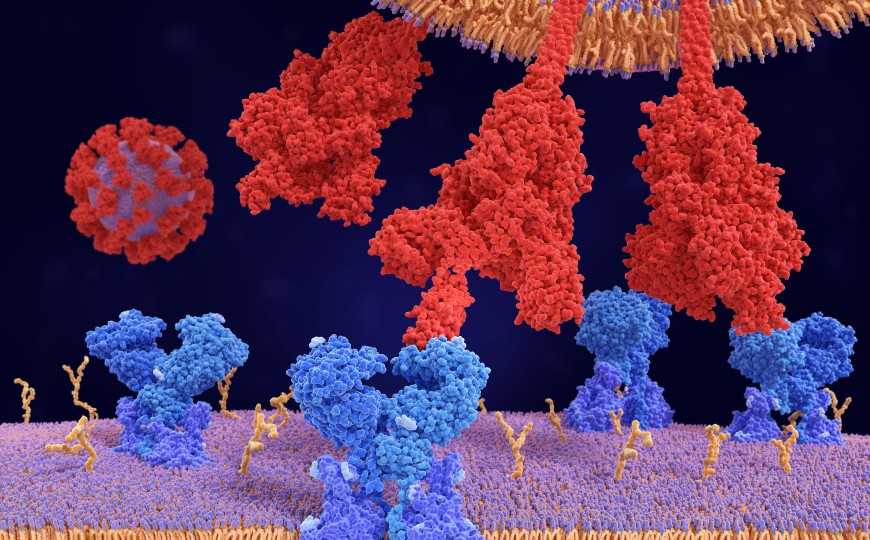
У пациентов с COVID-19 часто наблюдаются неврологические симптомы, такие как потеря обоняния и вкуса, головная боль, слабость и тошнота. Вирусную РНК обнаруживали в головном мозге и спинномозговой жидкости. Эти факты дают основания полагать, что коронавирус SARS-CoV-2 способен проникать в центральную нервную систему, однако механизмы проникновения пока неясны. В новой работе, опубликованной в Nature Neuroscience, ученые из США показали, что субъединица S1 S-белка коронавируса преодолевает гематоэнцефалический барьер (ГЭБ) мышей.
Ученые сосредоточились на белке S1, так как именно он связывается с клеточным рецептором ACE2, обеспечивая заражение клетки вирусом. Они работали с коммерчески доступным чистым S1. Белок пометили радиоактивным иодом и ввели мышам внутривенно. Меченый S1 (I-S1) легко проходил через гематоэнцефалический барьер — в течение 30 минут 50% белка преодолевало капиллярную стенку и оказывалось в паренхиматозном пространстве мозга. I-S1 обнаруживался во всех отделах мозга, при этом не было статистически значимых различий в поглощении белка разными отделами. Происходил также клиренс I-S1 из кровотока тканями печени, почек, легких и селезенки.
Для уточнения механизма, который позволяет белку преодолевать ГЭБ, ученые ввели мышам I-S1 вместе с агглютинином зародышей пшеницы (WGA). WGA проникает в мозг за счет абсорбцио-опосредованного трансцитоза: он связывается с гликопротеинами эндотелиальных клеток сосудов, интернализуется в везикулы и транспортируется через мембрану. Гликопротеины, подходящие для WGA, должны содержать сиаловую кислоту и N-ацетилглюкозамин. Многие вирусные белки связываются с гликопротеинами такого же состава, поэтому коинъекция WGA и вирусных белков увеличивает способность последних проникать в мозг и другие ткани. Введение мышам I-S1 с WGA увеличило интенсивность клиренса белка из кровотока. Это говорит о том, что I-S1 также использует абсорбцио-опосредованного трансцитоза, связываясь с гликопротеинами, содержащими сиаловую кислоту и N-ацетилглюкозамин. Такой вывод был подтвержден экспериментом с одновременным введением I-S1 и немеченного S1. Дополнительный S1 не повлиял на поглощение I-S1 тканью мозга, то есть сайт связывания I-S1 не так легко насытить, а это еще один признак адсорбционного трансцитоза.
После интраназального введения I-S1 также обнаруживался во всех отделах мозга мышей. Это значит, что SARS-CoV-2 может проникать в мозг через обонятельный нерв, однако такой путь менее эффективен, чем транспорт через ГЭБ.
Факторами риска смерти от COVID-19 считаются мужской пол и генотип APOE4. В завершающем эксперименте авторы проверили, влияют ли эти факторы на преодоление ГЭБ белком I-S1. Для этого они внутривенно вводили меченый белок мышам мужского и женского пола, несущих человеческие APOE4 или APOE3. Накопление I-S1 в мозгу не зависело от пола или генотипа APOE, однако у самцов мышей, несущих APOE3, было зарегистрировано повышенное поглощение белка в обонятельных луковицах, печени и почках. Это значит, что усиленное поглощение I-S1 тканями может вносить вклад в повышенный риск COVID-19 для мужчин, однако нет ассоциаций между риском COVID-19 и генотипом APOE4.
Источник
Rhea, E.M., et al. // The S1 protein of SARS-CoV-2 crosses the blood–brain barrier in mice. // Nature Neuroscience (2020); DOI: 10.1038/s41593-020-00771-8


 Меню
Меню





 Все темы
Все темы




 0
0











