Человеческий эндотелий вырастили в свиных эмбрионах
При выращивании донорских органов в животных желательно, чтобы все клетки органа имели человеческое происхождение, в том числе эндотелий сосудов, который контактирует с кровью и клетками иммунной системы. Исследователям удалось вырастить человеческий эндотелий в эмбрионах свиньи.
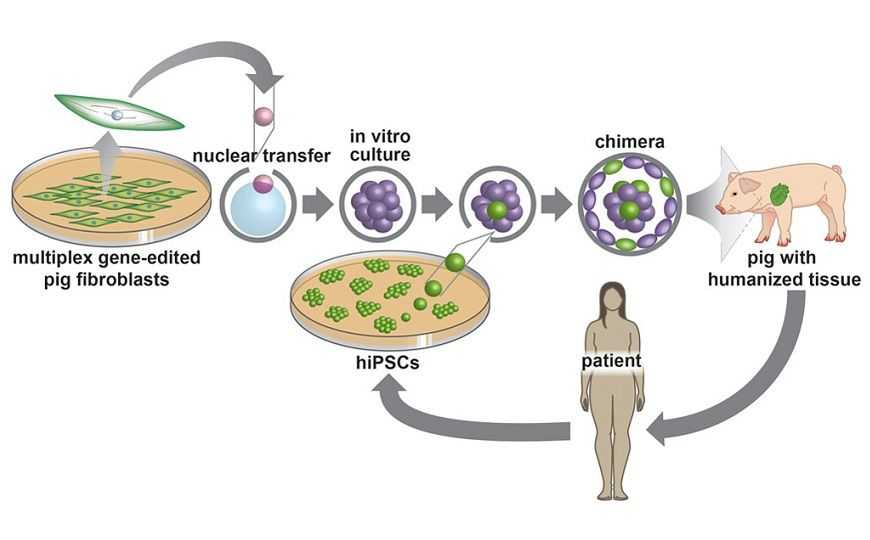
Человеческие индуцированные плюрипотентные клетки можно использовать для создания гуманизированных органов, внедряя их в бластоцисту свиньи. (Из статьи Мэри Гэрри и Дэниела Гэрри, в которой рассматривается возможность создания гуманизированного сердца для трансплантации.)
Человеческие органы теоретически можно выращивать в животных, после чего пересаживать их пациентам. Подобные техники исследуют на эмбрионах животных, у которых выключают регуляторный ген, отвечающий за развитие какого-либо органа. Например, плюрипотентные стволовые клетки (ПСК) крысы могут сформировать поджелудочную железу в мышиных эмбрионах с неработающим геном Pdx1, и наоборот. Однако эндотелий сосудов такого органа все равно образован из клеток хозяина, что может спровоцировать реакцию отторжения при пересадке.
Чтобы решить эту проблему, группа исследователей под руководством Мэри Гэрри и Дэниела Гэрри из Университета Миннесоты попробовала вырастить донорский эндотелий в мышиных и свиных эмбрионах с выключенным геном ETV2. Этот транскрипционный фактор отвечает за кроветворение и формирование эндотелия сосудов. Без него эмбрионы рано погибают, поскольку у них нет гематоэндотелиальных клеток — предшественников клеток крови и выстилки сосудов.
Сначала авторы статьи ввели меченные желтым флуоресцентным белком эмбриональные стволовые клетки (ЭСК) мышей в мышиные эмбрионы, нокаутные по ETV2. Такие химерные эмбрионы выживали, а их гематоэндотелиальные клетки светились желтым. Следовательно, меченые ЭСК дикого типа смогли восстановить их популяцию в мутантных эмбрионах.
С помощью клонирования исследователи получили свиные эмбрионы с выключенным ETV2. У них нарушался рост, не формировались сосуды, не было популяций кроветворных и эндотелиальных клеток через 18 дней после начала развития. На стадии 4 дней авторы ввели в такие эмбрионы свиные бластомеры — клетки раннего эмбриона — дикого типа, меченные зеленым флуоресцентным белком. На 18-й день зеленую метку обнаружили и в клетках крови, и в выстилке сосудов. Значит, предложенный способ получения донорского эндотелия работает и для свиных эмбрионов.
Затем ученые оценили эффективность добавления человеческих индуцированных плюрипотентных стволовых клеток (иПСК) в свиные эмбрионы. Сначала иПСК вводили в эмбрионы, полученные партеногенезом (активацией зрелой яйцеклетки), которые выращивали in vitro. Хотя часть иПСК погибала, те, что успешно вживлялись в эмбрионы, формировали функциональные контакты с клетками хозяина и делились. После этого иПСК вводили в эмбрионы с выключенным ETV2, которые подсаживали суррогатным самкам и анализировали на 17-18 день развития. Как и ожидалось, иПСК давали начало эндотелиальным клеткам. Эффективность получения таких химер была низкой — при подсаживании часть иПСК погибала путем апоптоза. Авторам удалось повысить эффективность: они гиперэкспрессировали антиапоптотический фактор BCL2 в иПСК перед введением в эмбрионы.
По мнению авторов, дальнейшие исследования увеличат эффективность создания химер. Также из иПСК можно получать другие органы в эмбрионах животных. Тем не менее, авторы не оценили безопасность повышения экспрессии BCL2 для последующей трансплантации.
Источник
Satyabrata Das et al. // Generation of human endothelium in pig embryos deficient in ETV2. // Nature Biotechnology, 2020; DOI: 10.1038/s41587-019-0373-y


 Меню
Меню





 Все темы
Все темы




 0
0