Экструзии в первую очередь подвергаются эпителиальные клетки с недостатком АТФ
Для нормального функционирования органов и поддержания плотного монослоя эпителиальным клеткам необходимо работать сообща. Поэтому клетки, способные нарушить какой-либо из этих процессов, устраняются в первую очередь. Исследователи из Великобритании и США показали, что при скучивании клеток механически активируемый канал ENaC накачивает в клетку Na+, вызывая деполяризацию мембраны, активацию потенциалзависимых K+ каналов Kv1.1 и Kv1.2, сжатие клетки за счет выхода воды и ее экструзию (выдавливание) из монослоя. При наличии достаточного количества АТФ клетка может удалить избыток Na+ с помощью Na+/K+ АТФазы, восстановить баланс своего мембранного потенциала и остаться в монослое, тогда как при недостатке АТФ происходит экструзия.
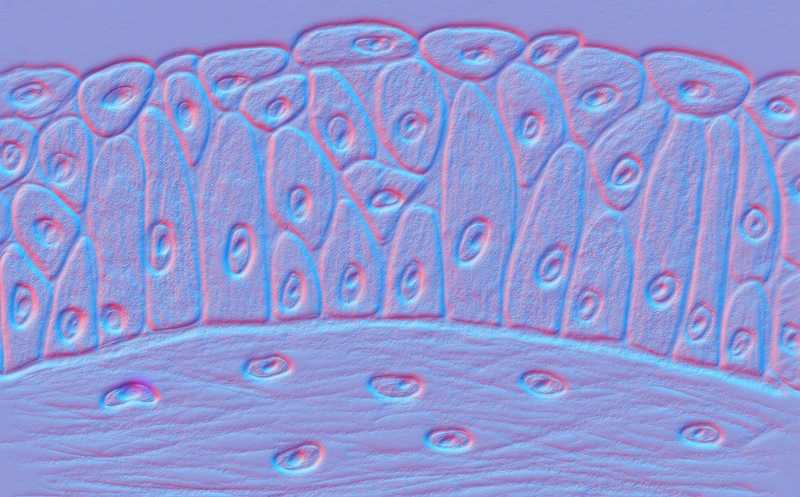
Экструзия (выдавливание) клеток — консервативный механизм поддержания числа клеток в эпителии, характерный как для губок, так и для человека. Во время экструзии живая клетка выталкивается за счет скоординированного базолатерального сокращения актомиозина выталкиваемой клетки и ее соседей. После экструзии клетка погибает из-за отсутствия сигналов, необходимых для выживания. Ранее исследователи из Великобритании и США показали, что экструзию активирует Piezo1, который сам активируется в ответ на скученность эпителиальных клеток. Piezo1 запускает канонический путь, основанный на секреции липида сфингозин-1-фосфата (S1P), который связывается с рецептором S1P2, сопряженным с G-белком, и активирует Rho-опосредованное сокращение актомиозина, необходимое для экструзии. Этот же путь S1P–S1P2–Rho отвечает за экструзию апоптотических клеток, гарантируя отсутствие зазоров в монослое. В новой работе те же авторы попробовали понять, какие именно клетки подвергаются экструзии.
Сначала исследователи предположили, что из эпителиального слоя удаляются клетки с наименьшей массой, но эта гипотеза не подтвердилась. Также экструзии не предшествовал всплеск концентрации Ca2+. Однако авторы отметили признаки снижения объема клетки или изменения ее формы. Действительно, около 70% клеток сжимаются перед экструзией, тогда как <0,03% клеток (8 из 750) сжимаются без экструзии. Неясно, почему оставшиеся 30% клеток не уменьшаются в объеме. Авторы предположили, что эти клетки подвергаются апоптотическому вытеснению. Интересно, что сжатие клетки, по-видимому, предшествует активации Piezo1.
Кратковременное изменение осмолярности провоцировало экструзию большого числа клеток. Однако даже при обработке гипертоническим раствором не все клетки сжимались одинаковым образом. Те клетки, объем которых уменьшился на 20%, удалялись из монослоя, на 11% — оставались в монослое.
Исследователи проверили, способны ли какие-то ингибиторы ионных каналов заблокировать экструзию. Они использовали библиотеку ингибиторов K+ и Cl− каналов. Все протестированные ингибиторы значительно подавляли экструзию. А 4-AP, ингибитор потенциалзависимых каналов Kv1.1 и Kv1.2, блокирует также апоптотическую экструзию. Но только DCPIB (с zVAD-fmk) и 4-AP, которые нацелены на Cl− канал SWELL1 и потенциалзависимые K+ каналы Kv1.1 и Kv1.2 соответственно, значительно блокировали сжатие клеток, вызванное гипертоническим раствором. Ингибиторы, блокирующие сигналы экструзии Piezo1, S1P и S1P2, не блокируют сжатие клеток в ответ на гипертонический раствор. Нокдаун каналов Kv1.1, Kv1.2 и SWELL1 предотвращали сжатие и экструзию.
Учитывая, что каналы Kv1.1 и Kv1.2, инициирующие сокращение и выталкивание клеток, являются потенциалзависимыми, авторы выяснили, может ли деполяризация мембраны инициировать выталкивание эпителиальных клеток. Действительно, клетки деполяризуются в среднем за 5 минут до сжатия и экструзии. Более того, несжимающиеся клетки не показывали признаков деполяризации. Активации выхода K+ оказалось недостаточно для индукции экструзии.
ENaC — высококонсервативный, механически активируемый канал, который вызывает деполяризацию посредством входа Na+ в клетку. Ингибирование ENaC амилоридом или подавление экспрессии любой из его субъединиц (α, β или γ) предотвращает как сжатие клеток под действием гипертонического раствора, так и экструзию. Скучивание клеток провоцирует вход Na+ в клетку зависящим от ENaC способом. Таким образом, скучивание клеток активирует зависимый от ENaC вход Na+, который вызывает деполяризацию мембраны, тем самым активируя потенциалзависимые калиевые каналы Kv1.1 и Kv1.2, отвечающие за сокращение клеток.
В конце авторы выяснили, какие именно клетки сожмутся и будут удалены. Na+/K+ АТФаза, которая необходима для реполяризации плазматической мембраны, отвечает за 30–70% всего потребления АТФ в клетке, в зависимости от типа клетки. Так что сжимаются клетки с низким уровнем АТФ. Кроме того, снижение уровня АТФ в клетке с помощью ингибитора митохондриальной АТФ-синтазы олигомицина А увеличило количество клеток, как сжимающихся, так и подверженных экструзии, по сравнению с контрольной группой. Добавление глюкозы к клеткам снижало скорость экструзии. Так что, вероятно, скучивание повышает уровень Na+, который не удаляется из клетки из-за недостатка энергии.
Для выполнения большинства функций органов и поддержания плотного монослоя эпителиальным клеткам необходимо работать сообща. Поэтому клетки, способные нарушить какой-либо из этих процессов, должны быть устранены в первую очередь. Эпителиальные клетки с достаточным количеством АТФ могут противостоять скучиванию, когда ENaC активирует вход Na+, используя Na+/K+ АТФазу для восстановления баланса своего мембранного потенциала. Однако скученные клетки с недостаточным уровнем АТФ для реполяризации мембран при активации ENaC не смогут откачивать Na+. Это повышение уровня Na+ в клетке активирует Kv1.1 и Kv1.2, вызывая сжатие клетки за счет выхода воды. Если клетка потеряет более 17% объема, активируется экструзия.
Один в поле не воин: как межклеточная адгезия помогает клеткам вытеснять конкурентов
Источник:
Saranne J. Mitchell, et al. Energy deficiency selects crowded live epithelial cells for extrusion: a Bayesian approach on a 14-year clinical data warehouse // Nature (2025), published 10 September 2025, DOI: 10.1038/s41586-025-09514-w


 Меню
Меню





 Все темы
Все темы




 0
0











