Гепатоциты для лечения печеночной недостаточности можно получать из химерных животных
Китайские ученые показали, что введение эмбриональных стволовых клеток мыши в бластоцисты крыс позволяет получить химерных животных, в печени которых много гепатоцитов мышиного происхождения. Гепатоциты химер обладали высокой степенью сходства с обычными мышиными гепатоцитами по функциональности и профилю экспрессии генов. Трансплантация «химерных» клеток мышам с фиброзом печени значительно облегчала симптомы заболевания. Таким образом, химерные животные перспективны в качестве источника гепатоцитов для трансплантации.
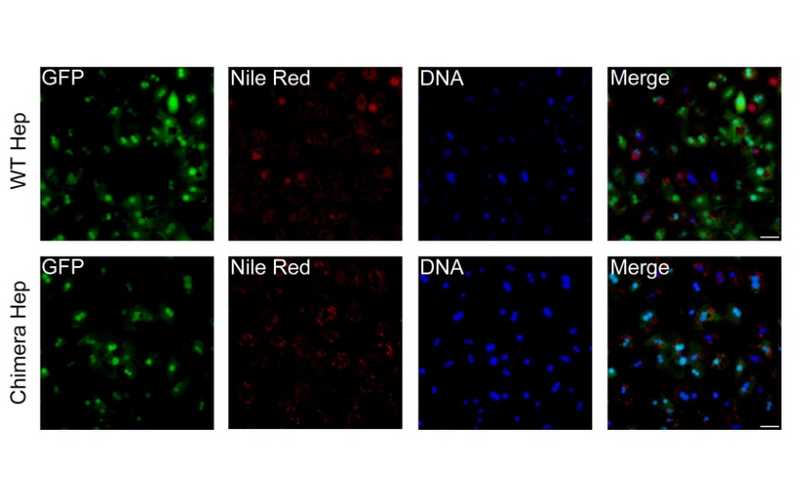
Мышиные гепатоциты, полученные из печени мышей дикого типа или химерных животных.
Credit:
Stem Cell Reports (2024). DOI:
10.1016/j.stemcr.2024.04.006 |
CC BY-NC-ND
Заболевания печени являются одним из острых вопросов здравоохранения во всем мире. К настоящему времени, при прогрессии заболевания к печеночной недостаточности (нарушении функции печени) единственным эффективным методом лечения служит трансплантация печени. При этом неизбежно возникает проблема недостаточного количества доноров. Одна из альтернатив к трансплантации целого органа — является трансплантация гепатоцитов, однако метода, позволяющего стабильно получать клетки высокого качества и отвечающие этическим нормам, к данному моменту не существует. Работа, опубликованная учеными из Китая, показала, что межвидовые химерные животные могут стать источником функциональных гепатоцитов для трансплантации.
Химерные животные — перспективное направлением для получения донорских клеток, тканей и органов. Ранее уже были успешно получены химерные почки, сердце, поджелудочная и другие органы. Однако данных, подтверждающих возможность получения функциональных гепатоцитов, до настоящего времени не существовало.
Для получения химерных животных ученые сначала вывели линию эмбриональных стволовых клеток мышей, экспрессирующую зеленый флуоресцентный белок (GFP). Далее стволовые клетки вводили в бластоцист крысы, который подсаживали самке. Химерность полученного потомства ученые подтвердили при помощи флуоресцентного анализа и ПЦР-тестирования на присутствие видоспецифичных вариантов гена Gapdh. Сортировка флуоресцентно-активированных клеток (FACS) показала, что печень химерных животных содержит 15–17% GFP-положительных клеток.
Анализ изолированных от химерных животных гепатоцитов показал, что они экспрессируют нормальные молекулярные маркеры. Доля GFP-положительных гепатоцитов составила 34–49%. При этом клетки мышиного происхождения обнаруживались не только в паренхиме, но и в желчных каналах.
Далее ученые отобрали только гепатоциты мышиного происхождения для изучения их функциональности in vitro. Было показано, что сортировку переживают около половины всех клеток. Выжившие GFP-положительные гепатоциты демонстрировали нормальную функцию в лабораторных условиях — накапливали жиры и гликоген на уровне гепатоцитов дикого типа (WT), а также синтезировали мочевину и экспрессировали типичные молекулярные маркеры гепатоцитов.
Профиль экспрессии генов GFP-положительных гепатоцитов соответствовал профилю нормальных гепатоцитов, при этом GFP-положительные клетки однозначно идентифицировались как мышиные по профилю экспрессии. В сравнении с гепатоцитами, полученными другими лабораторными методами (такими как индукция из стволовых клеток и перепрограммирование фибробластов), клетки химер были значительно ближе к гепатоцитам дикого типа. В частности, они менее активно экспрессировали гены, ассоциированные с процессами апоптоза, клеточной смерти и воспаления, в то же время демонстрируя высокий уровень экспрессии генов, связанных с функцией печени. Таким образом, химерные животные позволяют получать гепатоциты, крайне близкие к нормальным эндогенным гепатоцитам.
Наконец, авторы протестировали эффективность трансплантации химерных гепатоцитов для лечения печеночной недостаточности. Опыты проводились на мышиной модели фиброза печени. Трансплантация полученных от химерных животных клеток мышам с искусственно индуцированным фиброзом приводила к тому, что поверхность печени становилась более гладкой уже на седьмой день после пересадки, тогда как у контрольных мышей с фиброзом она была неровной. Также наблюдалось снижение маркеров повреждения печени (аспартатаминотрансфераза, аланинаминотрансфераза) в крови, накопления коллагена в печени и степени фиброза тканей. Средняя эффективность приживления пересаженных гепатоцитов составила 8,74% (диапазон значений от 3,43% до 15,92%).
Таким образом, результаты работы показали, что химерные животные — перспективный подход к получению функциональных гепатоцитов для трансплантации при заболеваниях печени.
Источник
Huang et al., Functional mouse hepatocytes derived from interspecies chimeric livers effectively mitigate chronic liver fibrosis // Stem Cell Reports 19, 1-13, published May 9, 2024, DOI: 10.1016/j.stemcr.2024.04.006


 Меню
Меню





 Все темы
Все темы




 0
0