Глиомы используют глутамат для стимуляции своего роста вместо передачи электрических сигналов
Уже известно, что глутамат — главный возбуждающий нейромедиатор — способствует росту уже имеющихся опухолей, но молекулярный механизм этого процесса оставался неизученным. Исследователи из США обнаружили, что клетки пилоцитарной астроцитомы (разновидности детской глиомы) способны перепрограммировать свои глутаматные рецепторы, чтобы они стимулировали рост клетки вместо передачи электрического сигнала. Понимание данного механизма открывает перспективы для разработки новых подходов к лечению опухолей мозга.
Пилоцитарные астроцитомы — медленно растущие опухоли мозга (во многих случаях доброкачественные), которые зачастую возникают в жизненно важных областях мозга и нарушают его работу у детей. Уже известно, что нейроны способны поддерживать рост опухолей посредством глутаматного сигналинга, однако конкретные молекулярные механизмы оставались загадкой. Авторы работы в Neuron показали, что клетки пилоцитарных астроцитом обогащены рецепторами к глутамату — основному возбуждающему нейромедиатору. Обычно они обеспечивают передачу сигналов между нейронами, но в опухоли переключаются на стимулирование пролиферации.
Исследователи проанализировали ранее опубликованные данные секвенирования РНК единичных клеток и обнаружили повышенную экспрессию глутаматных рецепторов (GluR) в клетках пилоцитарной астроцитомы, а именно субъединиц GRID2 и GRIK3. Затем они провели эксперименты на клеточных культурах и на ксенографтной модели — мышам пересаживали фрагменты опухолевой ткани, полученные от пациентов с пилоцитарной астроцитомой. Нокдаун генов, кодирующих GRID2 и GRIK3, приводил к значительному снижению пролиферации опухолевых клеток. Добавление глутамата в физиологических концентрациях, напротив, ускоряло деление клеток опухоли, хотя их электрическая активность при этом не менялась. Это отличает пилоцитарные астроцитомы от злокачественных глиом, в которых глутамат вызывает изменение мембранного потенциала.
Чтобы проследить весь сигнальный путь, исследователи поэтапно блокировали его предполагаемые звенья при помощи малых образующих шпильки РНК (shRNA) и наблюдали за изменениями в клетках. Так они показали, что стимуляция глутаматных рецепторов ведет к активации тирозинкиназы Src (экспрессия которой в опухолях повышена) и активации тирозинкиназного рецептора PDGFRα, что вызывает запуск каскада киназы, регулируемой внеклеточными сигналами (ERK) — одного из ключевых онкогенных механизмов.
Авторы также протестировали на клеточных культурах и мышах фармакологические ингибиторы компонентов выявленного сигнального пути. Мемантин, антагонист глутаматных рецепторов, уменьшал пролиферацию клеток и тормозил рост опухоли; дазатиниб блокировал Src и предотвращал активацию PDGFRα; авапритиниб, селективный ингибитор PDGFRα, снижал активность ERK и подавлял деление клеток. Это доказывает, что именно последовательная активация GluR–Src–PDGFRα–ERK лежит в основе роста пилоцитарных астроцитом.
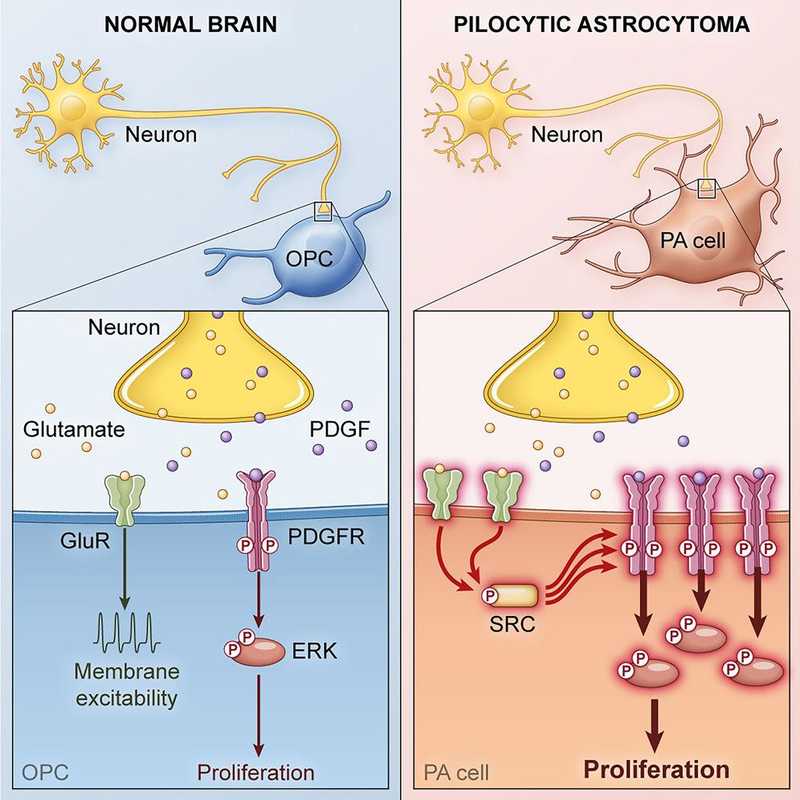
При стимуляции глутаматом мембрана клетки-предшественницы олигодендроцита (OPC) деполяризуется и проводит электрический сигнал (слева), а клетка опухоли мозга (PA) усиливает пролиферацию.
Credit:
Neuron (2025). DOI:
10.1016/j.neuron.2025.08.005 |
CC-BY-NC-ND 4.0
Авторы данной работы выявили, как опухоли мозга могут использовать нормальную нейронную активность в своих целях. Сделанное открытие не только объясняет связь между активностью нейронов и ростом глиом, но и намечает новые потенциальные стратегии терапии.
«Этот новый механизм роста опухоли объединяет два нормальных, но обычно не связанных между собой процесса в мозге — рост и электрическую передачу сигналов — в аномальной форме. Теперь, когда мы поняли, как эти клетки функционируют и растут, перед нами открываются безграничные перспективы изучения других нейромедиаторов и различных путей связи между нейронами и опухолевыми клетками», — комментирует доктор Корина Анастасаки, первый автор публикации.
Некоторые клетки глиомы обладают свойствами нейронов и глии одновременно
Источник
Corina Anastasaki, et al. Aberrant coupling of glutamate and tyrosine kinase receptors enables neuronal control of brain-tumor growth // Neuron 113, 1-19. Published online 1 September 2025. DOI: 10.1016/j.neuron.2025.08.005
Цитата по пресс-релизу


 Меню
Меню





 Все темы
Все темы




 0
0










