Иммунотерапия с помощью гидрогеля снижает вероятность рецидива опухоли у мышей
Ученые из США разработали новый метод для снижения вероятности рецидива после оперативного удаления солидных опухолей. Они инкапсулировали в биосовместимый гидрогель наночастицы с пексидартинибом и тромбоциты, конъюгированные с антителами к PD-1. Гидрогель имплантировали мышам на место удаленной опухоли. В результате снижалась местная плотность опухоль-ассоциированных макрофагов и увеличивалась плотность цитотоксических T-лимфоцитов.
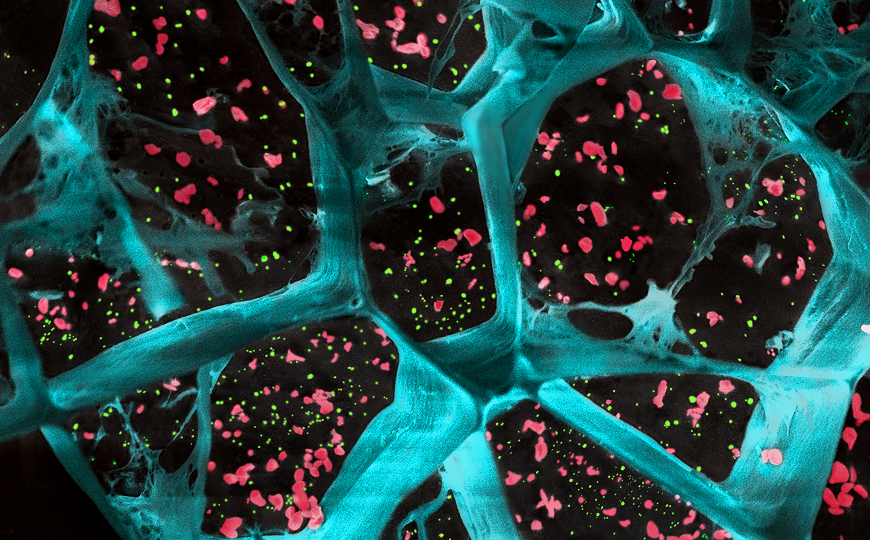
В гидрогеле (голубой) инкапсулированы тромбоциты (красные) и наночастицы (зеленые).
Credit:
UW–Madison |
Пресс-релиз
Хирургическое вмешательство остается основным методом лечения пациентов с солидными опухолями. При этом достаточно часто возникают рецидивы. Ингибирование контрольных точек иммунитета — многообещающий подход в борьбе с повторным развитием опухолей, однако его эффективность снижается из-за послеоперационного воспаления и вызванной им иммуносупрессии. В частности, ассоциированные с опухолью макрофаги выделяют большое количество противовоспалителтных сигнальных молекул. Это помогает раковым клеткам избежать внимания иммунитета и способствует повторному развитию опухоли и метастазированию. Есть корреляция между повышенным содержанием макрофагов в опухоли и возникновением рецидива, эта связь подтверждена клинически. Ранее исследования показывали, что истощение ассоциированных с опухолью макрофагов способствует инфильтрации CD8+ Т-лимфоцитов в опухоль.
Ученые из США предложили поместить одобренный FDA препарат пексидартиниб (Pexidartinib, PLX) в наночастицы из декстрана, и инкаспулировать их в альгинатный гидрогель. Пексидартиниб блокирует рецепторы CSF1 на поверхности опухолевых макрофагов, при этом практически не проявляет цитотоксичности в отношении остальных клеток. Препарат способствует истощению макрофагов, снижает иммуносупрессию и повышает уровень инфильтрации опухоли Т-лимфоцитами. В этот же гель исследователи поместили конъюгированные с антителами к PD-1 тромбоциты. В условиях воспаления тромбоциты выпускают эти антитела в окружающую среду, что помогает T-лимфоцитам узнавать и атаковать опухолевые клетки.
В in vitro экспериментах исследователи выяснили, что пексидартиниб высвобождается из гидрогеля постепенно, и при рН=6,5 спустя пять дней в окружающую среду попадает 50,3% вещества. In vivo через такой же промежуток времени из геля высвободилось примерно 33,7% препарата.
Авторы работы проверили действие гидрогеля на мышиной модели: гель с пексидартинибом имплантировали после операции по удалению меланомы. Плотность макрофагов в области действия геля снизилась в 2,3 раза по сравнению с одним пексидартинибом. Одновременно в два раза увеличилась плотность CD8+ Т-лимфоцитов.
Затем ученые проверили эффективность гидрогеля с пексидартинибом и иммунотерапевтическими тромбоцитами в профилактике рецидивов рака толстой кишки и меланомы. Такая комбинация также оказалась эффективной: она защищала мышей от повторного развития опухолей лучше, чем монотерапия, и увеличивала продолжительность жизни животных. При этом исследователи отметили, что вес мышей не снижался, то есть лечение не было токсичным. В месте имплантации гидрогеля плотность макрофагов снижалась на 73,7% по сравнению с контрольной группой.
Кроме того, авторы работы провели эксперименты на мышиной модели рака молочной железы и показали, что предложенная ими комбинация значительно снижает количество метастатических узлов в легких мышей после операции по удалению опухоли. Схожие результаты ученые получили и на модели саркомы.
Также ученые оценили комбинацию геля с пексидартинибом и системным введением тромбоцитов с антителами, блокирующих рецепторы PD-1. В других группах мышам либо не назначали иммунотерапию, либо вводили свободные антитела, не прикрепленные к тромбоцитам. Авторы работы пришли к выводу, что конъюгация с тромбоцитами увеличивает время циркуляции антител в крови. Кроме того, это позволяет сосредоточить их возле места операции. Таким образом, доставка ингибиторов контрольных точек иммунитета при помощи тромбоцитов оказалась более эффективным подходом для послеоперационной терапии.
В новой работе ученые показали, что гидрогель можно использовать для постепенной доставки лекарственных средств в место операционного вмешательства после удаления опухоли. Местное применение пексидартиниба позволила значительно ослабить иммуносупрессивное действие макрофагов и усилило эффект как местной, так и системной иммунотерапии.
Источник
Zhaoting Li, et al. Depletion of tumor associated macrophages enhances local and systemic platelet-mediated anti-PD-1 delivery for post-surgery tumor recurrence treatment. // Nature Communications 13, 1845 (2022), published 6 April 2022. DOI: 10.1038/s41467-022-29388-0


 Меню
Меню





 Все темы
Все темы




 0
0











