Инициацию различных типов глиобластом вызывают всего три генетических фактора
Ученые из Немецкого центра исследования рака исследовали пути эволюции глиобластомы и выявили три основных типа генетических перестроек, которые могут вызвать развитие опухоли в течение семи лет. Однако закономерных генетических изменений, вызывающих рецидивы глиобластомы, найдено не было.
Глиобластома — достаточно распространенный тип злокачественной опухоли среди взрослого населения. Опухоль диффузно прорастает в здоровые ткани головного мозга, поэтому ее хирургическое удаление редко бывает успешным. Последующие радио- и химиотерапия не убивают оставшиеся опухолевые клетки, и глиобластома разрастается вновь, вызывая рецидивы.
Существует предположение, что устойчивость опухолевых клеток к клиническим манипуляциям определяется набором специфических мутаций. Если это так, то возможно, что лечение оказывает избирательное действие на глиобластому, оставляя в живых клетки, имеющие подобные мутации. Эту гипотезу решили проверить ученые из Немецкого центра исследования рака. Они взяли образцы тканей головного мозга пациентов с глиобластомой. Затем провели полногеномное секвенирование 21 пары образцов — глиобластомы и крови пациента в качестве контроля, а также проанализировали транскриптомы опухолевых образцов. Для 43 пациентов выполнили таргетное секвенирование 50 генов, связанных с глиомами, в образцах первичных и рекуррентных опохолей, и сравнили их метиломы. Основываясь на полученных данных, исследователи разработали математическую модель развития опухоли.
Выяснилось, что при развитии первичной глиобластомы, вне зависимости от ее типа, который определяется по различиям метилирования, всегда присутствовала хотя бы одна из трех хромосомных перестроек: потеря полной 10-й хромосомы или плеча q, включая локус PTEN; потеря плеча p 9-й хромосомы или делеция локуса CDKN2A/B, предполагаемых генов-супрессоров опухолевого роста; полная или частичная дупликация 7-й хромосомы, включая локус EGFR.
Также было найдено множество генов, специфические мутации в которых могут способствовать появлению глиобластомы, в том числе 28 белок-кодирующих генов, 13 генов некодирующих РНК и участок промотора теломеразной обратной транскриптазы (TERT).
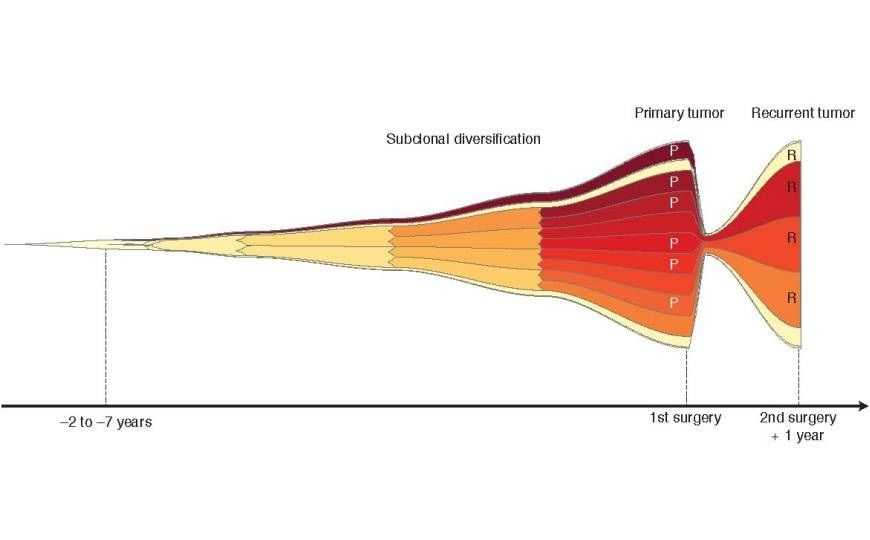
По подсчетам исследователей, глиобластомы могли начать развиваться за годы до постановки диагноза. Это странно, поскольку глиобластомы растут чрезвычайно быстро. «Мы можем объяснить это тем, что вначале многие раковые клетки умирают, и только в определенный момент начинается быстрый рост», — говорит Верена Кёрбер, первый автор статьи.
Для рецидивов глиобластомы не было обнаружено мутаций, общих хотя бы для трех пациентов. Однако отмечено повышенное количество мутаций в генах, инициирующих первичную глиобластому. К примеру, во многих образцах рецидивной формы встречались мутации гена MSH6, отвечающего за репарацию ошибочно спаренных нуклеотидов, и XIST. Также часты повторные мутации в генах PTEN, CDKN2A/B, EGFR, TERT и генах некодирующих РНК.
Исходя из предположения, что опухолевые клетки моноклональны, а появление субклонов может быть объяснено единичным эволюционным событием, авторы построили филогенетическое дерево, отображающее генетические изменения в течение развития опухоли.
В итоге установлено, что рекуррентная форма глиобластомы, в отличие от первичной, может развиваться множеством различных путей, и нет общего паттерна появления мутаций, приводящего к рецидиву. Вопреки первоначальной гипотезе, «это говорит о том, что современная стандартная терапия не оказывает какого-либо заметного селективного давления на раковые клетки и, следовательно, не способствует развитию резистентных субклонов. Это показывает, что нам всерьез необходимы новые формы лечения для глиобластом», — говорит ведущий автор исследования Петер Лихтер.
Источники
Körber V. et al. // Evolutionary Trajectories of IDHWT Glioblastomas Reveal a Common Path of Early Tumorigenesis Instigated Years ahead of Initial Diagnosis // Cancer Cell, 2019, DOI: 10.1016/j.ccell.2019.02.007


 Меню
Меню





 Все темы
Все темы




 0
0











