Ионная жидкость против рака печени
Ученые разработали новый метод местного воздействия на опухоль печени: чрескожная инъекция ионной жидкости LATTE вызывает некроз опухоли, не затрагивая здоровые ткани. LATTE можно использовать для внутриопухолевой доставки химиотерапевтических препаратов, при этом ионная жидкость усиливает действие лекарств. Эксперименты проводились на крысах, кроликах, свиньях и образцах от пациентов.
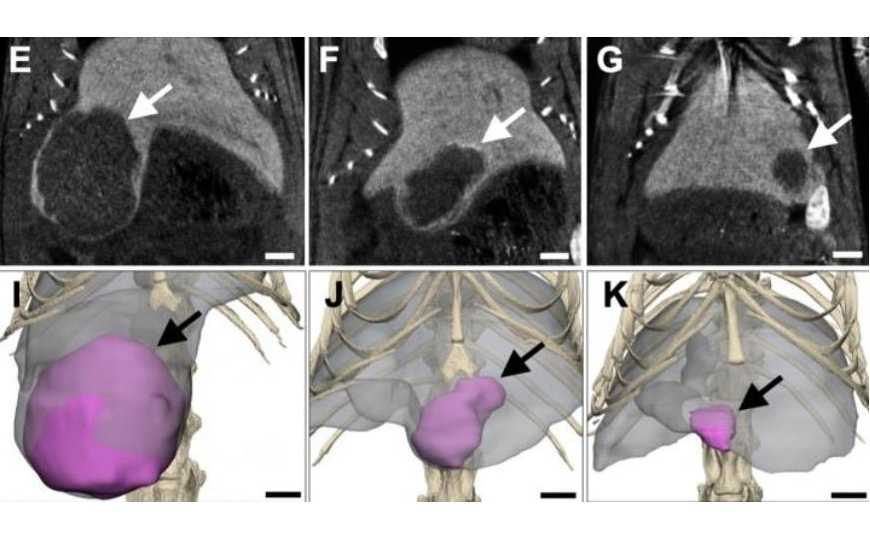
Credit: H. Albadawi et al., Science Translational Medicine (2021) | Пресс-релиз
Ученые из США разработали метод чрескожной абляции опухоли печени с помощью ионной жидкости и протестировали его на животных.
На ранней стадии гепатоцеллюлярной карциномы (HCC) из всех терапевтических опций предпочтительна пересадка печени. Однако дефицит донорских органов и связанное с этим длительное ожидание операции приводят к прогрессии заболевания. Для сдерживания прогрессии HCC применяется чрескожная локорегионарная терапия (ЧЛТ). Один из видов ЧЛТ — термическая абляция — при неудачном расположении опухоли может привести к ожогам прилегающих тканей. Жидкостная абляция, например, чрескожные инъекции этанола, более доступна и менее травматична, но также менее эффективна. После абляции этанолом велика вероятность серьезных осложнений и рецидивов.
Авторы работы, опубликованной в Science Translational Medicine, предположили, что агентом более эффективной и безопасной жидкостной абляции может быть ионная жидкость: она вызовет гибель опухолевых клеток из-за изменения осмотических условий. Разработанный ими состав получил название LATTE (Locally-active Agent for Tumor Treatment and Eradication), базовый компонент состава — ионная жидкость холин-геранат.
Для экспериментов LATTE смешивали с флуорецентным красителем и рентгеноконтрастным агентом. Первые тесты ученые провели на здоровой печени крыс. Было показано, что LATTE хорошо распространяется в тканях, и оптимальный баланс между вязкостью препарата и эффективностью диффузии достигается при концентрации 25%. Эту концентрацию использовали для дальнейшей работы.
Ответ опухоли на LATTE проверили на иммунокомпетентных крысах, несущих HCC линии N1S1. Контрольным крысам вводили чрескожно солевой раствор без LATTE либо этанол. Через две недели инъекций объем опухоли у крыс, получивших солевой раствор или этанол, был больше, чем у группы LATTE, в 34 и 14 раз соответственно. Флуоресцентный анализ показал диффузию ионной жидкости в опухоли, а КТ подтвердила полный ответ на терапию. При этом признаков поражения нормальных тканей не наблюдалось, что говорит о безопасности LATTE. Микроскопия срезов печени крыс выявила некроз всей опухоли в группе LATTE. Опухоль была окружена капсулой, содержащей лимфоциты, макрофаги и многоядерные гигантские клетки. Иммуногистохимическое окрашиваение выявило значительно сниженное количество пролиферирующих и повышенное количество апоптотических клеток HCC в группе LATTE по сравнению с группами этанола и солевого раствора.
Затем ученые проверили, можно ли использовать ионную жидкость для доставки химиотерапии. В экспериментах на крысиной печени и культурах человеческих опухолевых клеток было показано, что доксорубицин, растворенный в LATTE, сохраняется в области абляции до 28 дней после инъекции. При этом LATTE увеличивала цитотоксичность доксорубицина в синергетической манере и способствовала проникновению препарата в клетку. Смесь LATTE с доксорубицином также успешно протестировали in vivo на кроличьей модели рака печени.
Наконец, LATTE испытали на свиньях. Ионную жидкость вводили в печень чрескожно под контролем ультразвука. Анализ показал хорошую диффузию LATTE, которая усиливается в течение 90 минут с момента инъекции. Финальные опыты со свежими образцами опухолей от пациентов подтвердили результаты, полученные на крысах, кроликах и свиньях.
Таким образом, ионная жидкость LATTE не только сдерживает прогрессию опухоли, но и усиливает действие химиотерапии. Обогащение опухолей иммунными клетками позволяет предположить, что эффективность иммунотерапии на фоне LATTE также повысится. Авторы надеются, что безопасность, низкая стоимость и простота в использовании этой ЧЛТ сделает ее привлекательной для врачей и позволит большему количеству пациентов с HCC дождаться трансплантации.
Источник
Hassan Albadawi, et al. // Percutaneous liquid ablation agent for tumor treatment and drug delivery. // Science Translational Medicine 10 Feb 2021: Vol. 13, Issue 580, eabe3889; DOI: 10.1126/scitranslmed.abe3889


 Меню
Меню





 Все темы
Все темы




 0
0