Исследование сигналинга TCR выявило маркеры эффективности терапии ингибиторами контрольных точек
Британские ученые показали, что концентрация антигена в среде и работа контрольных точек иммунного ответа могут репрограммировать активацию Т-клеточных рецепторов (TCR), направляя таким образом дифференциацию клеток иммунной системы. Анализ экспрессии генов, связанных с TCR, позволяет оценить успешность лечения онкозаболеваний ингибиторами контрольных точек.
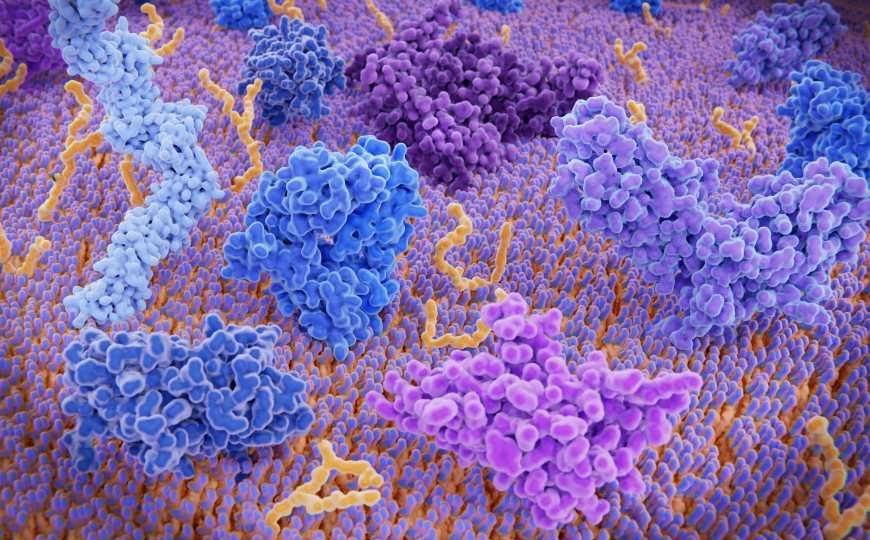
Рецепторы на поверхности Т-клетки. TCR (синий), CD-4 (голубой), CD-28 (темно-синий), PD-1 (пурпурный), CTLA-4 (фиолетовый), кальциевый канал (темно-фиолетовый).
Credit:
juangaertner | 123rf.com
Т-клеточный рецептор (TCR) играет ключевую роль в запуске иммунного ответа. При контакте со специфичным антигеном TCR запускает активацию Т-лимфоцитов — активное деление и дифференциацию клеток. Однако точные механизмы его взаимодействия с другими сигнальными путями в Т-лимфоцитах и подробности работы самого TCR до сих пор не до конца понятны. Ученые из Бирмингемского университета (Великобритания) показали, что концентрация антигена в среде и работа контрольных точек иммунного ответа способны репрограммировать работу TCR, влияя на силу сигнала от рецептора и возможность его реактивации.
Ранее ученые разработали систему для изучения активации Т-лимфоцитов — Nr4a3-таймер клеточной кинетики и активности (Nr4a3-Timer of cell kinetics and activity, Tocky). Система использует флуоресцентный белок-таймер с ограниченным временем жизни для оценки сигналинга TCR во времени — является ли сигнал новым, продолжающимся или же недавно прекратившимся. Для нового исследования ученые скрестили Nr4a3-Tocky мышей с Tg4 TCR трансгенной линией, которая распознает основной белок миелина (MBC). Этот белок использовали для стимуляции Т-лимфоцитов.
В первом опыте проверили влияние силы сигнала TCR на активацию клеток. Добавление MBC в дозах от 0,8 до 80 мкг показало, что процент активированных Т-клеток зависит от концентрации антигена. При этом динамика активированных клеток была сходной. Ученые также показали зависимость ранней экспрессии интерлейкина-10 (Il-10) от уровня сигнала TCR.
Связь TCR с экспрессией Il-10 позволила предположить, что доза антигена влияет на то, по какому пути пойдет активация лимфоцитов. Для проверки этого предположения ученые повторили обработку клеток MBC в разных дозах, отбирая из каждой группы клетки на одном и том же этапе активации и выделяя из них РНК для секвенирования. На 4-12 часах активации клетки показывали различия в экспрессии генов, зависящие от дозы антигена. Различия затронули экспрессию белков контрольных точек — то есть от дозы антигена зависит, сколько «выключателей» иммунного ответа будет на поверхности Т-клеток.
Ученые предположили, что клетки, в которых контрольные точки блокируют ответ на слабый сигнал TCR, будут более чувствительны к повторной стимуляции. Действительно, при первичной стимуляции дозой 8 мкг MBC больше клеток ответило на повторную стимуляцию дозами 8 или 80 мкг спустя 24 часа, чем при первичной стимуляции 80 мкг. Высокая доза антигена «затормозила» ответ на повторную стимуляцию.
Далее ученые повторили опыт с дополнительным введением ингибиторов контрольных точек иммунного ответа. Блокада PD-1 повышала способность клеток к ответу на повторную активацию. Секвенирование РНК также показало различие в экспрессии генов, связанных с активацией Т-лимфоцитов спустя 4 часа после стимуляции при блокаде PD-1. При этом 28 из 51 гена, экспрессия которых была повышена при блокаде PD-1, также показывали повышенную экспрессию при первоначальной обработке большими дозами антигена. Это означает, что блокада PD-1 не только повышает способности клеток к реактивации, но и усиливает сигнал TCR. Ученые также обнаружили, что экспрессия 25 из этих 28 генов повышается в клетках рака на мышиной модели при введении блокаторов PD-1.
Такие результаты позволяли предположить, что уровень экспрессии генов, связанных с работой TCR, может использоваться для оценки эффективности терапии с применением ингибиторов контрольных точек. Чтобы проверить это предположение, авторы проанализировали базу данных экспрессии генов в тканях меланомы до и после ингибирования PD-1. Сравнение профилей экспрессии, полученных в данном исследовании и при анализе тканей пациентов, выявило пять генов, активируемых ингибиторами, более высокие уровни экспрессии которых ассоциированы с лучшим ответом на терапию.
Авторы работы признают, что такой способ оценки эффективности терапии возможен лишь после ее начала и не позволяет прогнозировать ответ заранее. Однако мониторинг эффективности также полезен, поскольку дает возможность модифицировать индивидуальный план лечения.
Источник
T.A.E. Elliot et al. Antigen and checkpoint receptor engagement recalibrates T cell receptor signal strength // Immunity 54, 1–16, published September 16, 2021, DOI: 10.1016/j.immuni.2021.08.020


 Меню
Меню





 Все темы
Все темы




 0
0












