Из плюрипотентных стволовых клеток человека вырастили модель ранних этапов эмбриогенеза
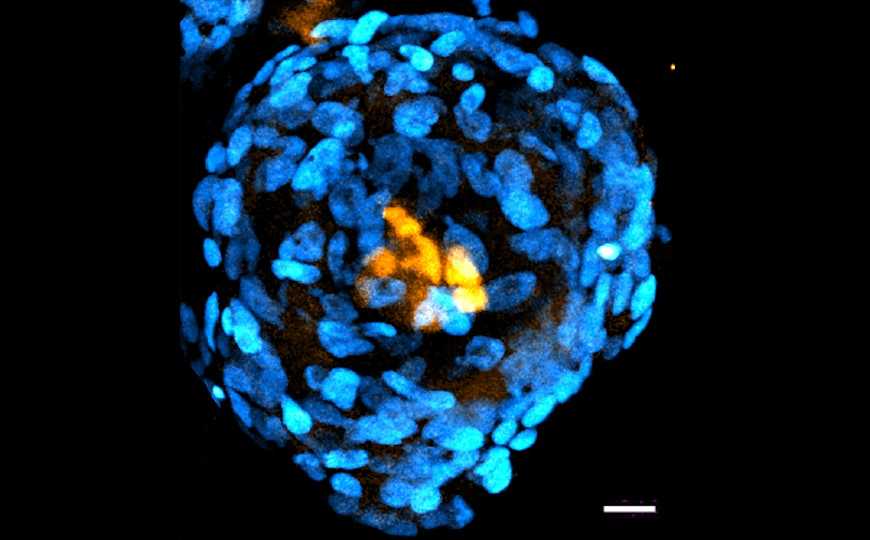
Ученые из США и Великобритании создали подобные эмбрионам структуры из плюрипотентных стволовых клеток человека с «расширенной плюрипотентностью». Эти структуры обладают многими морфологическими чертами эмбрионов с третьего по девятый-десятый день развития. Также часть их клеток экспрессирует гены, характерные для клеточных линий бластоцисты — эпибласта, гипобласта и трофэктодермы.
Патологии, которые возникают во время развития организма человека, несут за собой одни из самых тяжелых последствий для его жизни, и чем раньше образовалось нарушение, тем сильнее будет его влияние. Несмотря на важность изучения этого процесса, исследования на эмбрионах сопряжены со многими трудностями. Так, даже при наличии донорского материала ученые не вправе работать с ним дольше 14 дней.
Команда ученых из США и Великобритании разработала протокол для создания подобных эмбрионам структур (ПЭС) из плюрипотентных стволовых клеток человека (hPSC). Эти ПЭС обладают некоторыми чертами эмбрионов с третьего по девятый-десятый день развития, а также экспрессируют многие характерные для этой стадии гены. Ранее ученые не раз выращивали другие модели эмбрионов. Так, в прошлом году была опубликована работа по созданию из эмбриональных стволовых клеток человека гаструлоида, имитирующего 21-дневную стадию развития эмбриона (подробнее — на PCR.NEWS).
Не так давно ученые научились получать линии клеток с «расширенной плюрипотентностью» (extended/expanded pluripotency, EP). Такие клетки (hEPSC) способны стать как эмбриональными, так и внезародышевыми клетками.
Авторы разработали протокол, который позволяет сформировать ПЭС из hEPSC. Для этого они использовали данные, полученные в предыдущей работе на мышах. hEPSC культивировали в смеси сред и в условиях гипоксии, что способствует образованию полостных структур. Ученые проверили множество факторов роста, цитокинов и молекул, чтобы подобрать как можно более эффективные условия культивирования. В результате они выбрали BMP4, агонист WNT (CHIR99021) и ингибитор ROCK (Y-27632). Эти факторы повышают выживаемость и способствуют образованию агрегатов из клеток. Также FGF2 и ингибитор киназы ALK5 (A83-01) использовали для стимуляции дифференцировки. Через 48 часов их удаляли из среды.
Через 3–4 дня после засева клеток появлялись полостные структуры. На шестой день эти структуры имели схожую с бластоцистой морфологию, а часть клеток экспрессировала характерные для бластоцисты маркеры.
Авторы анализировали динамику поляризации клеток в полостных агрегатах. Данные иммуноцитохимии показали образование внеклеточных контактов: за счет E-кадгерина в базолатеральной области и за счет F-актина и PARD6 на апикальной. Также транскрипционный фактор GATA3 сильнее экспрессировался в поляризованных клетках, обогащенных PARD6. В предыдущем исследовании ученые обнаружили, что сигнальный путь PLC/PKC участвует в контроле поляризации клеток на ранних стадиях эмбриогенеза у мыши. При добавлении в среду ингибитора PLC уменьшились как интенсивность сигнала GATA3, так и апикальная концентрация PARD6.
Также авторы отслеживали формирование различных клеточных линий бластоцисты. Они выявили индукцию экспрессии генов, характерных для трофэктодермы — PLAC8, CDX2, KRT8 и KRT18. В части клеток детектировали экспрессию факторов, характерных для гипобласта — PDGFRA и GATA6, а также эпибласта — NANOG, POU5F1 и KLF4. Авторы показали, что в ПЭС находится больше клеток, схожих с гипобластными, чем в нормальном человеческом эмбрионе. РНК-секвенирование также выявило, что основную часть клеток ПЭС нельзя отнести к уже описанным для человеческого эмбриона линиям. Подобные результаты демонстрировали ранее на других моделях бластоцист.
Ученые заключают, что hEPSC не эквивалентны тотипотентным бластомерам, они способны образовывать только часть эмбриональных линий клеток. Те не менее, они могут формировать многоклеточные структуры, которые обладают многими морфологическими чертами, характерными для эмбрионов человека. Авторы считают, что их исследование можно использовать для создания полностью функциональной эмбрионоподобной платформы in vitro.
Источник
Sozen B., et al. Reconstructing aspects of human embryogenesis with pluripotent stem cells // Nature Communications, 12, 5550 (2021), published online 21 September 2021. DOI: 10.1038/s41467-021-25853-4


 Меню
Меню





 Все темы
Все темы




 0
0











