Как украсть хвост у бактериофага?
Горизонтальный перенос генов (ГПГ) между бактериями играет важную роль в их быстрой адаптации, в том числе для патогенных штаммов. Статья в Cell посвящена одному из новых механизмов ГПГ между неродственными видами — в ней описано семейство фаговых сателлитов-«пиратов», которые способны переносить гены вирулентности и устойчивости к антибиотикам между бактериями. Пиратством авторы назвали необычный механизм передачи — эти сателлиты способны продуцировать собственные капсиды и упаковываться в них, однако эти капсиды неинфекционны. Для передачи другой бактерии им необходимо присоединить к себе хвост другой фаговой частицы, и специфичность фага — донора хвоста определяет, бактерия какого вида станет новым хозяином сателлита.
Горизонтальный перенос генов (ГПГ) между бактериями имеет решающее значение для их эволюции, адаптации к окружающей среде, распространения устойчивости к антибиотикам и появления патогенов. Некоторые мобильные генетические элементы распространяются среди неродственных видов бактерий при помощи пока не изученных механизмов. Один из таких механизмов описали авторы статьи в Cell — они изучили новое семейство фаговых сателлитов, которые участвуют в переносе генов вирулентности и антибиотикорезистентности, а также могут способствовать появлению новых патогенных штаммов.
Недавно эти ученые обнаружили разновидность фаговых сателлитов — капсидообразующие хромосомные островки, индуцируемые фагами (capsid-forming phage-inducible chromosomal islands, cf-PICI). В отличие от других сателлитов, cf-PICI продуцируют собственные капсиды и упаковывают свою ДНК, однако их капсиды бесхвостые и неинфекционные — они полагаются исключительно на хвосты фагов для переноса. Капсиды взаимодействуют с хвостами различных других фагов, образуя химерные частицы — они вводят ДНК cf-PICI в клетки бактерий. Вид бактерии-хозяина, в которую внедрится cf-PICI, зависит от захваченного фагового хвоста — авторы назвали это явление хвостовым пиратством.
Анализируя cf-PICI, исследователи обратили внимание, что один из этих элементов (EcCIGN02175, или EcCI1) встречался в пяти родах и семи видах: Escherichia coli, Klebsiella pneumoniae, Shigella flexneri, Citrobacter freundii, Citrobacter amalonaticus, Enterobacter asburiae и Enterobacter hormaechei. Сравнение состава EcCI1 выявило четыре вариабельных региона: два фланкирующих оперона, которые кодировали гены для формирования капсида cf-PICI, и вероятно, антифаговые системы; один ниже по течению от alpA, с неизвестной функцией; и один внутри упаковочного модуля, содержащий гены для хвостового коннектора и адапторных белков. Крайне похожей структурой обладал KpCI1, обнаруженный у K. pneumoniae.
Чтобы оценить, могут ли EcCI1 и KpCI1 передаваться между видами бактерий, авторы провели анализ штаммов E. coli и K. pneumoniae, несущих ген устойчивости к тетрациклину tetA в cf-PICI. В этих бактериях происходила репликация сателлитов и упаковка их ДНК в капсиды — такая способность указывает на то, что оба штамма содержат хелперный фаг, способствующий распространению сателлитов. Однако уровень межвидовой передачи был неожиданно низким.
Для дальнейшего исследования выбрали KpCI1 из-за более простой структуры. Этот островок индуцировался и упаковывался в небольшие капсиды, однако отсутствие инфекционных частиц указывало на то, что хелперный фаг не предоставлял хвоста, необходимого для их сборки. Более детальный анализ механизма подтвердил это предположение — KpCI1 индуцировался и упаковывался в частицы за счет репликации фага, и этот процесс не зависел от сборки инфекционных частиц. Хвосты, в свою очередь, требовались только для нее, чтобы обеспечить передачу KpCI1 другим бактериям. Возможно, некоторым cf-PICI требуется два хелперных фага — один для индукции, другой в качестве источника хвостов.
Затем авторы задались вопросом: что происходит с бесхвостыми частицами cf-PICI, высвобождающимися после индукции, и есть ли у них какая-то биологическая функция? Предыдущие исследования показали, что в ходе литического цикла хвосты фагов образуются в избытке. Авторы предположили, что со свободными хвостами фагов, инфицирующих разные виды, могут связываться капсиды cf-PICI. Они подтвердили это в опытах с лизатами бактерий, инфицированных фагом HK022, а также убедились, что cf-PICI не конкурируют за хвосты интактных фагов и не удаляют их. Они используют именно избыток свободных хвостов, присутствующих в лизате, и формируют химерные частицы.
Исследователи подтвердили возможность межвидового переноса cf-PICI в более реалистичных условиях. Они совместно культивировали три штамма: K. pneumoniae JP24853, несущий хелперный фаг и KpCI1; E. coli JP24850 с лизогенным фагом HK022, который служит донором хвостов для KpCI1; и E. coli JP24888, несущего нетрансмиссивную плазмиду pBAD18-kmR. Гипотеза заключалась в том, что K. pneumoniae будет спонтанно высвобождать бесхвостые капсиды KpCI1, которые затем присоединят хвосты HK022 и проникнут в клетки штамма-реципиента JP24888. Их интеграцию в геном авторы подтвердили методом ПЦР, причем все 16 протестированных колоний дали положительный результат.
Чтобы подтвердить биологическую значимость cf-PICI для кишечных бактерий, ученые использовали в качестве реципиента вид, часто встречающийся в кишечнике человека — Enterobacter hormaechei (штамм Ehh_18). Его геном содержит пять профагов, которые могут стать донорами хвостов, и резидентный cf-PICI, который авторы удалили перед началом эксперимента. Оказалось, что EcCI1, индуцированный в клетках E. coli, успешно переносился в геном Ehh_18.
Анализируя распространенность этого явления в природе, авторы идентифицировали еще 79 элементов cf-PICI в различных виромах. Являются ли частицы этих cf-PICI бесхвостыми или химерными, еще предстоит выяснить. Кроме того, ученые подробно охарактеризовали структуру и геометрию бесхвостого капсида, формируемого cf-PICI, и описали взаимодействия отдельных субъединиц в процессе сборки.
Полученные результаты показывают, что cf-PICI могут переноситься как внутри вида, так и между видами при наличии совместимых фаговых хвостов. Они подчеркивают потенциал бесхвостых cf-PICI как природного механизма, который обеспечивает горизонтальный перенос генов между различными видами бактерий-хозяев.
Фаги могут влиять на чувствительность бактерий к антибиотику
Описан новый механизм горизонтального переноса генов бактериофагами
Источник
He, Lingchen et al. Chimeric infective particles expand species boundaries in phage-inducible chromosomal island mobilization. // Cell (2025). DOI: 10.1016/j.cell.2025.08.019


 Меню
Меню





 Все темы
Все темы
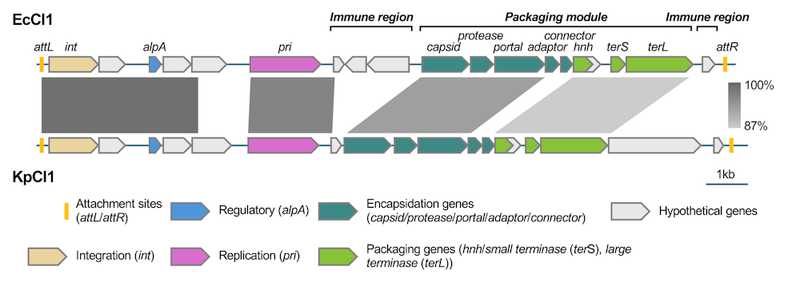 Структура элементов EcCI1 и KpCI1.
Структура элементов EcCI1 и KpCI1.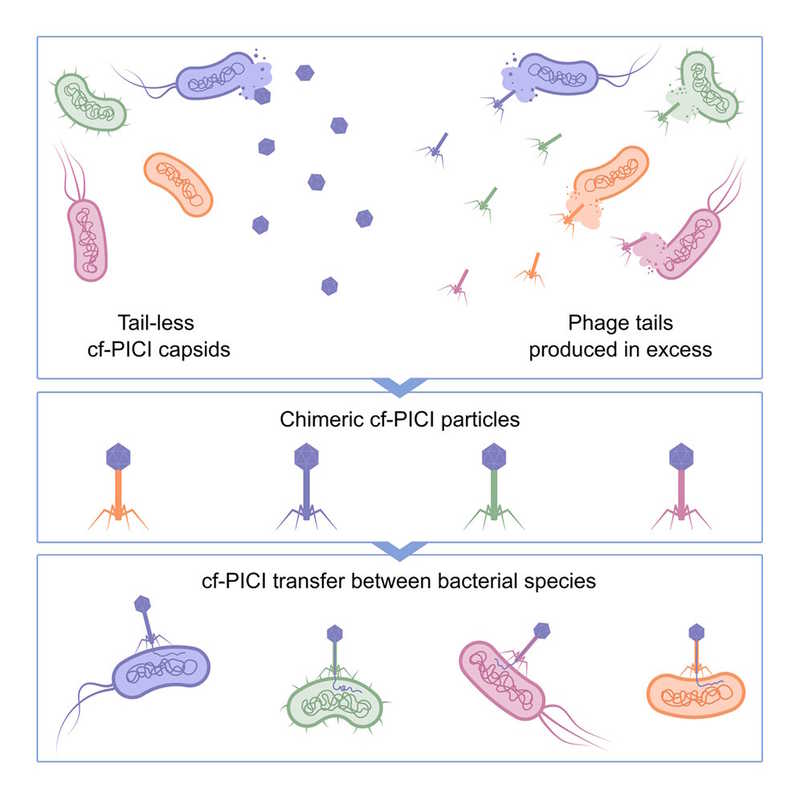 Credit:
Credit:



 0
0