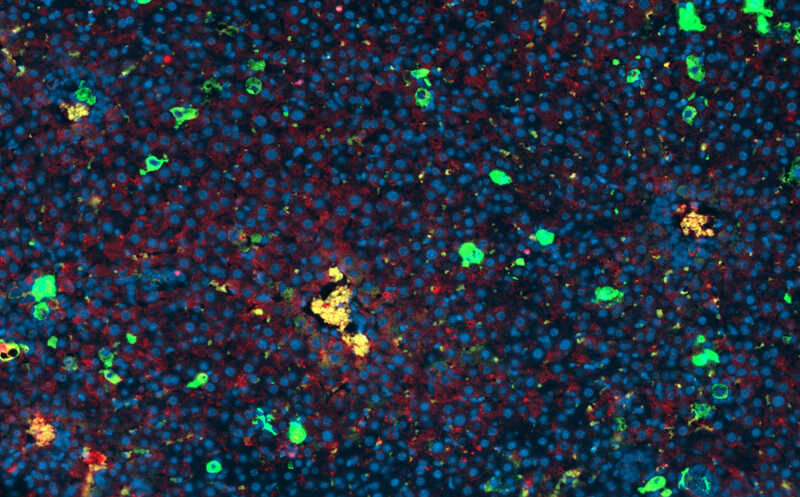
Какие иммунные клетки спасают голодную мышь от инфекций?
Недостаток пищи и инфекции неизменно сопровождали животных на протяжении всей эволюции, зачастую совпадая по времени. Однако как голодающий организм справляется с инфекцией, если работа иммунной системы требует затрат глюкозы? Авторы статьи в Immunity выявили механизм адаптации. Они показали на мышах, что глюкокортикоиды — гормоны стресса — вырабатываются в ответ на нехватку калорий и способствуют перестройке иммунной системы. Они ограничивают активацию эффекторных Т-клеток, функции которых требуют много глюкозы, и вместо этого стимулируют размножение нейтрофилов, способных получать энергию за счет гликолиза. Такой «экономный» режим позволяет организму бороться с инфекцией и избегать гипогликемии при недостатке питания.
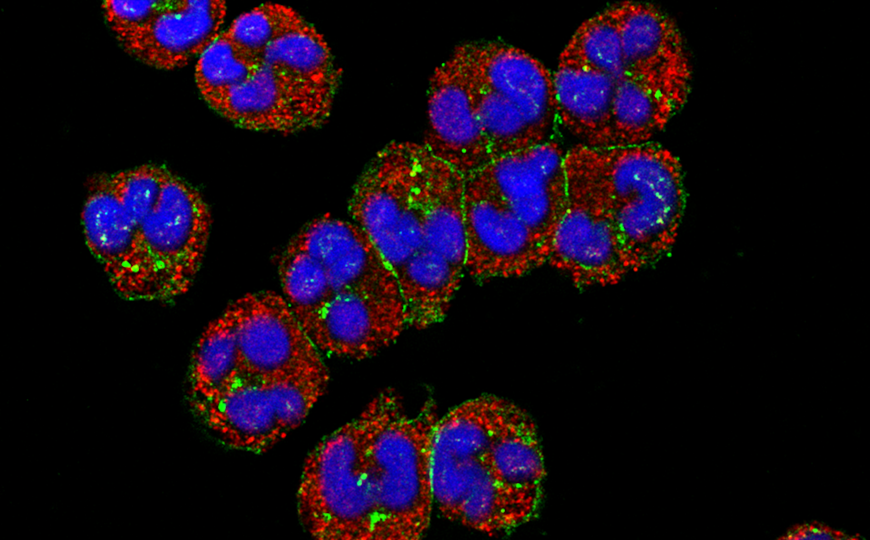
Конфокальная микроскопия нейтрофилов человека.
Credit:
Thai Tran, National Institute of Arthritis and Musculoskeletal and Skin Diseases |
пресс-релиз
Нехватка пищи и инфекции — две постоянных угрозы на протяжении всей эволюции млекопитающих, которые нередко встречались одновременно. Однако работа иммунной системы требует затрат глюкозы, и долгое время не было ясно, как организм одновременно поддерживает иммунный ответ и избегает гипогликемии при нехватке пищи. Ученые из США и Бразилии выяснили, что ключевую роль играют глюкокортикоиды. Их выработка повышалась у мышей при ограничении питания, и это изменение гормонального статуса «перенастраивало» иммунную систему на более экономный, но эффективный режим при бактериальной инфекции.
Сначала авторы работы изучили гомеостаз наивных Т-клеток в условиях нехватки пищи. Мышам сократили дневной рацион до половины от нормы, что привело к снижению веса в общей сложности на 20% за время эксперимента. При дефиците пищи количество наивных CD8+ T-клеток во вторичных лимфоидных органах сокращалось, а в костном мозге, наоборот, возрастало. Ученые показали, что это было связано именно с миграцией T-клеток, опосредованной CXCR4, а не с их размножением в костном мозге.
Ранее эта же группа ученых показала, что ограничение калорий повышает уровень глюкокортикоидов в крови, и что эти гормоны поддерживают гомеостаз глюкозы в крови голодающего животного. Теперь исследователи установили, что у мышей, получающим достаточно пищи, введение глюкокортикоидов повышало экспрессию CXCR4 на наивных CD8+ Т-клетках и стимулировало их миграцию в костный мозг.
Секвенирование РНК (RNA-seq) наивных CD8+ Т-клеток из костного мозга мышей, которых ограничили в питании, выявило обогащение путей, связанных с реакцией на глюкокортикоиды, циркадным ритмом и липидным обменом. Кроме того, повышалась экспрессия антиапоптотического гена Bcl2.
Затем авторы оценили влияние голодания и связанного с ним повышения уровня глюкокортикоидов на защиту организма от инфекций. Известно, что иммунный ответ на инфекцию требует большого количества глюкозы. Ее уровень в крови мышей закономерно снижался при недостатке питания, но поддерживался на стабильно невысоком уровне.
В качестве модели инфекции ученые заразили мышей Yersinia pseudotuberculosis. Эта бактерия — хорошо изученный модельный патоген, она может заражать человека через пищу, вызывая лихорадку, диарею и брыжеечный лимфаденит. Несмотря на голодание, защита организма сохранялась — при ограничении калорий у мышей была такая же выживаемость и бактериальная нагрузка на восьмой (пиковый) день инфекции, что и в контрольной группе, питание которой не ограничивали.
Ученые задались вопросом, какие популяции иммунных клеток отвечают за защиту от инфекций при дефиците калорий и как при этом стабилизируется уровень глюкозы в крови. Они показали, что при одновременной инфекции и недостатке пищи у мышей формировалось меньше эффекторных CD8+ Т-клеток. Это указывает на наличие компенсаторного механизма, связанного, по-видимому, с другими клетками иммунной системы.
Иммунное профилирования крови и селезенки показало, что иммунная реакция на инфекцию может быть связана с нейтрофилами, количество которых возрастало. Дальнейшие опыты подтвердили роль глюкокортикоидов в регуляции такого «переключения» иммунной системы. Авторы выяснили, что глюкокортикоиды ограничивают ответ эффекторных Т-клеток, которым, как уже показано, требуется много глюкозы. В отличие от них, нейтрофилы способны получать энергию за счет гликолиза, что снижает расход глюкозы. Также данные секвенирования РНК показали, что при голодании в нейтрофилах снижается активность механизмов, поддерживающих клеточный гомеостаз глюкозы, и усиливается аутофагия.
Кроме того, ученые установили, что глюкокортикоиды предотвращают именно дифференцировку наивных Т-клеток в короткоживущие эффекторные клетки, но способствуют формированию предшественников эффекторных клеток памяти (memory-precursor effector cells). Это усиливает защиту на случай потенциального повторного заражения.
Таким образом, в работе описана стратегия адаптации, которая поддерживает иммунный гомеостаз и обеспечивает баланс между защитой от патогенов и поддержанием уровня глюкозы при нехватке пищи, и ключевую роль в регуляции этого баланса играют глюкокортикоиды.
Источник
Luisa Menezes-Silva, et al. Hormonal rewiring of immunity during dietary restriction ensures host defense and systemic glucose conservation. // Immunity, Published online February 10, 2026. DOI: 10.1016/j.immuni.2026.01.003


 Меню
Меню





 Все темы
Все темы




 0
0