Киназа TAK1 защищает раковые клетки от цитокинов
Несмотря на перспективность иммунотерапии рака, некоторые опухоли проявляют устойчивость к ней. Ученые из Австралии и Ирландии обнаружили механизм, который защищает раковые клетки от гибели под действием цитокинов. Ключевую роль в нем играет киназа TAK1, которая поддерживает переключатели клеточной гибели в антиапоптотическом состоянии. Нокаут этой киназы приводил к тому, фактор некроза опухоли и интерферон γ запускали апоптоз в раковых клетках. У мышей опухоли с делецией TAK1 были уязвимы к атакам эффекторных Т-клеток и росли медленнее, а низкая экспрессия этой киназы у пациентов с меланомой оказалась предиктором лучшего ответа на иммунотерапию.
123rf.com
Иммунотерапия контрольных точекИммунотерапия контрольных точек значительно продвинула лечение многих видов рака, в частности меланомы, немелкоклеточного рака легких и почечноклеточной карциномы. Антитела, нацеленные на PD-1, его лиганд PD-L1 или CTLA-4, восстанавливают противоопухолевую функцию Т-клеток и могут вызывать стойкий клинический ответ. Однако такой метод лечения эффективен не для всех пациентов, и это указывает на необходимость дальнейшего изучения механизмов, позволяющих опухоли уклониться от иммунного ответа.
Противоопухолевый иммунитет требует не только способности CD8+ Т-клеток распознавать опухолевые антигены, но и цитотоксичности, опосредованной цитокинами, в первую очередь фактором некроза опухоли (TNF) и интерфероном γ (IFNγ). Ученые из Австралии и Ирландии исследовали киназы, обеспечивающие резистентность опухоли к цитотоксическому воздействию, и обнаружили среди них ключевую — TAK1.
Кином (совокупность киназ) анализировали путем CRISPR-скрининга. Клетки меланомы B16F10-OVA, стабильно экспрессирующие овальбумин и Cas9, трансдуцировали с использованием библиотеки гидовых РНК (гидРНК), нацеленной на все аннотированные киназы. Затем их подвергали трем раундам культивации с активированными CD8+ Т-клетками, специфичными к овальбумину. Выжившие опухолевые клетки отправляли на секвенирование, чтобы оценить, как менялась представленность разных гидРНК.
Анализ обогащения и истощения выявил четкие признаки отбора на каждом из раундов. Особенно выделялась гидРНК, нацеленная на ген TAK1 — после трех раундов наблюдалось ее значительное истощение, то есть нокаут TAK1 сделал опухолевые клетки уязвивыми к цитотоксичности. Также наблюдалось ожидаемое обогащение гидРНК, нацеленных на JAK1 и JAK2. Данные аналогичных скринингов, проведенных на других моделях рака, подтвердили этот результат.
Чтобы подтвердить роль TAK1 в резистентности к цитотоксичности, авторы провели конкурентный анализ: клетки меланомы дикого типа и с нокаутом TAK1 смешивали в равных пропорциях, а затем культивировали с CD8+ Т-клетками. Каждый из вариантов мишеней экспрессировал свою флуоресцентную метку. Через 48 часов доля нокаутных опухолевых клеток заметно снижалась, что говорит об их избирательной элиминации.
Чтобы выяснить, как TAK1 влияет на экспрессию генов в ответ на действие цитокинов, авторы секвенировали РНК клеток B16F10 (дикого типа и с нокаутом TAK1) после стимуляции TNF, IFNγ или их комбинацией. В клетках дикого типа все три варианта стимуляции вызывали существенное перепрограммирование транскрипции, наиболее сильно — при комбинированном воздействии.
Экспрессия генов, индуцированная TNF, была значительно нарушена в клетках с нокаутом TAK1 — в них были подавлены канонические мишени NF-κB. Транскриптомный ответ на IFNγ при этом не менялся. В соответствии с этим, воздействие одновременно TNF и IFNγ на клетки с нокаутом TAK1 избирательно снижало в них экспрессию генов-мишеней NF-κB, но не генов, стимулируемых IFNγ.
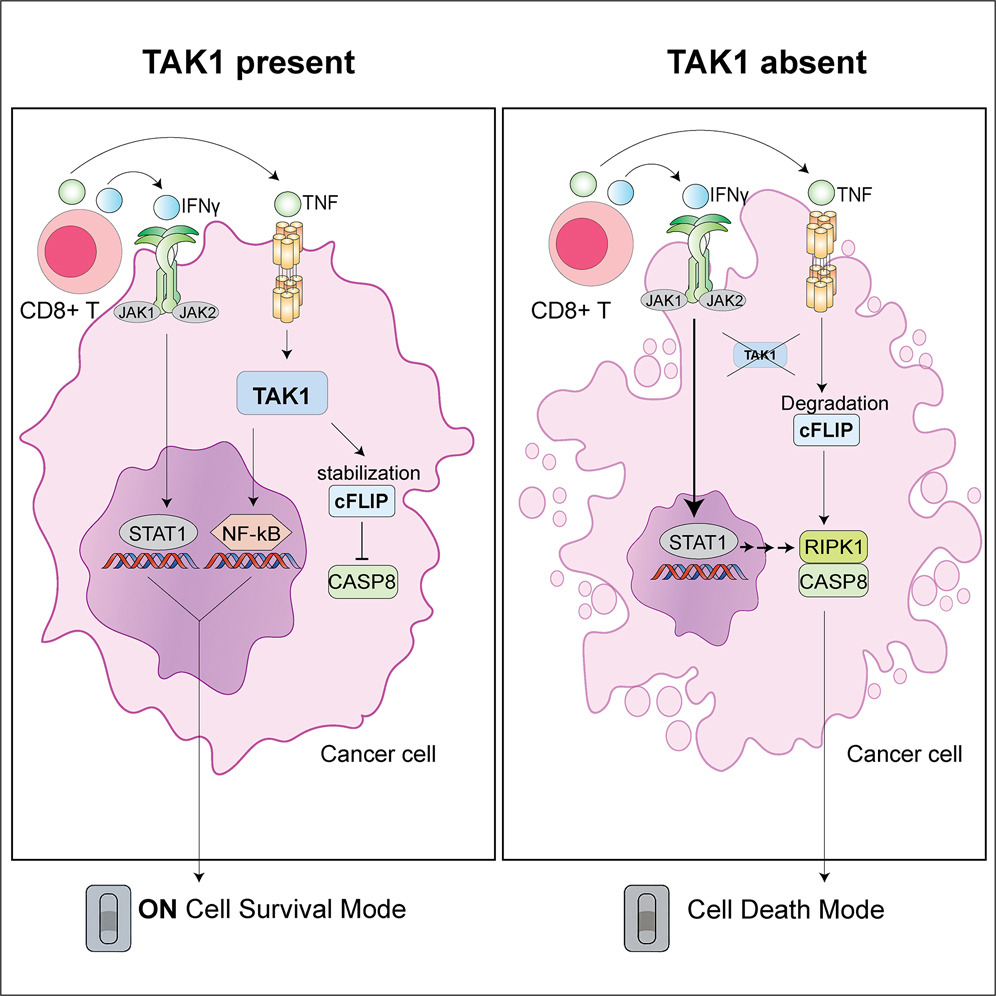
Фосфопротеомное профилирование B16F10 после обработки смесью IFNγ и TNF выявило характерные изменения в клетках с нокаутом TAK1. Одним из важных обнаружений были изменения в фосфорилировании RIPK1 — переключателе клеточной гибели, — причем в ингибиторном сайте S25 оно снижалось, а в киназном домене возрастало. Авторы делают вывод, что TAK1 поддерживает RIPK1 в состоянии, способствующем выживанию, а делеция TAK1 меняет фосфорилирование этого переключателя и тем самым стимулирует апоптоз.
Исследователи предположили, что за повышенную чувствительность к TNF и IFNγ в отсутствие TAK1 может отвечать антиапоптотический регулятор cFLIP, который контролирует активацию каспазы-8. В клетках B16F10 дикого типа после обработки IFNγ и TNF уровни этого белка оставались относительно стабильными, а при дефиците TAK1 заметно снижались. По-видимому, деградация cFLIP в этом случае способствует активации каспазы-8 и приводит к апоптозу опухолевых клеток в ответ на IFNγ и TNF.
Затем авторы изучили влияние делеции TAK1 in vivo. Они подкожно вводили иммунокомпетентным мышам клетки B16F10 дикого типа или с нокаутом этого гена. Делеция TAK1 не влияла на пролиферацию in vitro, но у мышей опухоли с его нокаутом росли значительно медленнее, а выживаемость хозяев была дольше, то есть иммунная система активнее боролась с опухолью. Роль иммунных клеток подтвердили на иммунодефицитных мышах (NSG), у которых отсутствуют функциональные лимфоциты и NK-клетки. В этом случае опухоли с нокаутом TAK1 росли так же, как контрольные опухоли дикого типа. Конкурентный анализ, в ходе которого мышам NSG подсаживали одновременно клетки меланомы с нокаутом TAK1 и без, а затем вводили CD8+ T-клетки, подтвердил избирательное уничтожение нокаутных опухолевых клеток.
Исследователи также оценили клиническую значимость экспрессии TAK1 в контексте иммунотерапии. Анализируя данные пациентов с меланомой, они показали, что TAK1 может служить прогностическим биомаркером ответа на иммунотерапию. У пациентов с более низкой экспрессией этого гена до иммунотерапии был лучший прогноз.
Таким образом, дефицит TAK1 повышает чувствительность опухолей к цитотоксичности, опосредованной Т-клетками. Это указывает на TAK1 как на потенциальную терапевтическую мишень, ингибирование которой может преодолеть резистентность раковых клеток к иммунотерапии.
Химерный белок из антитела и лектина мешает раковым клеткам уклоняться от иммунного ответа
Источник
Tirta M. Djajawi, et al. A TAK1 cytokine toxicity checkpoint controls anti-cancer immunity. // Cell Reports, Published online December 19, 2025. DOI: 10.1016/j.celrep.2025.116665


 Меню
Меню





 Все темы
Все темы
 Credit:
Credit:



 0
0









