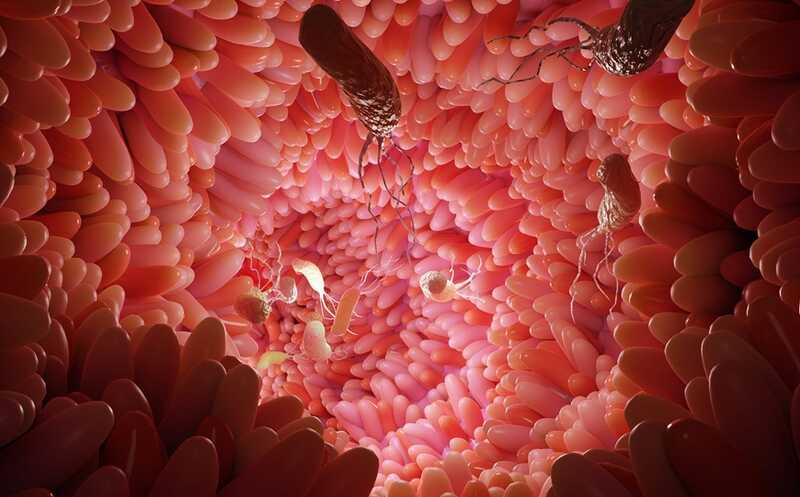
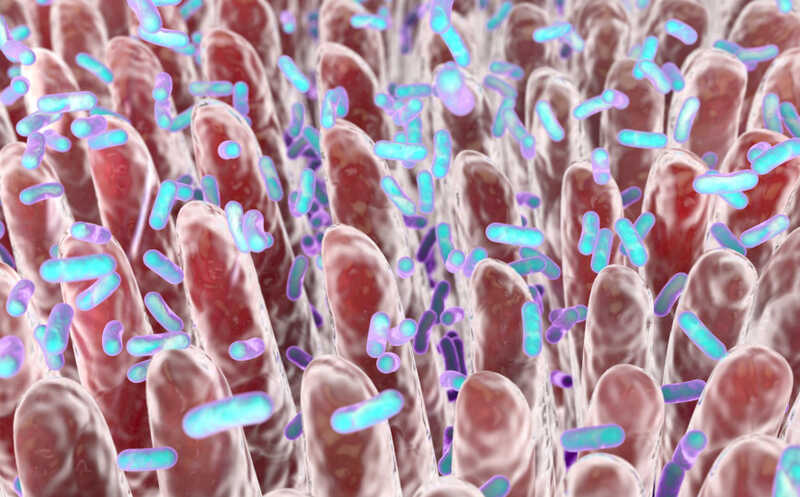
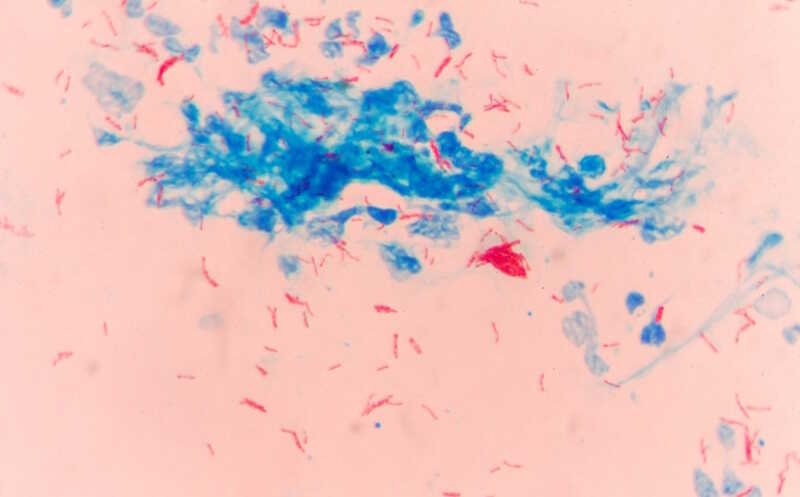
Кишечные бактерии могут накапливать в себе лекарства
Кишечные бактерии накапливают в своих клетках человеческие лекарства, не модифицируя их. На примере антидепрессанта дулоксетина ученые показали, что аккумуляция лекарств может изменять метаболизм бактерий, что приводит к сдвигу структуры всего сообщества. Кроме того, нематоды демонстрировали сниженный ответ на дулоксетин в присутствии бактерий, накапливающих препарат.
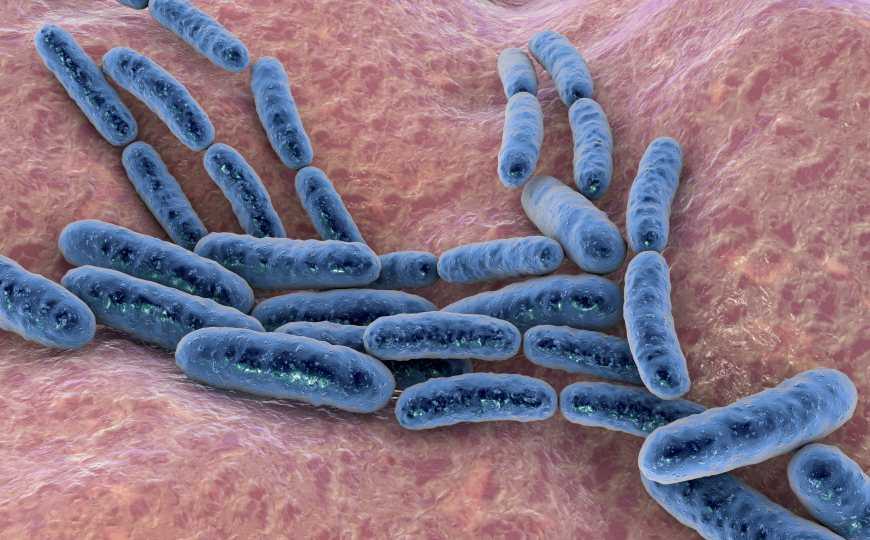
Кишечные бактерии могут существенно влиять на доступность и эффективность различных лекарств. Считается, что в большинстве случаев это влияние обусловлено химическим преобразованием лекарств бактериями — биотрансформацией. Авторы новой статьи, опубликованной в Nature, исследовали другой вид взаимодействия кишечных бактерий с лекарствами — биоаккумуляцию, то есть способность бактерий накапливать в себе ксенобиотики, не преобразуя их.
В работе использовали 15 лекарственных препаратов и 25 штаммов кишечных бактерий, относящихся к 21 видам, в том числе Bifidobacterium longum, Escherichia coli и Bacteroides uniformis. Ученые выбрали филогенетически неродственные виды с различными особенностями метаболизма, чтобы получить наиболее полную картину человеческой кишечной микробиоты. Они попарно проверили взаимодействия каждой бактерии с каждым препаратом, всего получилось 375 пар.
Клетки выращивали в специальной среде, содержащей 50 мкМ препарата — примерно в такой концентрации препараты находятся в кишечнике. Изменения концентрации отслеживали с помощью жидкостной хроматографии. В ходе скрининга были выявлены 70 случаев взаимодействия бактерии с препаратом, из которых 29 были ранее неизвестны. Семнадцать новых взаимодействий сводились к биоаккумуляции, при этом в некоторых парах накопление препарата бактерией влияло на ее рост.
Авторы изучили воздействие человеческих лекарств на физиологию кишечных бактерий на широко распространенном антидепрессанте дулоксетине и накапливающей его бактерии Clostridium saccharolyticum. Оказалось, что дулоксетин в бактериальных клетках взаимодействует с 55 белками, большая часть из которых является ферментами метаболизма. Кроме того, с помощью метода термального протеомного профилирования (thermal proteome profiling) ученые выявили бактериальные белки, которые претерпевают структурные изменения под действием дулоксетина. Ученые установили, что накопление дулоксетина в клетках C. saccharolyticum воздействует на метаболизм аминокислот, биосинтез пуринов и пиримидинов, а также пентозофосфатный путь.
Чтобы оценить, как дулоксетин влияет на спектр метаболитов, выделяемых бактериальными клетками, ученые инкубировали в присутствии препарата четыре вида бактерий, накапливающих его, и два ненакапливающих. Для трех накапливающих штаммов (C. saccharolyticum, Lactobacillus plantarum и E. coli IAI1) и одного ненакапливающего (Lactococcus lactis) детектировались существенные изменения в экзометаболоме после инкубации.
Интересно, что накопление препаратов бактериальными клетками может сказываться и на составе бактериального сообщества. Ученые воссоздали стабильное сообщество кишечных бактерий видов Bacteroides thetaiotaomicron, Eubacterium rectale, Lactobacillus gasseri, Ruminococcus torques и Streptococcus salivarius и подвергли его действию дулоксетина. S. salivarius способен к накоплению дулоксетина, при этом препарат подавляет рост E. rectale в отсутствие других бактерий. Если же с дулоксетином выращивали все сообщество, численность E. rectale увеличивалась более чем в 100 раз. Ученые предполагают, что накопление дулоксетина бактерией S. salivarius изменяет спектр секретируемых ей метаболитов, что и приводит к взрывному росту численности E. rectale. Это означает, что человеческие лекарства могут модулировать микробные сообщества не только за счет прямого воздействием на отдельные виды, но и за счет перекрестных метаболических и пищевых путей.
Наконец, ученые проверили, как биоаккумуляция дулоксетина кишечными бактериями изменяет хозяйский ответ на препарат. В качестве модельного организма выбрали нематоду Caenorhabditis elegans. Поведенческий ответ нематоды на дулоксетин был ослаблен, если в среде присутствовала бактерия, накапливающая препарат.
Авторы планируют расширить исследование до оценки индивидуальных ответов на препараты в зависимости от состава кишечного бактериального сообщества.
Источник
Klünemann, M., Andrejev, S., Blasche, S. et al. Bioaccumulation of therapeutic drugs by human gut bacteria. // Nature , 2021, published 08 September 2021, DOI: 10.1038/s41586-021-03891-8


 Меню
Меню





 Все темы
Все темы




 0
0