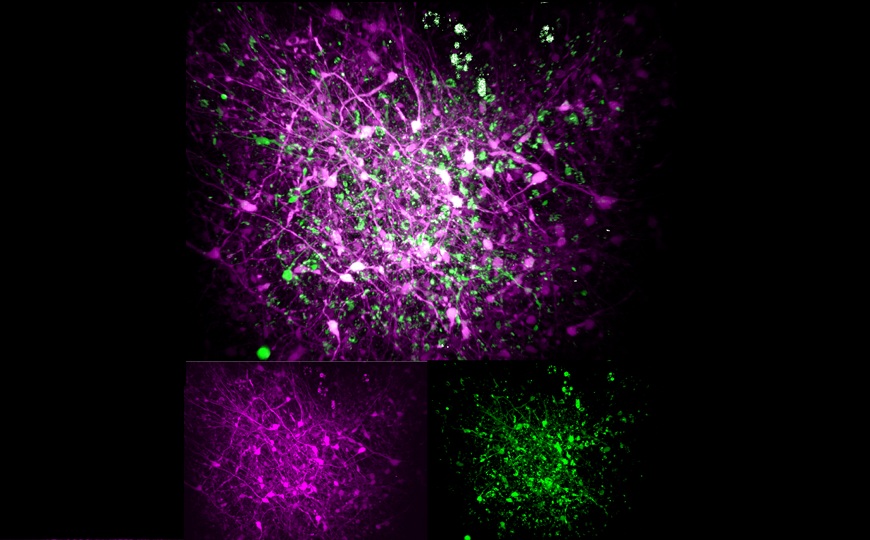
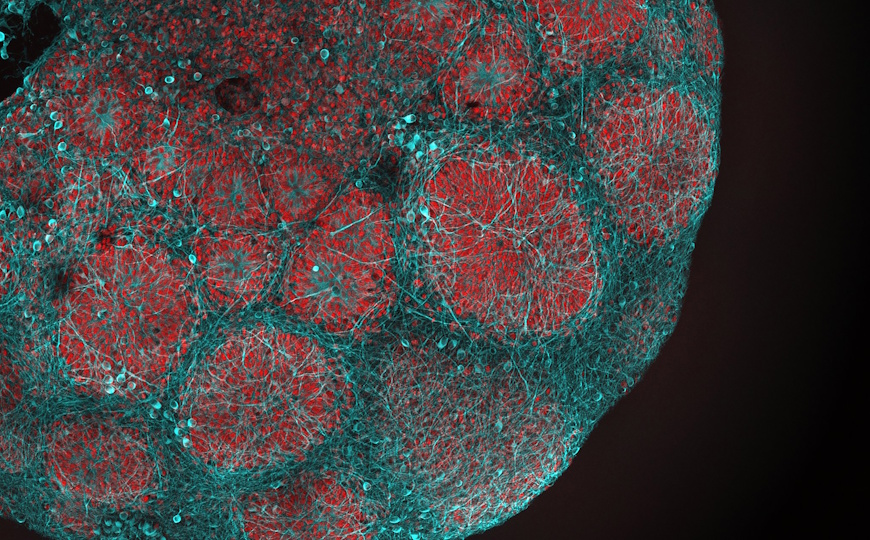
Клетки желудка человека впервые заставили секретировать инсулин
Международная группа исследователей показала на органоидах, что клетки человеческого желудка можно перепрограммировать в инсулин-секретирующие клетки, подобные β-клеткам поджелудочной железы. К клеткам желудка человека такой метод применили впервые. Полученные β-клетки оказались функциональны в организме иммунодефицитных мышей — у животных с диабетом, которым в жировую ткань подсадили органоиды с β-клетками, нормализовался уровень глюкозы в крови. Такой подход может лечь в основу клеточной терапии диабета как альтернатива поиску донорских трансплантатов и пожизненной иммуносупрессии.
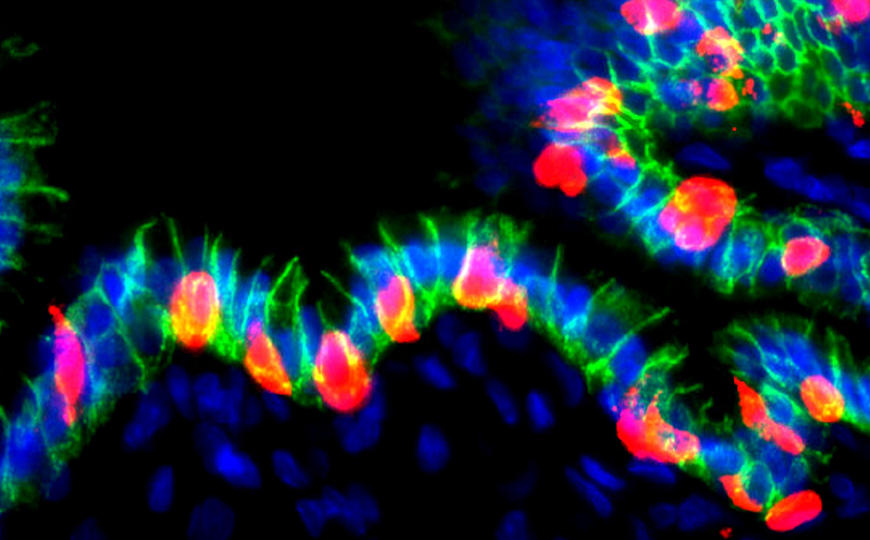
Клетки органоидов человеческого желудка, в которых индуцировали продукцию инсулина.
Credit:
Hyunkee Kim |
пресс-релиз
Получение функциональных β-клеток, вырабатывающих инсулин, — одна из главных задач развивающихся сегодня подходов к лечению сахарного диабета. В последние годы ученые разработали способ получать из человеческих эмбриональных стволовых клеток (hESC) и индуцированные плюрипотентные стволовые клетки (hiPSC) в органоиды, имитирующие островки поджелудочной железы. После пересадки животным эти органоиды способны выделять инсулин и регулировать уровень глюкозы. Технология в настоящее время проходит
клинические испытания, однако ее применение у людей осложняется необходимостью иммуносупрессивной терапии, повышающей риск инфекций и онкозаболеваний.
Альтернативный подход предполагает, что β-клетки не культивируются вне организма, а образуются непосредственно в слизистой оболочке желудка. Ранее эксперименты на мышах показали, что делеция гена Foxo1 в предшественниках эндокринных клеток в слизистой оболочке, а также активация
трех транскрипционных факторов — NEUROG3, PDX1 и MAFA (совместно обозначаемых как NPM) — стимулирует образование инсулин-продуцирующих аналогов β-клеток в слизистой оболочке пищеварительного тракта,
преимущественно в желудке.
Исследователи из США, Китая и Таиланда впервые воспроизвели этот процесс с использованием человеческих клеток. Они использовали органоиды человеческого желудка (hGO) — миниатюрные модели желудка с эпителиальными и мезенхимальными компонентами — полученные из hESC. Эти органоиды трансплантировали мышам, одновременно стимулируя экспрессию NPM и флуоресцентного белка Cherry с помощью тетрациклин-контролируемой системы регуляции экспрессии генов (Tet). После 30 дней дифференцировки органоиды напоминали слизистую оболочку антрального отдела желудка: они содержали муцин-продуцирующие клетки (то есть вырабатывающие слизь) и гормон-продуцирующие энтероэндокринные клетки, а также экспрессировали характерные для этого отдела желудка гены (TFF2, MUC5AC, GAST и другие).
После активации транскрипционных факторов NPM в эпителии органоидов формировались клетки, синтезирующие c-пептид — один из компонентов проинсулина. Секвенирование РНК подтвердило повышенную экспрессию генов, участвующих в развитии β-клеток и выработке инсулина. Секвенирование РНК единичных клеток также позволило выявить минорные популяции клеток, встречающихся в островках поджелудочной железы наряду с инсулин-продуцирующими β-клетками — δ-, ε- и α-клетки. Анализ траекторий развития с помощью псевдовремени показал, что под действием NPM в клетках желудочного эпителия подавлялись сигнальные пути, связанные с пищеварением и каскадом WNT, а характерные для β-клеток сигнальные пути, связанные с синтезом белков и окислительным фосфорилированием, наоборот, активировались. Функциональные тесты подтвердили способность новообразованных β-клеток выделять инсулин в ответ на повышение уровня глюкозы.
Чтобы проверить, как такие органоиды поведут себя в организме, их трансплантировали иммунодефицитным мышам. Трансплантаты сохранялись в течение 6 месяцев и проявляли признаки дальнейшего созревания. В них также появлялись клетки, экспрессировавшие одновременно гормоны гастрин, грелин и соматостатин, которые характерны для антрального отдела желудка. При этом органоиды не разрастались в организме мышей-реципиентов.
Ключевым этапом эксперимента стала проверка способности органоидов контролировать уровень глюкозы в крови в мышиной модели сахарного диабета. Введение доксициклина таким мышам после трансплантации органоидов индуцировало в них развитие β-клеток. Это обеспечило нормализацию уровня глюкозы на протяжении всех шести недель эксперимента. В то же время мышей с диабетом, органоиды которых не стимулировали доксициклином, развивалась гипергликемия. Более того, клетки в трансплантированных органоидах реагировали на колебания уровня глюкозы так же, как нормальные β-клетки, что подтвердило их функциональную зрелость.
Хотя на сегодняшний день методика далека от клинического применения, эта работа доказывает принципиальную возможность превращения тканей человеческого желудка в источник инсулина, что может лечь в основу клеточной терапии сахарного диабета.
Дальнейшие направления, предлагаемые авторами, включают поиск способов доставки NPM в слизистую оболочку антрального отдела желудка человека, изучение слизистой оболочки тела желудка в качестве другого потенциального источника инсулина и проведение экспериментов с другими линиями hESC. Также исследователи предполагают уточнить, могут ли инсулинпродуцирующие клетки органоидов формировать организованные устойчивые структуры по типу островков поджелудочной железы.
Источник
Lu, J., et al. Modeling in vivo induction of gastric insulin-secreting cells using transplanted human stomach organoids. // Stem Cell Reports (2025). DOI: 10.1016/j.stemcr.2025.102708


 Меню
Меню





 Все темы
Все темы



 0
0