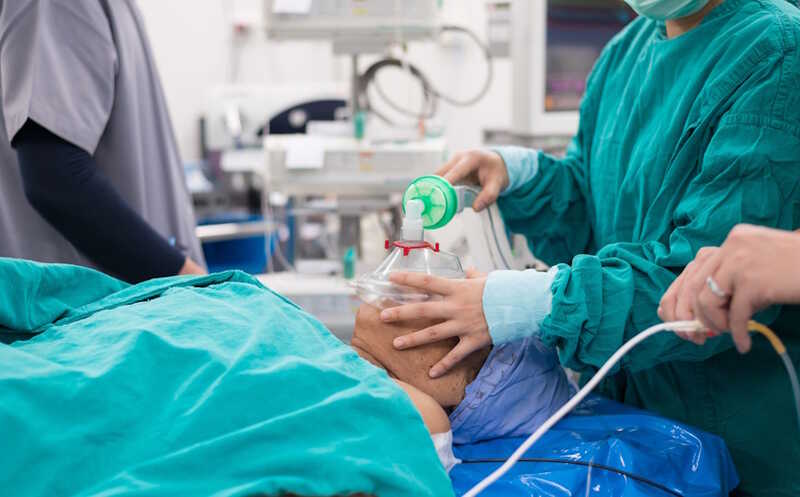
Митохондриальную ДНК с мутациями можно избирательно удалить
Японские ученые разработали агенты, которые алкилируют мутантный аденин в специфических последовательностях ДНК. Впоследствии такая поврежденная ДНК элиминируется клетками. Они также создали систему для доставки этого агента в митохондрии. Авторы работы рассматривают эту систему как основу для терапии митохондриальных наследственных болезней.
На данный момент известно около 800 точечных мутаций, которые могут присутствовать в митохондриальной ДНК (мтДНК) человека. Часто они приводят к развитию тяжелых патологий, таких как наследственная оптическая нейропатия Лебера, приводящая к потере остроты зрения, или синдром MELAS (mitochondrial encephalopathy, lactic acidosis, and stroke-like episodes). . Редактирование мтДНК затруднено ее недоступностью для типичных молекулярных инструментов. Авторы работы, опубликованной в Cell Chemical Biology, создали систему специфического алкилирования аденина в определенных последовательностях ДНК. Подвергнутая такому алкилированию ДНК быстро элиминируется клетками.
Основу системы составляет пирролимидазольный агент, который обладает способностью связывать ДНК, а его специфичность по отношению к распознаваемым последовательностям можно менять, изменяя расположение пиррольных и имидазольных групп. К пирролимидазольному агенту пришит специальный пептид, благодаря которому он может попадать в митохондрии (mitochondria penetrating peptide, MMP). Третий элемент системы, связанный с пирролимидазольным агентом и MМP — хлорамбуцил, вещество, алкилирующее аденин в составе ДНК. Благодаря алкилирующему действию хлорамбуцил используется как противораковый препарат. Пирролимидазольный агент обеспечивает специфичность алкилирования, поскольку распознает последовательность рядом с аденином-мишенью.
Авторы опробовали разработанную трехкомпонентную систему на культуре клеток HeLa S3, а мишенью для алкилирования была выбрана непатогенная мутация m.8950G>A. Для митохондрий этой клеточной линии характерна гетероплазмия по данной мутации: геномы некоторых митохондрий содержат ее, геномы других — неизмененную последовательность. Гетероплазмия митохондрий распространена также in vivo. Если с помощью этого метода удалить митохондрии с патогенной мутацией, оставив только «здоровые», возможно, состояние организма вернется к норме.
Ученые продемонстрировали, что алкилирование действительно специфично по отношению к последовательности. Попутно они создали агент, алкилирующий аденин в позиции 9037, тем самым подтвердив, что созданная ими система может быть запрограммирована на модификацию различных сайтов в митохондриальной ДНК.
Чтобы оценить воздействие алкилирующей системы на живые клетки, ученые оценили уровень гетероплазмии в клетках HeLa, подвергнутых действию системы, с помощью количественной ПЦР. Наблюдения за уровнем гетероплазмии митохондриальной ДНК на 10-й и 20-й день показали, что постепенно количество митохондрий, несущих ДНК с мутацией m.8950G>A, снижался, то есть клетки элиминировали мтДНК, содержащую алкилированный конъюгат.
Авторы разработки предположили, что в будущем эта система может быть использована для терапии митохондриальных заболеваний — с ее помощью можно очищать клетки от мтДНК, несущей патогенные мутации.
Источник
Takuya Hidaka et al. Targeted elimination of mutated mitochondrial DNA by a multi-functional conjugate capable of sequence-specific adenine alkylation // Cell Chemical Biology, Published August 26, 2021, DOI: 10.1016/j.chembiol.2021.08.003.


 Меню
Меню





 Все темы
Все темы




 0
0