Модель «пациента на чипе» может быть создана из собственных клеток больного
Исследователи из США создали орган на чипе; образцы тканей сердца, кости, печени и кожи окружены эндотелием и соединены сосудами, в которых циркулируют иммунные клетки и сигнальные вещества. Чип размером с предметное стекло можно заселить тканями, полученными из индуцированных плюрипотентных клеток конкретного человека. Это позволит персонализировать терапию, подбирая наиболее эффективные в каждом случае лекарства.
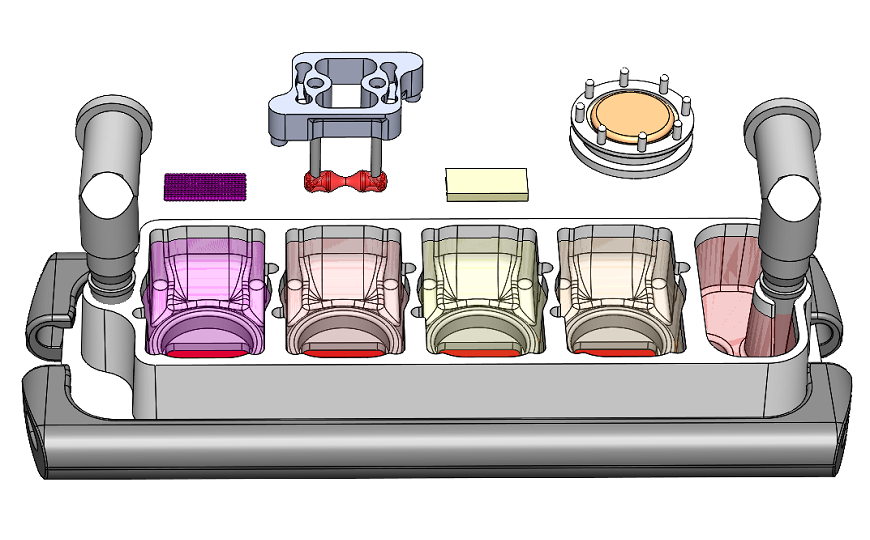
Схема органов на чипе: культуры тканей, представляющие печень, сердце, кости и кожу, соединены сосудистым кровотоком. Эти ткани могут быть созданы из иПСК пациента.
Credit:
Keith Yeager/Columbia Engineering
Орган на чипе — устройство для выращивания культур клеток человека, которое имитирует работу отдельных органов или систем органов. Такие устройства используют для моделирования заболеваний, изучения эффективности и безопасности лекарств. Они дешевы и дают качественно иную информацию, чем исследования на лабораторных животных.
Чтобы моделировать функции организма, системные заболевания, метаболизм лекарства, клетки различных тканей должны взаимодействовать, так же, как в организме. Поэтому орган на чипе обычно состоит из микроконтейнеров с клетками, соединенных микроканалами. Кроме того, желательно, чтобы ткани сохраняли жизнеспособность достаточно долго — недели, лучше месяцы.
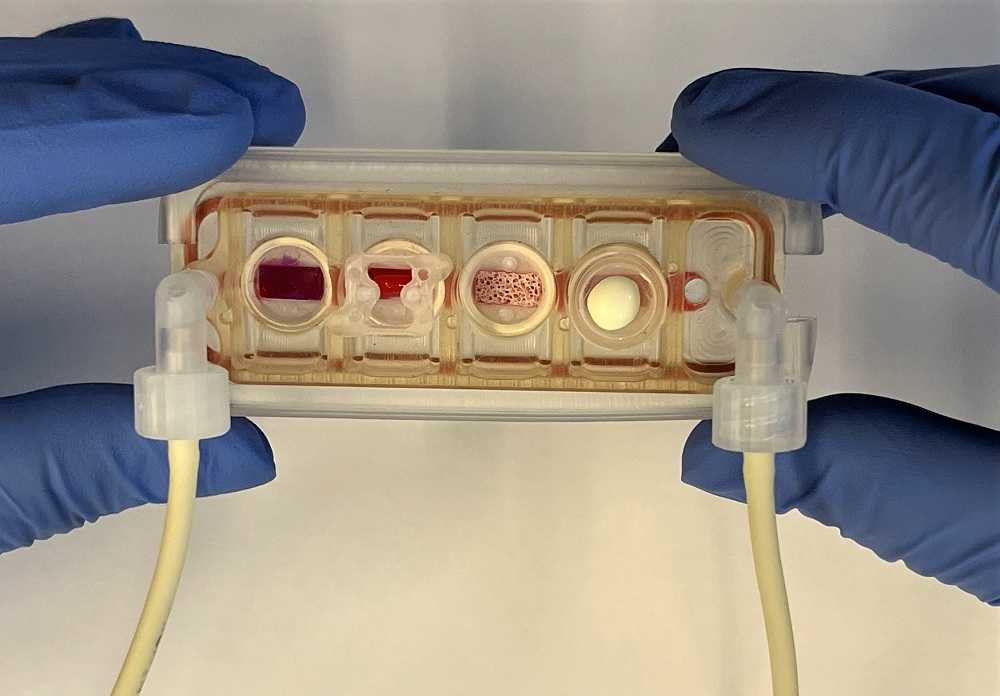
На этой неделе исследователи из Колумбийского университета (Нью-Йорк) в месте с коллегами из Гарвардского университета, других научных центров и компаний опубликовали в Nature Biomedical Engineering статью о создании мультиорганного чипа, ткани которого сохраняли свои молекулярные, структурные и функциональные фенотипы в течение 4 недель. На пластинке из биосовместимого полимера расположены образцы тканей сердца, кости, печени и кожи, соединенные сосудами, в которых циркулируют иммунные клетки, а также цитокины и внеклеточные везикулы.
«Обеспечение связи между тканями при сохранении их индивидуальных фенотипов было серьезной задачей, — говорит первый автор работы Кейси Рональдсон-Бушар, ведущий автор исследования. — Поскольку мы сфокусировались на использовании моделей тканей, полученных от пациентов, мы должны были индивидуально провести созревание каждой ткани, чтобы она при функционировании имитировала реакции, которые вы могли бы увидеть у пациента (…) В организме каждый орган поддерживает свою среду, при этом взаимодействуя с другими органами через сосуды, которые несут циркулирующие клетки и биологически активные факторы. Поэтому мы решили соединить ткани сосудами, сохраняя при этом индивидуальные ниши каждой ткани».
Контейнеры с образцами тканей, каждый в своей оптимизированной среде, отделяет от сосудистого русла барьер с избирательной проницаемостью, выращенный из клеток эндотелия. Этот барьер повышает правдоподобие модели: ткани, окруженные эндотелием, более сходны с настоящими органами. Разработчики поместили в сосуды моноциты, дающие начало макрофагам — клеткам иммунной системы, которые играют важную роль в управлении тканевыми реакциями на травмы, заболевания и терапию.
Все ткани вырастили из одной и той же линии индуцированных плюрипотентных стволовых клеток человека (иПСК), полученных из небольшого образца крови. Это доказывает, что возможно создать такие чипы для конкретных людей — фактически получить «пациента на чипе».
Ткани, представленные на чипе, особенно подвержены неблагоприятному влиянию противораковых препаратов. Авторы исследовали влияние доксорубицина — широко используемого противоракового препарата — на сердце, печень, кости, кожу и сосуды: наблюдаемые эффекты, в том числе фармакокинетика и фармакодинамика, повторили те, о которых сообщалось в клинических исследованиях. Параллельно они разработали новую вычислительную модель всасывания, распределения, метаболизма и секреции лекарств. Модель правильно предсказала особенности метаболического превращения доксорубицина в доксорубицинол и его диффузию в чипе.
Авторы также определили некоторые микроРНК, которые могут служить ранними биомаркерами кардиотоксичности доксирубицина и вызванной им кардиомиопатии: их появление указывает на необходимость снижения дозы или прекращения терапии.
Среди ограничений предложенного подхода исследователи называют отсутствие на чипе образцов других важных для метаболизма органов: кишечника, почек, жира. Также не исключено, что полимер могут абсорбировать лекарство и снижать его концентрацию; для предотвращения этого, возможно, придется модифицировать поверхность полимера.
Источник
Ronaldson-Bouchard, K., et al. A multi-organ chip with matured tissue niches linked by vascular flow // Nature Biomedical Engineering 6, 351–371. 2022. DOI: 10.1038/s41551-022-00882-6


 Меню
Меню





 Все темы
Все темы




 0
0