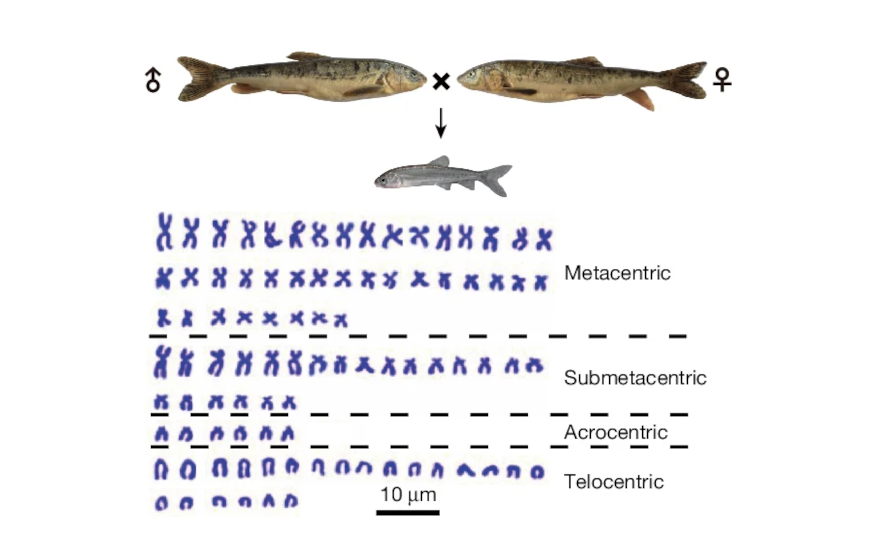
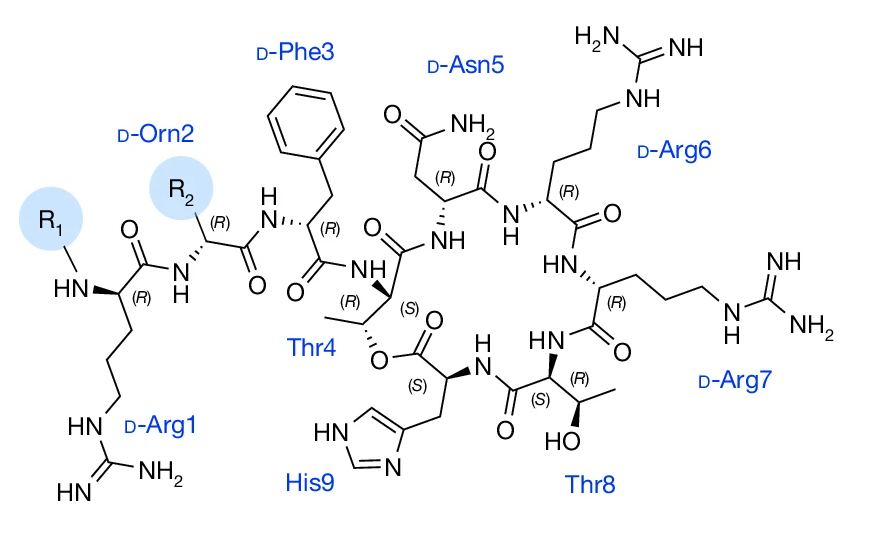
На мутации в геноме возбудителя туберкулеза влияет организм человека
Секвенирование геномов Mycobacterium tuberculosis показало, что генетическое разнообразие бактерий в организмах одних людей больше, чем в других. Более того, разные линии патогена в одном и том же хозяине накапливают мутации с различной скоростью.
Bigstockphoto.com
Борьба с эпидемией туберкулеза в мире осложняется появлением устойчивых к антибиотикам штаммов. Предполагаемая частота мутаций в геноме Mycobacterium tuberculosis (Mtb)— около 0,5 на 10000 копирований геномов, что немного по сравнению с большинством других бактерий. Однако высокая частота приобретенной резистентности среди клинических штаммов заставляют задуматься, не может ли частота мутаций возрастать в организме одного пациента.
Когда у пациента развивается активный туберкулез, в его организме присутствуют от 1010 до 1012 бацилл, и такая большая популяция должна содержать многочисленные мутации. С другой стороны, инфекция Mtb вызывает изменения в организме, соответственно, изменяется среда обитания микобактерий. Было высказано предположение, что эти изменения напрямую влияют на мутагенез, и следовательно, на возникновение лекарственной устойчивости.
Чтобы проверить это предположение, авторы статьи в Science Advances исследовали образцы мокроты у 18 пациентов с туберкулезом, еще не получавших лечения антибиотиками, и секвенировали 795 изолятов Mtb. Все изоляты были восприимчивыми, за исключением одного, устойчивого только к изониазиду. Для каждого пациента отобрали около 50 отдельных колоний, кроме того, для 9 пациентов выполнили глубокое полногеномное секвенирование всех колоний с чашки Петри.
Общее число мутаций de novo в бактериальных геномах, выделенных от разных пациентов, варьировало очень сильно — от 0 до 116 однонуклеотидных полиморфизмов (SNP). Накопление разнообразия могло протекать по одной из двух моделей: независимое появление отдельных SNP лишь в некоторых колониях (очевидно, это ситуация, когда небольшое количество бацилл вызывает инфекцию, достаточно быстро размножается и вызывает активное заболевание) либо ступенчатый рост в несколько стадий, когда преимущественно размножаются отдельные субпопуляции.
Интересно. что частота мутаций различалась в изолятах, полученных от одного и того же пациента. Как показало сравнение синонимичных и несинонимичных мутаций, причиной вряд ли мог быть положительный отбор. У четырех пациентов, чьи колонии продемонстрировали различную частоту мутаций, было больше общих SNP de novo, и при этом большинство SNP составляли замены C на T и G на A. Такая картина мутагенеза обычно связана с окислительным повреждением. Повышенная чувствительность этих конкретных штаммов к активным формам кислорода не подтвердилась. Видимо, имело место более сильное воздействие окислительного стресса на бактерии в организмах этих пациентов, то есть явление определялось особенностями хозяина.
Все 18 участников этого исследования были ВИЧ-негативными, но в другом исследовании, где участвовали ВИЧ-позитивные больные туберкулезом, бактерии накапливали существенно меньше мутаций. Таким образом, преобладание мутаций, ассоциированных с активными формами кислорода, может быть обусловлено давлением со стороны иммунной системы.
Эти результаты подтверждают гипотезу, согласно которой мутагенез Mtb in vivo, в том числе и появление вариантов, связанных с лекарственной устойчивостью, модулируется средой-хозяином. Важно установить, при каких именно условиях возрастает частота мутаций — в этом может быть ключ к возникновению лекарственной устойчивости во время лечения.
Авторы отмечают, что неизвестно, насколько репрезентативна бактериальная популяция мокроты по отношению ко всей микобактериальной популяции внутри человека. Бактерии в мокроте в основном отражают популяцию Mtb из очагов, которые открыты и связаны с дыхательными путями. Тем не менее считается, что туберкулезные бациллы в мокроте происходят из мест интенсивного бактериального роста, поэтому можно предположить, что исследованные изоляты наиболее клинически значимы.
Источник
Qingyun Liu, et al. // Mycobacterium tuberculosis clinical isolates carry mutational signatures of host immune environments. // Science Advances 29 May 2020: Vol. 6, no. 22, eaba4901; DOI: 10.1126/sciadv.aba4901


 Меню
Меню





 Все темы
Все темы




 0
0