Некоторые пробиотики подавляют защитные свойства кишечника вместо того, чтобы восстановить их
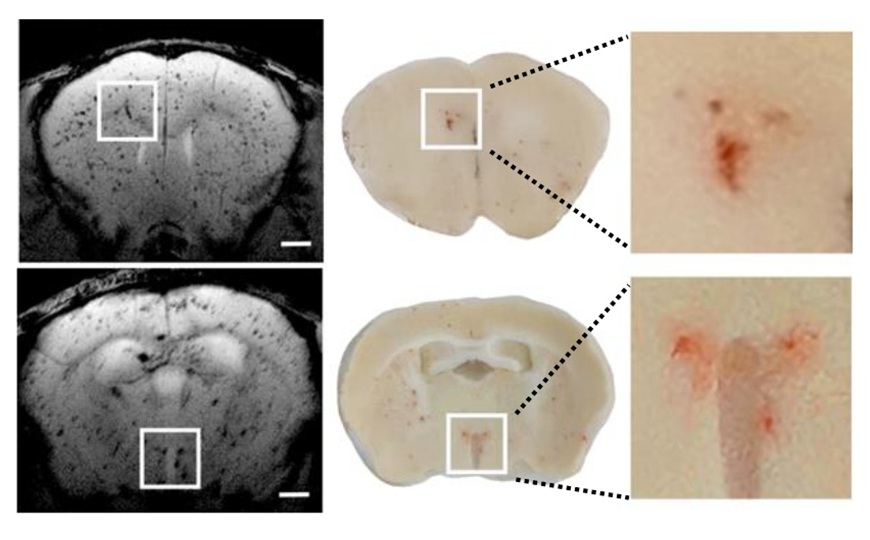
Антибиотикотерапия может нарушить кишечную микробиоту и ослабить устойчивость к таким патогенам, как Clostridioides difficile. Ученые из США исследовали влияние двух распространенных пробиотических штаммов — Lactobacillus acidophilus NCFM и L. gasseri Lg-36 — на восстановление устойчивости к C. difficile у мышей после курса антибиотиков. Оказалось, что L. acidophilus не только не защищает организм, но и усугубляет инфекцию, увеличивая бактериальную нагрузку. В то же время L. gasseri ускоряет восстановление устойчивости, полностью подавляя колонизацию C. difficile уже к третьей неделе. Этот эффект сопровождается увеличением численности бактерий семейства Muribaculaceae, способных ограничивать рост C. difficile.

Прием антибиотиков может нарушить баланс кишечной микробиоты и снизить устойчивость организма к патогенам, включая Clostridioides difficile — одну из главных причин антибиотик-ассоциированной диареи. Чтобы восстановить бактериальный баланс, многие пациенты принимают пробиотики, в том числе различные штаммы Lactobacillus, однако их влияние на возвращение резистентности к патогенам остается плохо изученным. Исследователи из США провели эксперимент на мышах, чтобы выяснить, как два популярных пробиотических штамма — L. acidophilus NCFM и L. gasseri Lg-36 — влияют на восстановление устойчивости к C. difficile после антибиотикотерапии.
Мышам давали антибиотик цефоперазон, а затем однократно вводили один из пробиотиков или ничего (контроль). После этого каждую неделю животных заражали спорами C. difficile и наблюдали за симптомами инфекции, бактериальной нагрузкой и составом микробиоты в течение четырех недель. Оказалось, что штамм L. acidophilus замедлял восстановление резистентности и повышал количество C. difficile и уровни токсинов на 2–3 неделе. Даже после того, как сам пробиотик переставал обнаруживаться в кишечнике, его влияние сохранялось. Напротив, штамм L. gasseri способствовал снижению нагрузки C. difficile, ускорял восстановление резистентности, а на третьей неделе полностью предотвращал колонизацию патогеном. Причем к этому времени сам L. gasseri уже не детектировался в кишечнике.
Дополнительные in vitro эксперименты показали, что L. gasseri вырабатывает термостабильный белковый антибактериальный фактор, чувствительный к протеинкиназе K (вероятно, бактериоцин), подавляющий рост C. difficile. Геномный анализ выявил у Lg-36 уникальные гены, кодирующие такие бактериоцины. Однако защитный эффект на 3-й неделе, вероятно, был обусловлен не прямым действием бактериоцина, а вторичным эффектом на состав микробиоты.
Микробиомный анализ показал значительный рост количества представителей семейства Muribaculaceae в группе, получавшей L. gasseri. Особенно выделялись три вида, коррелирующие с восстановленной резистентностью. В лабораторных условиях представители этих бактерий — Muribaculum intestinale и Duncaniella muris — замедляли рост C. difficile, особенно при наличии сахаров, которые обычно потребляет патоген. Это говорит о возможной конкуренции за субстраты как одном из механизмов защиты.
Таким образом, разные пробиотические штаммы могут оказывать противоположное влияние на восстановление кишечной микробиоты и устойчивость к патогенам после приема антибиотиков. L. acidophilus в данной модели усугублял инфекцию C. difficile, тогда как L. gasseri, напротив, способствовал восстановлению резистентности. Эти эффекты реализуются как напрямую (через бактериоцины), так и опосредованно (через изменение микробного состава и стимулирование роста Muribaculaceae). Авторы подчеркивают необходимость детальной оценки каждого пробиотического штамма, особенно в контексте восстановления после антибиотиков, и рассматривает Muribaculaceae как перспективных кандидатов в пробиотики следующего поколения.
Терапия акне пробиотиками может быть наиболее успешной в подростковом возрасте
Источник:
Foley M., et. al. Differential modulation of post-antibiotic colonization resistance to Clostridioides difficile by two probiotic Lactobacillus strains. // mBio (2025), published online 21 July 2025. DOI: 10.1128/mbio.01468-25


 Меню
Меню





 Все темы
Все темы



 0
0