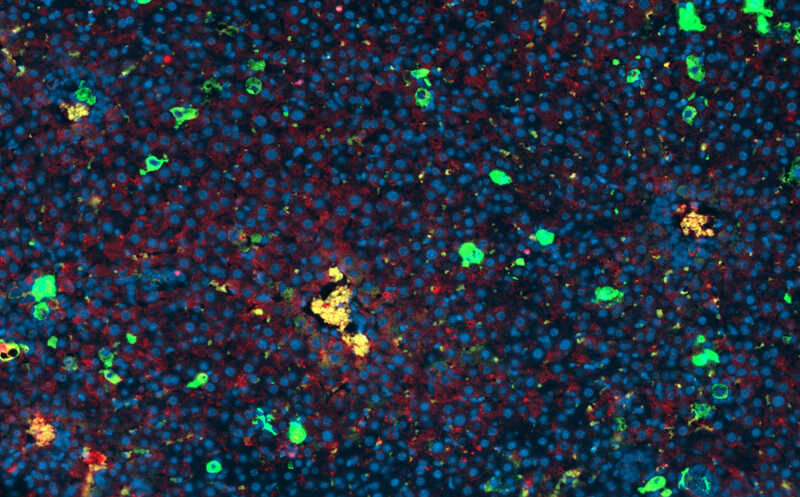
Нейрофиброз вызывает резистентность к инсулину и ожирение
В периферических тканях причиной инсулинорезистентности и ожирения может быть фиброз — разрастание внеклеточного матрикса. Международный коллектив ученых показал, что ожирение может вызывать ремоделирование особого типа нейронального внеклеточного матрикса — перинейрональных сетей — в дугообразном ядре гипоталамуса. Эти сети физически препятствуют доступу инсулина к клеткам, а их разрастанию способствует нейровоспаление. Исследователи улучшили чувствительность к инсулину и снизили вес мышей с ожирением, разрушив перинейрональные сети с помощью фермента хондроитиназы или малой молекулы — флуорозамина.
Фиброз, то есть разрастание внеклеточного матрикса (ВКМ) периферических тканей, часто приводит к инсулинорезистентности, поскольку препятствует доступу инсулина к клеткам, а это, в свою очередь, становится причиной ожирения. В мозге есть особый вид ВКМ — перинейрональные сети, которые окружают синапсы нейронов и регулируют их работу. Ремоделирование перинейрональных сетей уже связывали с множественным склерозом, хроническим болевым синдромом и эпилепсией. Теперь международный коллектив ученых показал, что нейрофиброз — разрастание перинейрональных сетей — служит причиной инсулинорезистентности и развития метаболического синдрома.
Ученые сосредоточились на дугообразном ядре гипоталамуса: этот участок мозга регулирует нейроэндокринную систему, а при метаболическом синдроме его клетки становятся устойчивыми к инсулину. В дугообразном ядре гипоталамуса вокруг нейронов образуются перинейрональные сети, причем они увеличиваются в размерах у мышей, которых кормили диетой с высоким содержанием жиров и сахаров. Разрастание ВКМ предшествовало набору веса и появлению признаков метаболического синдрома, при этом такого же разрастания перинейрональных сетей не происходило в других участках мозга — в вентромедиальном ядре гипоталамуса или в ретроспленальной коре.
Исследователи показали, что перинейрональные сети при нейрофиброзе дугообразного ядра в основном состоят из аггрекана (протогликановый хондроитинсульфат 1). Также при ожирении в них накапливаются другие компоненты ВКМ: верзикан, нейрокан и бревикан.
В дугообразном ядре гипоталамуса есть две важные популяции нейронов, экспрессирующие AgRP (агути-подобный пептид) либо POMC (проопиомеланокортин). У здоровых мышей перинейрональные сети образуются вокруг 45% AgRP+ и 24% POMC+ нейронов. При ожирении они разрастаются только вокруг AgRP+ нейронов, что указывает на их важную роль в развитии метаболического синдрома. В норме период обновления перинейрональных сетей равен 5 неделям, за которые они успевают и образоваться, и разложиться, однако при ожирении он увеличивается вдвое. Причина этого — сниженная экспрессия протеаз ВКМ и повышенная экспрессия их ингибиторов, что в целом замедляет деградацию перинейрональных сетей.
Чтобы подтвердить, что именно нейрофиброз вызывает ожирение, ученые разрушали перинейрональные сети с помощью хондроитиназы ABC, которую вводили прямо в дугообразное ядро мышей с ожирением. В результате вес мышей уменьшался, они начинали меньше есть, в клетках белой и бурой жировой ткани активировался термогенез. Также у мышей еще до сброса веса улучшался гомеостаз глюкозы и снижалась инсулинорезистентность. Те же результаты получили, когда вводили хондроитиназу в мозг мышей с диабетом 2 типа (линия db/db) и мышей, являющихся генетической моделью ожирения (линия NZO).
Далее ученые оценили, как нейрофиброз влияет на инсулиновый сигналинг в клетках дугообразного ядра гипоталамуса. При ожирении нарушалось фосфорилирование киназы AKT, которое происходит после связывания инсулина с его рецептором. Если же перинейрональные сети разрушали хондроитиназой, то чувствительность клеток к инсулину повышалась за счет восстановления инсулинового сигналинга: повышалось фосфорилирование как рецептора инсулина, так и AKT. Эти эффекты наблюдались уже через два дня после введения хондроитиназы — до того, как снижался вес.
Влияние нейрофиброза на инсулиновый сигналинг подтвердили и с помощью генной инженерии. У мышей с нокаутом по рецептору инсулина хондроитиназа.не оказывала положительных эффектов.
Исследователи предположили, что разросшиеся перинейрональные сети физически препятствуют доступу к клеткам. Это удалось подтвердить за счет методов флуоресцентной визулизации. Также ученые показали in vitro, что аггрекан, хондроитин 4-сульфат и другие компоненты ВКМ связывают инсулин за счет электростатических взаимодействий.
В норме AgRP+ нейроны передают тормозящие сигналы в другой отдел гипоталамуса — паравентрикулярное ядро. При ожирении эти нейроны становились гиперактивными. Если перинейрональные сети разрушали хондроитиназой, то в нейронах восстанавливалась экспрессия калиевых ионных каналов, что приводило к гиперполяризации мембраны нейронов и снижало частоту их спайков. Этот процесс также опосредован инсулином. Кроме того, исследователи показали, что при ожирении AgRP+ нейроны подают больше спонтанных сигналов в паравентрикулярное ядро, таким образом распространяя метаболическую дисфункцию.
В периферических тканях фиброз часто развивается в очагах воспаления. Ученые предположили, что и причиной нейрофиброза может быть нейровоспаление. Действительно, у мышей с ожирением был воспален гипоталамус. Если им вводили растворимые рецепторы TNFα и TGFβ, снижающие воспаление за счет связывания этих молекул, то в дугообразном ядре уменьшались перинейрональные сети. Это также замедляло набор веса, снижало аппетит и ускоряло насыщение, улучшало чувствительность к инсулину. И напротив, если здоровым мышам вводили вирусные вектора, несущие гены TNFα и TGFβ для их оверэкспрессии, таким образом индуцируя нейровоспаление, то в дугообразном ядре гипоталамуса происходило разрастание перинейрональных сетей, что приводило к набору веса, снижению насыщаемости и системной инсулинорезистентности. Таким образом, воспаление в гипоталамусе приводит к метаболическому синдрому, который охватывает весь организм.
Нейрофиброз может быть мишенью для лечения ожирения. Ученые показали это на примере флуорозамина — малой молекулы, которая подавляет синтез хондроитинсульфатов. Флуорозамин вводили мышам с ожирением в желудочки мозга в течение 10 дней, что снизило нейрофиброз в дугообразном ядре, но не в других отделах мозга. В результате вес мышей снижался, они меньше ели, у них улучшалась чувствительность к инсулину. У мышей с диабетом 2 типа флуорозамин способствовал ремиссии метаболического синдрома. В целом флуорозамин оказывал те же положительные эффекты, что и хондроитиназа, хотя эти вещества действуют по разным механизмам. Исследователи также показали, что флуорозамин можно вводить мышам интраназально, и он сохраняет эффективность. Это подтверждает возможность терапевтического применения у людей.
Нейропептид Y защищает от ожирения и поддерживает способность к термогенезу
Источник
Beddows, C. A. et al. Pathogenic hypothalamic extracellular matrix promotes metabolic disease // Nature. 2024. DOI: 10.1038/s41586-024-07922-y


 Меню
Меню





 Все темы
Все темы




 0
0