Нобелевская премия-2024: открытие микроРНК
В этом году Нобелевская премия по физиологии или медицине присуждена Виктору Эмбросу и Гэри Равкану «за открытие микроРНК и их роли в посттранскрипционной регуляции гена». В 1993 году они впервые описали РНК нематоды Caenorhabditis elegans. Эта РНК не кодировала белка и в то же время играла ключевую роль в регуляции развития животного. Так был открыт новый регуляторный механизм, действующий на уровне матричной РНК.
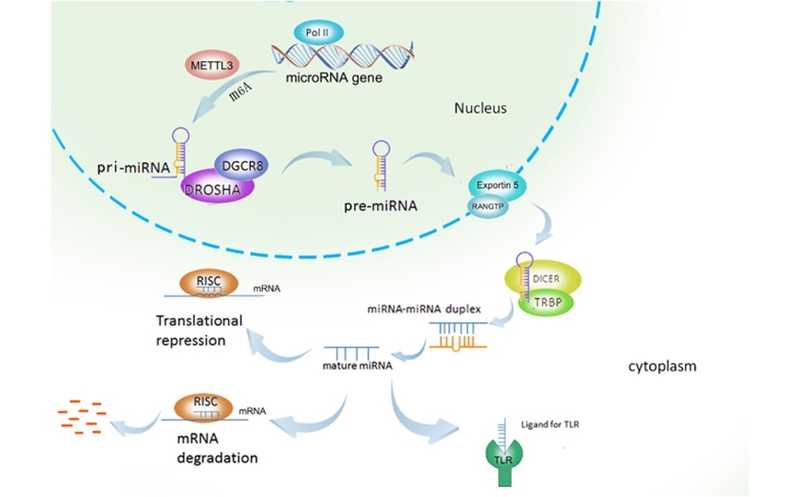
Биогенез и активность микроРНК
Credit:
Sig Transduct Target Ther (2016). DOI: 10.1038/sigtrans.2015.4 | CC BY 4.0
Как регулируется активность генов в клетке, за счет чего обеспечивается включение нужных генов в определенное время и определенном типе клеток — вопрос, который был поставлен в самые первые годы существования молекулярной биологии. В 1960-е годы были открыты транскрипционные факторы — белки, которые связываются с регуляторными участками гена и контролируют активность транскрипции (синтеза матричной РНК). Но только в 1990-е выяснилось, что есть и другой уровень регуляции — посттранскрипционный, мишенью которого является мРНК.
Виктор Эмброс и Гэри Равкан в конце 1980-х были постдоками у Роберта Хорвица в MIT, который получил Нобелевскую премию в 2002 году вместе с Сиднеем Бреннером и Джоном Салстоном. В лаборатории Хорвица работали с Caenorhabditis elegans — свободноживущей почвенной нематодой длиной около 1 мм. Это один из самых простых многоклеточных организмов, удобный для детального изучения на клеточном и молекулярном уровне. Популярным модельным объектом C. elegans стала после работ Сиднея Бреннера.
Эмброс и Равкан исследовали гены, контролирующие своевременную активацию других генов. Они изучали две мутантные линии червей с нарушениями развития, lin-4 и lin-14. Эмброс показал, что ген lin-4 — негативный регулятор гена lin-14.
К анализу мутантов lin-4 Виктор Эмброс вернулся в своей лаборатории в Гарвардском университете. Он клонировал ген lin-4, и оказалось, что его продукт — очень короткая молекула РНК, которая не кодировала белок. Было непонятно, как он может регулировать активность другого гена.
В то же время Гэри Равкан клонировал ген lin-14 в своей лаборатории в Массачусетской больнице общего профиля и Гарвардской школе медицины. Он показал, что lin-4 не ингибирует продукцию мРНК lin-14. Это означало, что регуляция происходит на более поздней стадии — мРНК синтезируется, но белок не вырабатывается. Экспериментально было установлено, что для ингибирования продукции белка необходим определенный участок в 3’-некодирующей области мРНК lin-14.
Когда Эмброс и Равкан сопоставили полученную информацию, стало ясно, что РНК lin-4 частично комплементарна именно необходимому для ингибирования сегменту мРНК lin-14. В дальнейших экспериментах они продемонстрировали, что связывание действительно происходит и блокирует синтез белка lin-4. Таким образом, они открыли новый принцип регуляции активности генов.
Две статьи Эмброса и Равкана с коллегами о lin-4 и lin-14 были опубликованы в журнале Cell в 1993 году. Сначала они не привлекли особого внимания — необычный регуляторный механизм воспринимался как особенность C. elegans, вероятно, несвойственная позвоночным. Однако в 2000 году Равкан с соавторами опубликовал статью о регуляторной РНК let-7, которая оказалась высококонсервативной и встречалась у самых разных таксонов животных, включая человека. Интересно, что у всех билатеральных животных, даже у позвоночных, не имеющих личиночных стадий, экспрессия гена let-7 четко изменяется во времени. В последующие годы были обнаружены сотни микроРНК.
Связывание микроРНК с мРНК приводит к подавлению синтеза белка или деградации мРНК. За открытие РНК-интерференции — пути подавления экспрессии, в котором важную роль играют микроРНК, — в 2006 году получили Нобелевскую премию Эндрю Файер и Крейг Мелло.
Сегодня мы знаем более тысячи генов микроРНК в геноме человека, которые кодируют более двух тысяч зрелых форм микроРНК. При этом одна микроРНК может регулировать экспрессию множества генов, и один ген может регулироваться разными микроРНК.
Нарушение активности микроРНК может приводить к развитию онкозаболеваний, потере зрения и слуха, аномалиям развития. Первым заболеванием человека, для которого описали связь с микроРНК, был хронический лимфолейкоз, причем микроРНК в этом случае могут работать и как супрессоры опухолей. и как онкогены. Синдром DICER1 — редкое тяжелое заболевание, при котором повышен риск развития доброкачественных и злокачественных опухолей в легких, почках, яичниках, щитовидной железе — связан с аутосомно-доминантной мутацией в гене DICER1, продукт которого расщепляет пре-микроРНК, чтобы получились микроРНК.
Источник
Press release. NobelPrize.org. Nobel Prize Outreach AB 2024. Mon. 7 Oct 2024.


 Меню
Меню





 Все темы
Все темы



 0
0











