Новый CRISPR-тест для диагностики шистосомоза
Ученые из Великобритании разработали новый высокочувствительный и специфичный CRISPR-тест для обнаружения Schistosoma haematobium в моче. Метод может найти широкое применение в регионах со сложной санитарно-эпидемиологической обстановкой и помочь в искоренении шистосомозов.
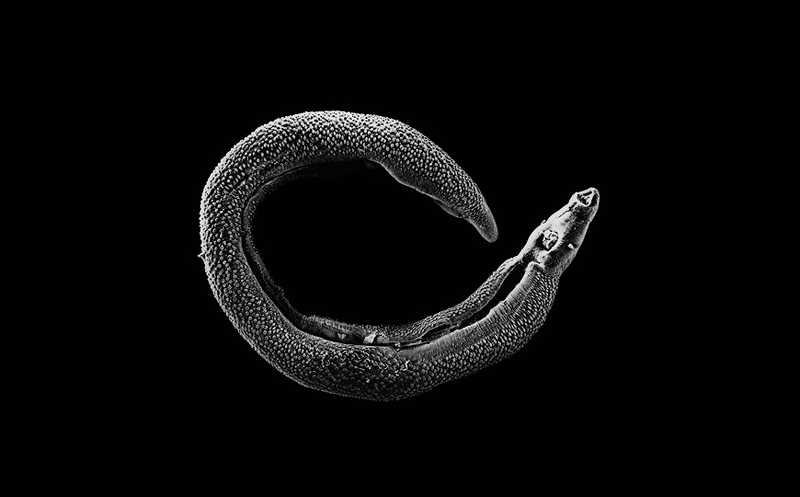
Трематода Schistosoma haematobium вызывает паразитарные болезни у людей. По последним данным, около 240 миллионов человек страдают шистосомозами, 90% из них проживают в странах Африки. Ежегодно заболевание уносит жизни сотен тысяч человек. Шистосомозы наиболее распространены у детей. Они могут вызывать повреждение печени, воспаление кишечника и мочевыводящих путей, почечную недостаточность, бесплодие и рак мочевого пузыря, шейки матки. ВОЗ планирует искоренить шистосомозы к 2030 году, однако перед учеными и врачами стоит множество проблем. Отсутствие эффективного и удобного метода диагностики — одна из них.
Учитывая успех CRISPR-технологии в диагностике вирусных и бактериальных болезней (диагностика COVID-19 создала много прецедентов, есть даже тест на туберкулез, основанный на этом принципе), исследователи из Лондонского центра забытых тропических заболеваний и Лондонского университетского колледжа вместе с коллегами решили создать чувствительный, специфичный и доступный диагностический тест на S. haematobium.
Тест получил название CATSH; это оптимизация одной из версий протокола DETECTR «всё в одном». Конструирование crРНК осуществляли с помощью онлайн-программы CRISPOR, в качестве мишени использовали фрагмент последовательности Dra1 (богатый повторами регион генома паразита). Было получено три варианта crРНК, из них для финального анализа выбрана одна, показавшая более высокую флуоресценцию конечной точки.
Реакционная смесь состоит из трех компонентов: компонент А содержит необходимые вещества для рекомбиназной полимеразной амплификации (РПА), компонент В — одноцепочечную ДНК с флуорофором FAM и гасителем (подробнее в статье Дженнифер Дудны с коллегами), компонент С — Cas12a и crРНК. Компонент С обнаруживает целевые ампликоны, образовавшиеся во время РПА, при этом также происходит расщепление оцДНК и высвобождение флуоресцирующих зондов, сигнал от которых регистрируется в реальном времени. Для старта реакции добавляли ацетат магния, а затем пробирки инкубировали в течение 40 минут при 37°С. Сначала исследование проводилось на специально подготовленных материалах с ДНК S. haematobium или его яйцами. Затем для анализа использовалась моча с яйцами паразита или без.
Аналитическая чувствительность CATSH составила 1,35 пг геномной ДНК S. haematobium. Тест стабильно и быстро (за 12 минут) обнаруживал одно яйцо паразита в исследуемом материале. К тому же CATSH оказался способен выявить и другие виды шистосом — S. bovis и S. curassoni, но не S. mansoni. При работе с образцами мочи чувствительность сохранялась, но необработанная моча мешала корректной реакции между компонентами смеси. Ученые заметили, что инкубация мочи в молекулярно-транспортной среде улучшает обнаружение яиц, поэтому образцы инкубировали в течение часа, а затем центрифугировали. При этом общее время анализа составило 2 часа.
Затем исследователи проверили, насколько стабильны реактивы в разных условиях. После лиофилизации сохранилось примерно 60% от конечной точки флуоресценции нелиофилизированных реагентов, но все еще была возможна детекция 10 пг ДНК. При хранении в морозильной камере при -20°С в высушенном виде в течение одного месяца и даже после четырех часов при 30°С также сохранялась возможность определения 10 пг ДНК. Лиофилизация и длительный срок хранения компонентов позволяют использовать CATSH в полевых условиях.
CATSH показал стабильное и достоверное определение шистосом в материале. Предполагается, что метод может обнаружить яйца шистосомы в моче даже при низкой интенсивности инвазии. Авторы отмечают, что при больших объемах образца, необходимо концентрирование.
Источник
Cherkaoui, D., et al. CRISPR-assisted test for Schistosoma haematobium // Scientific Reports 13, 4990. March 27, 2023. DOI: 10.1038/s41598-023-31238-y


 Меню
Меню





 Все темы
Все темы



 0
0