Полимерный электрод синтезировался в мозге живой мыши
Мягкие проводящие синтетические материалы, способные интегрироваться в живую нервную ткань, необходимы для развития биоэлектронной медицины и нейротехнологий. Один из перспективных подходов — инъекция мономеров, из которых полимерный электрод синтезировался бы на месте. Однако для этой реакции нужны катализаторы, как правило, токсичные. Авторы статьи в Science провели синтез оптически чувствительного полимера в мозге мыши, причем катализировал реакцию гемоглобин. Для «включения» электрода и стимуляции нейронов использовали ближний инфракрасный свет, проникающий в ткани. Воздействие было тормозящим, и оно изменило поведение мышей — они стали чаще ошибаться при выполнении задания.
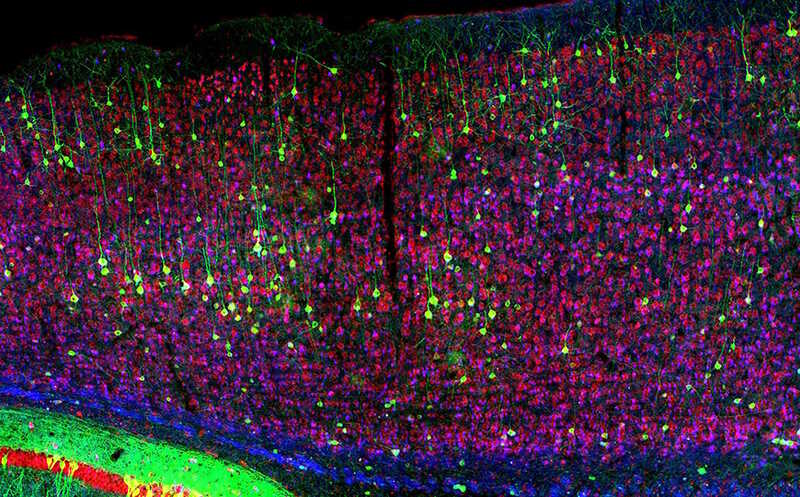
Исследователи из Университета Пердью (США) синтезировали светочувствительные полимерные электроды с полупроводниковыми свойствами прямо в мозге живых мышей. Это может стать новым направлением в разработке5 минимально инвазивных биоэлектронных интерфейсов.
Биосовместимые электроды в мозге или другой ткани (например, для лечения нейродегенеративных заболеваний или контроля сердечной деятельности) должны быть сделаны из мягких синтетических материалов. Перспективные свойства демонстрируют проводящие полимеры — макромолекулы с чередующимися одинарными и двойными углерод-углеродными связями. Их биосовместимость лучше, чем у металлов и неорганических полупроводников, они обладают регулируемыми оптическими и электрохимическими свойствами и могут одновременно транспортировать ионы и электроны. Однако импланты из таких полимеров трудно поместить в нужное место организма. Доставка объектов микрометрового — миллиметрового размеров обычно требует хирургического вмешательства. Но можно делать инъекцию раствора мономеров в мозг и затем производить полимеризацию на месте.
Подобные эксперименты ранее уже выполнялись. В некоторых работах животных генетически модифицировали, чтобы в их клетках появились компоненты, нужные для полимеризации. Но маловероятно, что такой подход удастся применить к человеку. Альтернативой может быть сборка, запускаемая определенными условиями среды (уровнем рН, концентрацией активных форм кислорода). В одной из работ электроды из поли(3,4-этилендиокситиофена) синтезировались в центральной и периферической нервной системе данио за счет ферментативной сборки. Но и в этой работе использовались экзогенные окислители, а токсичные побочные продукты реакции вызывали апоптоз.
Авторы новой работы сумели обойти это ограничение. Полимер с полупроводниковыми свойствами — n-допированный поли(бензодифурандион), или n-PBDF — образовывался прямо в мозге бодрствующей мыши или в эмбрионе рыбки данио. Для его синтеза с последующим восстановительным допированием требовались только естественные компоненты крови — гемоглобин и вода (обычно эту реакцию катализирует ацетат меди, неподходящий для применения in vivo). Кстати, другие гемсодержащие белки, такие как миоглобин или цитохром с, тоже катализировали эту реакцию.
Спектроскопия эмбрионов рыбок подтвердила образование n-PBDF в желточных мешках. Эмбрионы развивались нормально, двигались естественно, через неделю после инъекции выжило более 80%. В мозге мышей полимер был локализован в месте инъекции и оставался стабильным без признаков воспаления или гибели нейронов. Поведение животных не изменилось.
Таким образом, можно предположить, что в месте инъекции возникает «бесшовный» интерфейс между полимером и окружающими тканями, и для этого не требуются обширные хирургические вмешательства или токсичные вещества.
Что касается способов «включения» n-PBDF, он обладает оптической чувствительностью — воспринимает ближний инфракрасный свет, проникающий в ткани на несколько миллиметров. Это делает возможной обратимую температурную или электрическую стимуляцию нейронов с миллисекундным временным разрешением и субмикронным пространственным разрешением. В нейронах изменялась активность натриевых и калиевых каналов, критически важная для возбуждения и торможения. (Эти данные были получены в экспериментах на нейронах вне организма.)
Наконец, провели эксперименты на мышах, которым вводили мономеры в первичную моторную кору, захватывая дендриты. Стимуляция участков n-PBDF в ближнем ИК-диапазоне обратимо подавляла возбудимость дендритов (обычно дендриты трудно таргетировать). Воздействие было тормозящим, и у мышей значительно изменялось поведение: до эксперимента они были обучены нажимать на рычаг за вознаграждение, и при стимуляции возрастало число ошибок. Подавление избыточного возбуждения нейронов может быть полезно при таких неврологических заболеваниях, как эпилепсия или болезнь Паркинсона.
Тем не менее вопросы остаются: например, не создаст ли нежелательных побочных эффектов одновременная электрическая и температурная стимуляция, не токсичны ли мономеры и полимеры n-PBDF на больших временных промежутках, и наконец, насколько применим этот метод для крупных биообъектов, таких как человек. Также было бы интересно проверить, можно ли аналогичным образом создавать электроды для возбуждения, а не торможения сигналов нейронов или комбинировать эти методы модуляции нейронной активности с другими, например, с магнитной стимуляцией.
Источники
Sanket Samal, et al. Blood-catalyzed n-doped polymers for reversible optical neural control // Science. 2 Apr 2026. Vol 392, Issue 6793. DOI: 10.1126/science.adu5500
M. R. Antognazza, G. Lanzani. Cured by blood // Science. 2 Apr 2026. Vol 392, Issue 6793. DOI: 10.1126/science.aeg1547


 Меню
Меню





 Все темы
Все темы




 0
0