Препараты на основе лектинов могут заменить антитела в иммунотерапии рака
Ученые из Калифорнийского университета в Ирвайне разработали новый класс иммунопрепаратов на основе лектинов, которые используют принцип «липучки» для уничтожения опухолевых клеток. Созданные ими молекулы GlyTR связываются с углеводными антигенами, которые обильно экспрессируются злокачественными клетками, но практически отсутствуют в нормальных тканях; это взаимодействие привлекает к опухолевым клеткам T-лимфоциты. Такой подход может быть полезен при разработке универсальной иммунотерапии, не зависящей от свойств опухолевого микроокружения.
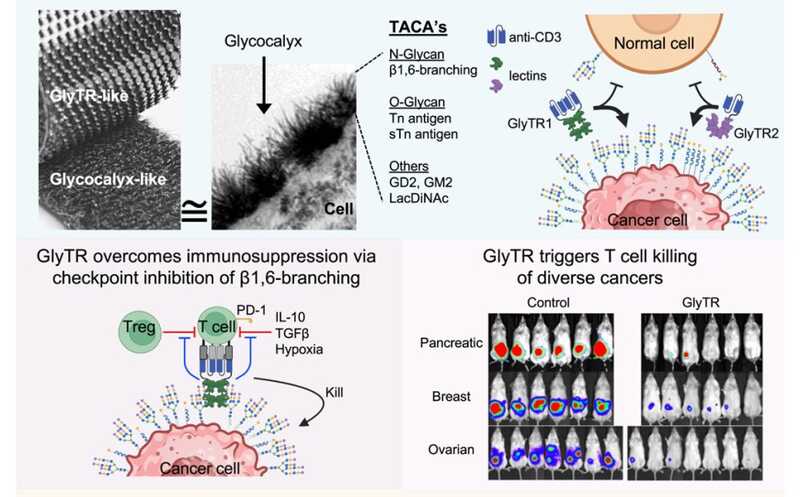
Cell (2025). DOI: 10.1016/j.cell.2025.09.001 | CC BY 4.0
Современные иммунотерапевтические стратегии, включая биспецифические антитела и CAR-T-клетки, уже доказали свою эффективность в лечении B-клеточных лимфопролиферативных заболеваний, однако их применение при солидных опухолях ограничено. Одна из главных трудностей заключается в отсутствии безопасных антигенов: антитела с высоким сродством (аффинностью) могут атаковать здоровые ткани даже при минимальной экспрессии в них белка-мишени, вызывая тяжелые побочные эффекты.
Перспективными мишенями могут стать опухоль-ассоциированные углеводные антигены (TACA). Поскольку практически все поверхностные белки клетки гликозилированы, плотность TACA на единицу поверхности может быть в тысячи раз больше, чем у белковых антигенов. Особенно важны β1,6GlcNAc-разветвленные N-гликаны и антиген Tn — первые в значительно большем количестве экспрессируются на поверхности опухолевых клеток при активации сигнальных путей RTK/RAS/PI3K, а второй — при нарушении биосинтеза O-гликанов (полисахаридов, присоединяющихся к ОН-группе аминокислотного остатка белка). Наличие этих молекул ассоциировано с ростом, инвазией и метастазированием опухоли.
Однако антитела против чистых углеводов оказались малоэффективными. Вместо антител авторы нового исследования предложили предложили использовать лектины — белки, естественно связывающиеся с углеводами. Так появилась идея гликан-зависимых рекрутеров T-клеток (GlyTR, glycan-dependent T cell recruiter, читается как «глиттер») — гибридных молекул, которые объединяют лектин и фрагмент антитела против CD3 — молекулы на поверхности T-лимфоцитов. Благодаря множественным точкам связывания лектины действуют как текстильная «липучка»: прочно фиксируются на клетках с высокой плотностью антигена, но не взаимодействуют с поверхностью клеток, на которых плотность целевых гликанов низкая.
Первый вариант препарата, GlyTR1, был создан на основе лектина L-PHA из фасоли обыкновенной (Phaseolus vulgaris), способного связываться с β1,6-разветвленными гликанами. Соединив четыре домена L-PHA с двумя фрагментами антитела к CD3, исследователи получили молекулу, которая может одновременно распознавать опухоль и активировать Т-лимфоциты. Препарат был одинаково эффективен при использовании Т-клеток разных доноров и успешно подавлял клетки тройного негативного рака молочной железы. При этом для стимуляции T-клеточной цитотоксичности было достаточно малой концентрации GlyTR1 (∼0.5–1 нг/мл).
Вторая молекула, GlyTR2, была создана на основе человеческого лектина CD301, экспрессируемого в макрофагах и дендритных клетках. CD301 распознает сразу несколько углеводных антигенов — Tn, сиалил-Tn, GD2, GM2 и LacDiNAc. Оптимизированная конструкция с четырьмя доменами CD301 эффективно связывала гликаны и была достаточно стабильной. GlyTR2 взаимодействовал с клетками T-клеточного лейкоза и тройного негативного рака молочной железы, индуцируя активацию Т-клеток и противоопухолевую токсичность. Важно, что он не взаимодействовал с эритроцитами (антигены на их поверхности имеют сходство с мишенями CD301), а сила эффекта зависела от плотности антигена на поверхности клеток и не изменялась при использовании T-лимфоцитов разных доноров.
Оба препарата показали высокую способность к связыванию с клетками различных злокачественных опухолей: рака молочной железы, рака легкого, рака яичников, рака поджелудочной железы, рака простаты, рака толстой кишки, различных лимфопролиферативных новообразований. На образцах колоректального рака было показано, что связывание усиливается с увеличением стадии опухолевого процесса (при метастатическом заболевании плотность β1,6-разветвленных гликанов максимальна).
В гуманизированных мышиных моделях GlyTR1 и GlyTR2 продемонстрировали эффективность против протоковой аденокарциномы поджелудочной железы, тройного негативного рака молочной железы и рака яичников (как локализованных, так и метастатических), а также T-клеточного лейкоза. Оценить изменение общей выживаемости не представлялась возможным, так как гуманизация (введение мышам человеческих лимфоцитов) приводила к развитию реакции «трансплантат против хозяина» и гибели животных. Исследователям не удалось создать эффективный и безопасный мышиный аналог GlyTR, что, вероятно, связано с различиями в свойствах мышиных и человеческих T-клеток.
Еще одной особенностью GlyTR1 оказалась способность блокировать иммуносупрессивные свойства β1,6-разветвленных гликанов в отношении T- и B-лимфоцитов. Кроме того, активность GlyTR1, в отличие от «классических» биспецефических антител, не снижалась в иммуносупрессивном опухолевом микроокружении при высоких уровнях IL-10, TGFβ, гипоксии и в присутствии регуляторных Т-клеток. Это было подтверждено как в органоидной модели с использованием интерфейса «воздух-жидкость», так и в культурах метастатических опухолей (саркомы Юинга и колоректального рака), полученных от пациентов. GlyTR1 эффективно уничтожал опухолевые клетки, даже когда более 70% T-лимфоцитов в реактивном микроокружении демонстрировали признаки истощения.
Чтобы оценить безопасность GlyTR, ученые провели иммуногистохимическое исследование человеческих тканей с антителами к L-PHA, GlyTR1 и GlyTR2. Положительная реакция определялась в пищеварительном тракте, клубочках и канальцах почек и некоторых других органах. Однако эксперименты на мышах показали, что GlyTR с флуоресцентными метками не накапливаются в этих органах. В гуманизированных мышиных моделях GlyTR не приводили к потере веса, недомоганию, нарушениям функции печени, почек, поджелудочной и щитовидной желез, электролитным нарушениям, цитопении или развитию воспаления.
Исторические данные подтверждают безопасность GlyTR1: в 1960-е годы XX века экстракт красной фасоли, содержащий L-PHA, использовался для терапии апластической анемии и оказался хорошо переносимым. GlyTR2, основанный на человеческом белке CD301, также не должен вызывать патологических реакций.
в ближайшее время планируется начало производства GlyTR1 и переход к клиническим испытаниям первой фазы в рамках программы NCI Experimental Therapeutics. Как сообщается в пресс-релизе, терапия будет протестирована на пациентах с различными метастатическими солидными опухолями — это группа с наибольшей неудовлетворенной потребностью в лечении.
Гликокаликс эндотелиальных клеток защищает мозг мышей от нейродегенерации
Источник
Zhou, R.W., et al. Safe immunosuppression-resistant pan-cancer immunotherapeutics by velcro-like density-dependent targeting of tumor-associated carbohydrate antigens // Cell (2025). DOI: 10.1016/j.cell.2025.09.001


 Меню
Меню





 Все темы
Все темы




 0
0