Производное противомикробного соединения из губок подавляет рост малярийного плазмодия
Малярия — острое инфекционное заболевание, возбудитель которого часто приобретает резистентность к противомалярийным препаратам. Авторы статьи в Science синтезировали кандидатное лекарство, аналогичное по структуре соединениям, которые получают из губок, а также описали механизм действия этого препарата. Он оказался эффективен в отношении не только чувствительных, но и устойчивых к существующей терапии штаммов малярийного плазмодия.
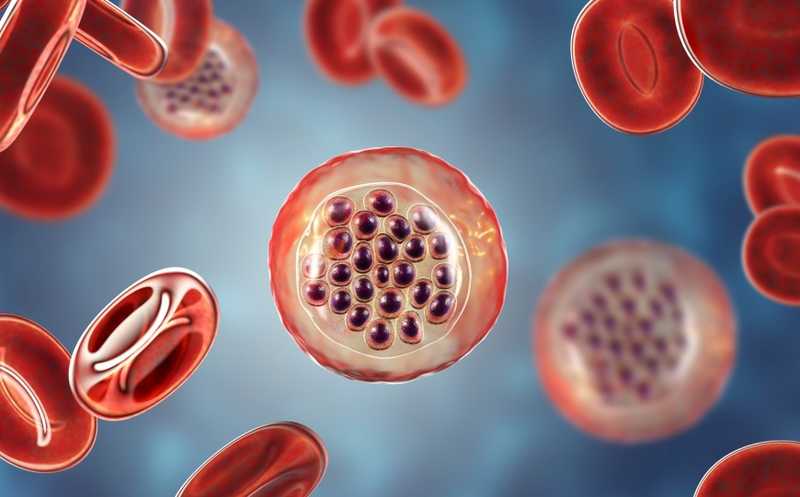
Малярия — острое инфекционное заболевание с характерными циклическими приступами лихорадки, которое передается через укусы комаров рода Anopheles. Основной возбудитель — малярийный плазмодий (Plasmodium falciparum) — часто приобретает резистентность к существующим методам терапии. Проблема осложняется дефицитом препаратов для профилактики и лечения малярии, а также сложностью разработки противомалярийных вакцин. Все это создает острую потребность в новых лекарственных средствах против малярии.
Такими средствами могли бы стать калихинолы — эти получаемые из губок соединения проявляют активность в отношении как чувствительных, так и устойчивых к лекарствам штаммов P. falciparum. Однако они сложны в крупномасштабном производстве и пока недостаточно изучены. Авторы статьи в Science сообщают о синтезе нового препарата против малярии MED6-189, представляющего собой упрощенный аналог калихинола, и подробно описывают механизм его действия.
Исследователи синтезировали несколько аналогов калихинолов A и B с упрощенной структурой, а затем проверили их противопаразитарную активность in vitro. Наиболее перспективным оказалось соединение MED6-189 — оно ингибировало рост различных штаммов малярийного плазмодия, в том числе устойчивых к препаратам (например, к хлорохину).
Механизм действия MED6-189 определили с помощью мультиомиксного подхода. Он показал, что основной мишенью кандидатного препарата является апикопласт — особая органелла, обнаруженная у большинства простейших типа Apicomplexa, к которому относятся и малярийные плазмодии. Она представляет собой нефотосинтезирующую пластиду, в которой сосредоточены жизненно важные для паразита метаболические процессы, такие как синтез жирных кислот, предшественников изопреноидов и часть пути биосинтеза гема. Изменения профиля метаболитов указали на то, что соединение нарушает биогенез апикопласта и биосинтез мембран. Белки апикопласта, с которыми в первую очередь связывался MED6-189, участвовали в транспортировке везикул и биогенезе липидов.
Результаты тестирования MED6-189 in vitro подтвердились и в опытах на гуманизированных мышах. Препарат также показал высокую активность в отношении других патогенных плазмодиев — P. knowlesi и P. сynomolgi.
С помощью длительного in vitro отбора на устойчивость к MED6-189 с последующим генетическим анализом ученые выявили мутацию в гене PfSec13, кодирующем нуклеопорин ядерного порового комплекса и играющем важную роль в обеспечении везикулярного транспорта. Отредактировав геном малярийных плазмодиев с помощью CRISPR-Cas9, ученые подтвердили, что мутации в гене PfSec13 ассоциированы с пониженной чувствительностью к препарату.
Исследователи считают, что комплексный механизм действия MED6-189 обеспечивает его высокую эффективность против возбудителей малярии и предотвращает развитие устойчивости к нему, что делает соединение перспективным для борьбы с малярией.
Источник
Z. Chahine et al., A kalihinol analog disrupts apicoplast function and vesicular trafficking in P. falciparum malaria. // Science 385, eadm7966 (2024). DOI: 10.1126/science.adm7966


 Меню
Меню





 Все темы
Все темы




 0
0