Пространственная протеомика обнаружила потенциальный маркер глиомы в крови
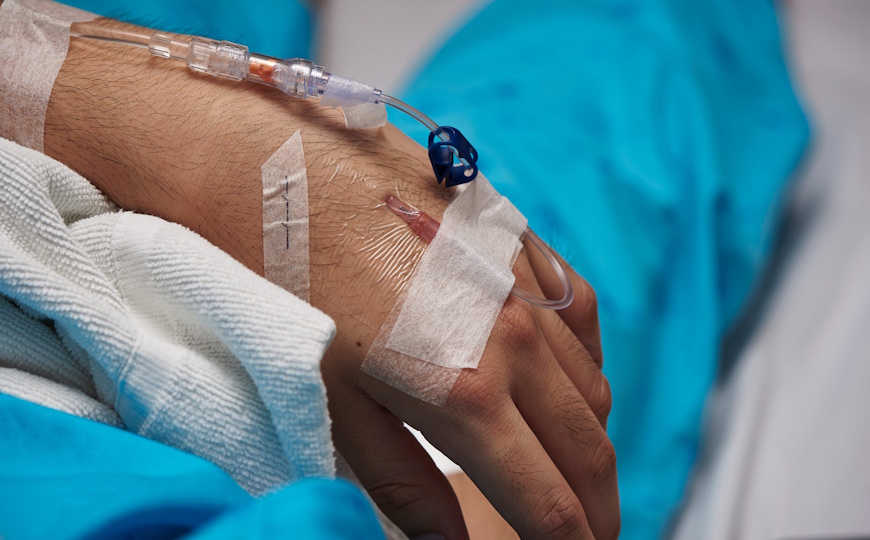
Китайские ученые применили для исследования глиом стратегию пространственно-многомерной протеомики. Во время операций они взяли у пациентов образцы крови из артерий и вен вблизи глиомы и образцы опухолевой и неопухолевой ткани. Также они собрали образцы периферической крови пациентов с глиомой и без глиомы, затем получили протеомы всех образцов и провели их масштабное сравнение. Это не только принесло новую информацию о развитии опухоли, но и позволило выявить потенциальный биомаркер для скрининга — белок SERPINA6, уровень которого снижен в крови пациентов с глиомой.
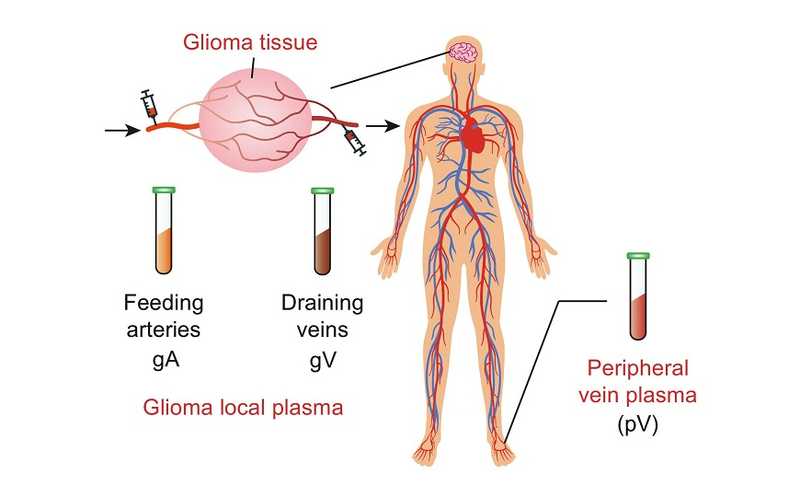
Глиома — злокачественная опухоль головного мозга. Чтобы понять молекулярные механизмы ее возникновения, необходимо идентифицировать белки, появление которых в крови и нервной ткани ассоциировано с глиомой. (Гематоэнцефалический барьер препятствует выходу белков в кровь из мозга, однако опухоли могут нарушать этот барьер, поэтому изменения протеома затрагивают и кровь.) Такой подход называется сравнительной протеомикой.
Ученые из Института перспективных исследований Уханьского университета (Китай) разработали новую стратегию выявления белковых маркеров глиомы. Уникальность предложенной стратегии заключается в многомерности выявления различий в профилях белков. Исследователи сравнивали не только белки опухолевой и неопухолевой ткани, но и белки крови из артерий и вен в области глиомы (то есть выясняли, как изменяется протеом крови, проходящей через опухоль, какие биомолекулы глиома поглощает, а какие секретирует, как она регулирует основные пути метаболизма), а также белки периферической крови.
В исследование включили несколько когорт. В одной группе у пациентов во время операций собирали кровь из артерий и вен в области глиомы, а также из периферических вен. Во второй группе собирали образцы безопухолевых тканей головного мозга, тканей глиомы и тканей, расположенных рядом с опухолью. Наконец, третья и четвертая группы включали пациентов с неглиомным заболеванием (гемифациальным спазмом) и с глиомой; у них брали периферическую кровь; на этих группах валидировали биомаркеры. Протеомный анализ проводили методом жидкостной хроматографии с тандемной масс-спектрометрией.
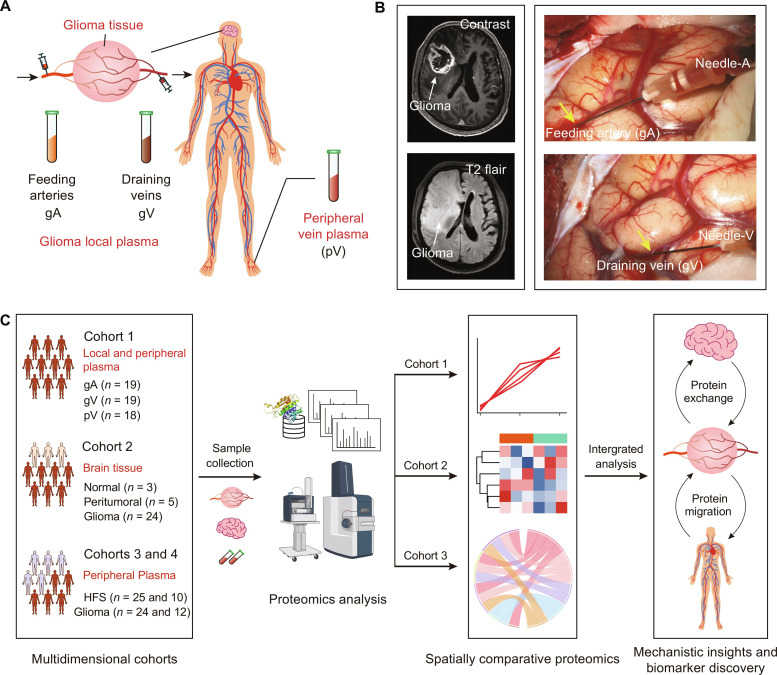 Схема исследования (пояснения в тексте). Credit: Science Advances. 2024. DOI:
10.1126/sciadv.adk1721 |
CC BY-NC 4.0 DEED
Схема исследования (пояснения в тексте). Credit: Science Advances. 2024. DOI:
10.1126/sciadv.adk1721 |
CC BY-NC 4.0 DEED
Среди белков, которых было больше в периферической крови, меньше — в артериях возле глиомы и еще меньше в венах, оказались иммуноглобулины, белки, связанные с системой комплемента, а также представители суперсемейства ингибиторов сериновых протеаз (серпины). Особенно заметно была снижена вблизи опухоли концентрация SERPINA6. Это заставило авторов предположить, что его концентрации в периферической крови людей с глиомой могут быть ниже, чем у людей без глиомы. Предположение подтвердилось, что побудило авторов проанализировать потенциал SERPINA6 как биомаркера глиомы. И действительно, исходя из данных об уровне SERPINA6, в когорте 4 (10 пациентов с глиомой и 10 пациентов без глиомы ) удалось поставить правильный диагноз 90% пациентов с опухолью и 70% пациентов без нее.
Предполагаемая функция серпинов — ингибирование циркулирующих протеаз (факторы XIa, XIIa, Ха, IXa, калликреин, плазмин, тромбин), отвечающих за свертывание крови. Известно, что в сосудах глиомы часто образуются тромбы, так что авторы статьи установили возможную причину.
Существенно больше в сосудах возле глиомы, чем в периферической крови, оказалось белков — участников путей свертывания крови, гликолиза, утилизации активных форм кислорода; все эти процессы типичны для опухолевого метаболизма. Авторы выявили в локальном окружении глиомы резкое увеличение экспрессии белка PMS2P5, участвующего в репарации ошибочно спаренных нуклеотидов (мисматч-репарации); очевидно, опухоль активировала системы восстановления поврежденной ДНК. И в периферической крови пациентов с глиомой его было больше, чем у пациентов без глиомы.
Наконец, среди белков, которых было много в периферической крови и в венах возле глиомы (то есть они могли продуцироваться как глиомами, так и тканями пациента вне ЦНС), внимание авторов привлек опухолевый супрессор, ингибитор миграции клеток CRTAC1. Его уровень был снижен в периферической крови пациентов по сравнению с людьми без глиомы.
Ожидаемо различались профили экспрессии белков в опухоли и здоровой ткани мозга. В том числе 13 белков, уровни которых в крови были разными в сосудах глиомы и в периферической крови, также отличались по уровню экспрессии в глиоме и неопухолевых тканях.
Авторы исследования полагают, что SERPINA6 можно будет использовать в качестве надежного биомаркера, например, для преддиагностического скрининга людей с высоким риском развития глиомы. Разработанный ими метод пространственно-многомерной протеомики может быть использован и для исследования других опухолей.
Источник
Shen L., et al. Mechanistic insight into glioma through spatially multidimensional proteomics // Science Advances. 2024. 6; 10(7): eadk1721. DOI: 10.1126/sciadv.adk1721


 Меню
Меню





 Все темы
Все темы




 0
0