Работу ДНК-гиразы в бактериях визуализировали на уровне единичных молекул
Использование новых методов микроскопии позволило реконструировать с разрешением до единичных молекул картину работы ДНК-гиразы. Этот фермент, необходимый для репликации бактериальной ДНК, — важнейшая мишень для антибиотиков.
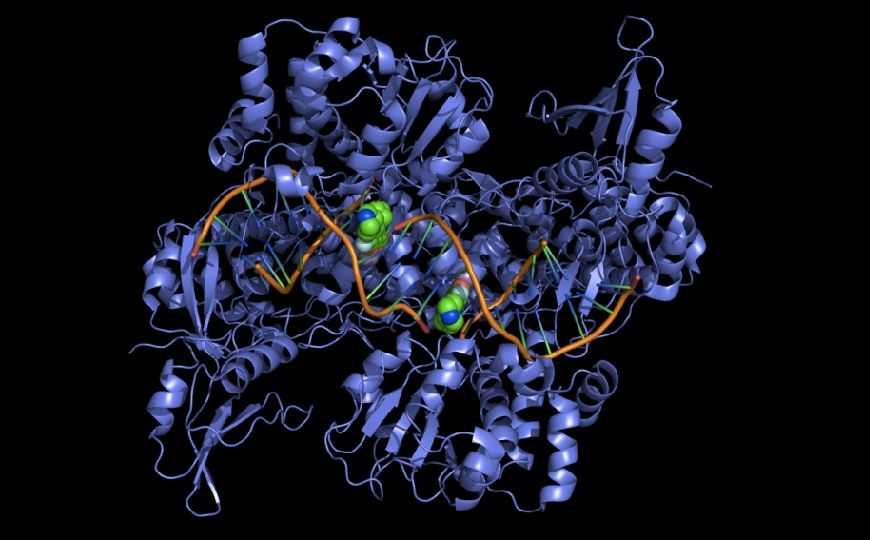
ДНК-гираза обеспечивает релаксацию суперскрученных петель кольцевой хромосомы бактерий, формируемых полимеразными комплексами во время репликации и транскрипции. Без ДНК-гиразы полимеразный комплекс останавливается, а накопившиеся участки суперскрученности мешают разделению дочерних кольцевых геномов, что в итоге приводит к гибели бактерии. Эффективные в отношении многих бактерий антибиотики фторхинолоны — ингибиторы гиразы, однако из-за распространения антибиотикорезистентности возникает потребность в новых препаратах. Визуализация деталей работы ДНК-гиразы и репликационного комплекса на молекулярном уровне может помочь создать новые высокоэффективные антибиотики.
Авторы статьи, опубликованной в Nucleic Acids Research, изучали взаимное расположение молекул ДНК-гиразы и репликационного комплекса, используя специальные методы флуоресцентной микроскопии, позволяющие достичь разрешения, сравнимого с величиной крупного белкового комплекса. Бактерии иммобилизовали в низкофлуоресцентной агарозе. Для визуализации использовали гиразу, слитую с mYPet (желтый флуоресцентный белок), и компонент реплисомы DnaN, слитый с красным флуоресцентным белком mCherry. За расстояние между ДНК-гиразой и репликационным комплексом принимали расстояние между наиболее яркими красными и желтыми пикселей изображения, обработанного математическими методами.
Для достижения разрешения, сравнимого с размером белковой молекулы, использовали технологию PALM: субъединицу ДНК-гиразы, белок GyrA в клетках метили фотоактивируемым производным mCherry — PAmCherry. Этот белок способен активироваться под действием облучения и быстро «выцветать», то есть терять способность флуоресцировать при повторном облучении. При определенном уровне возбуждающего облучения активируется лишь часть молекул такого белка, а при последующих актах облучения эти молекулы не дают сигнала. Таким образом, при помощи специального микроскопа можно снять «последовательное включение» молекул на очень малой площади так, чтобы сигналы от отдельных молекул белка не перекрывали друг друга. Из таких последовательных кадров при помощи компьютерных и математических методов реконструируется изображение с разрешением, недостижимым для обычного флуоресцентного или светового микроскопа.
Еще более интересная технология, основанная на фотоактивации, использовалась для отслеживания перемещений комплексов ДНК и гиразы. Движение молекул регистрируют точно так же, последовательно снимая возбужденные группы флуорофоров. Скорость диффузии свободных молекул в водном растворе внутри клетки известна с достаточно большой точностью. Все молекулы гиразы, которые движутся существенно медленнее, вероятно, связаны c ДНК, а значит, по замедлению диффузии гиразы можно следить за ее активностью.
Анализ распределения наиболее ярких красных и желтых пикселей показал, что ДНК-гираза и репликационный комплекс отстоят друг от друга в среднем на 256 нм. Дополнительным доказательством корректности полученных данных стала проверка частоты колокализации гиразы и реплисомы: в условиях эксперимента около 30% бактерий не содержало реплисом (деление или только заканчивалось, или еще не начиналось). Только в 30% таких реплисома-негативных бактерий наблюдались сфокусированные сигналы от ДНК-гиразы.
Для определения стехиометрии ДНК-гиразных «фокусов» использовался специальная техника — slimfield microscopy, которая оперирует поляризованным (slimfied) лазерным излучением и позволяет сделать миллисекундные снимки участка размером несколько десятков квадратных микрон. Точность линейных измерений для ДНК-гиразы составила около 40 микрон, при этом удалось установить, что расстояние между реплисомой и «фокусами», содержащими связанную с ДНК гиразу, составляет в среднем 135 нм, что существенно больше диаметра реплисомы (50 нм). Это означает, что гираза не находится в прямом контакте с работающим репликационным комплексом.
По данным, полученных при фотоактивации, общее число субъединиц гиразы GyrA в пересчете на клетку — около 1450. Авторы замечают, что из-за неполной фотоактивации это число может быть занижено примерно вдвое, но в дальнейших расчетах пользуются им. Из этого количества может получиться более 700 активных молекул гиразы (такая молекула включает две субъединицы GyrA и еще две GyrB). Однако при обработке ципрофлоксацином, который «пришивает» активный гетеротетрамер гиразы к ДНК, иммобилизованными оказались только около 600 комплексов гиразы, то есть формировать функциональные молекулы способно около 80% белка. В необработанной клетке с ДНК была связана примерно половина от этого количества, а из этих 300 комплексов лишь около 20 вовлечено в работу с реплисомой.
Поскольку фермента экспрессируется явно больше, чем нужно для обеспечения репликации, исследователи выясняли, в каких еще процессах он принимает участие. В клетке единовременно происходит около 1000 актов транскрипции, они вносят в ДНК примерно в 30 раз больше супервитков, чем репликация, и было естественно предположить, что гираза удаляет их. Однако ингибирование РНК-полимеразы рифампицином повлияло на число связанных с ДНК гиразных комплексов лишь незначительно. Учитывая, что скорость транскрипции разных генов различна, авторы предположили, что гираза не компенсирует напрямую супервитки, индуцируемые синтезом РНК, а действует на геном по более сложному и пока не понятому алгоритму.
Не полностью ясен и механизм совместной работы гиразы и топоизомеразы IV в процессе репликации. Топо IV необходима для разделения катенанов, которые формируются из дочерней и родительской цепей ДНК при ее удвоении. Число молекул гиразы и топо IV в районе реплисомы кажется недостаточным для снятия суперскрученности и разделения цепей. Однако эту «недостачу» проще объяснить, если предположить, что гираза может действовать, не диссоциируя с ДНК, а декатенирование ДНК не влияет на репликацию и индуцируется топологически после прохождения реплисомы. Наблюдения за перемещениями гиразы и репликационного комплекса позволяют сделать вывод, что положительные супервитки ДНК, формирующиеся при репликации, могут активировать гиразу на расстоянии в многие тысячи пар оснований от репликационной вилки.


 Меню
Меню





 Все темы
Все темы




 0
0