Российские ученые разработали белок-фотосенсибилизатор с повышенной фототоксичностью
Команда ученых из Сколтеха, Института биоорганической химии РАН и РНИМУ им. Н.И. Пирогова создали улучшенную версию генетически кодируемого фотосенсибилизатора SuperNova. В экспериментах на E. coli и человеческих клетках новый белок продемонстрировал более высокие скорость созревания хромофора, яркость и фототоксичность.
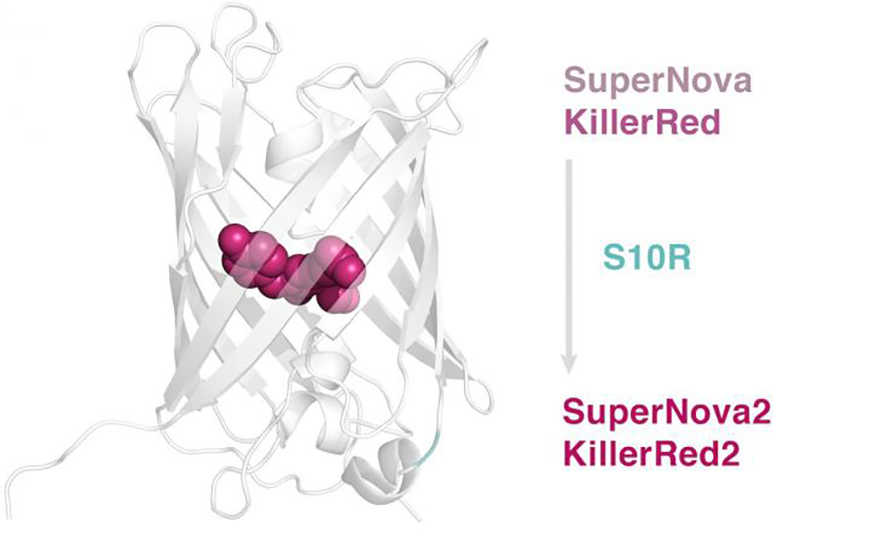
Credit: Skoltech | Пресс-релиз
Российские ученые разработали мономерный генетически кодируемый фотосенсибилизатор с повышенной фототоксичностью, что делает его более удобным инструментом в исследовательской работе.
Генетически кодируемые фотосенсибилизаторы — это белки, которые используются как оптогенетические инструменты. Ароматическая часть белка (хромофор), попадая под воздействие света и поглощая фотоны, генерирует активные формы кислорода, что приводит к цитотоксичности. Эта цитотоксичность нашла применение в разных областях исследований: от инактивации отдельных белков-мишеней или клеток до запуска сигнальных каскадов с активными формами кислорода и использования в качестве меток для электронной микроскопии.
К генетически кодируемым фотосенсибилизаторам относятся и белки семейства GFP. Такие белки олигомерны, однако в некоторых приложениях мономерные фотосенсибилизаторы более предпочтительны: их можно соединять с другими белками для адресной доставки активных форм кислорода без вмешательства в нормальную физиологию клеток.
Ранее на основе разработанного российскими учеными димерного фототоксичного белка KillerRed их японские коллеги создали и описали мономерный фотосенсибилизатор SuperNova.
«Наша лаборатория давно занимается созданием и улучшением флуоресцентных белков. Данная тема является частью моей диссертации, — рассказывает первый автор работы Дмитрий Горбачев, исследователь-стажер Центра наук о жизни Сколтеха. — SuperNova может использоваться для прицельной инактивации клеточных белков или уничтожения клеток. При сравнении фототоксичности белков KillerRed и SuperNova я обнаружил, что SuperNova имеет гораздо более низкую фототоксичность, и решил ее улучшить».
Ученые улучшали белок путем мутагенеза. Прежде таким способом не удавалось улучшить фототоксичность GFP-подобных белков, отчасти из-за непонимания, что именно в структуре белка определяет фототоксичность. Кроме того, нет подходящих высокопроизводительных скрининговых методов. В предыдущей работе авторы заметили, что во многих случаях улучшение скорости созревания хромофора коррелирует с фототоксичностью белка in vivo. Теперь они применили это наблюдение.
Ученые использовали случайный мутагенез для создания библиотеки мутантных вариантов SuperNova. В ходе скрининга на Escherichia coli использовали яркость колоний в красной части спектра как показатель созревания хромофора. Один из вариантов показывал значительно улучшенную яркость, он содержал замену S10R (серин на аргинин). Этот вариант получил название SuperNova2. Как и ожидалось, доля белка с созревшим хромофором увеличилась по сравнению с SuperNova. Далее ученые сравнили фототоксичность SuperNova и SuperNova2 в клетках человеческой линии HeLa Kyoto. Новый вариант белка продемонстрировал более высокую яркость и фототоксичность.
Кроме того, внесли замену S10R в белок KillerRed — предшественник SuperNova. Интересно, что в бактериях полученный таким образом KillerRed2 был более тусклым, чем белок без мутации. При этом в эукариотических клетках его яркость и фототоксичность увеличились.
Таким образом, ученые создали фотосенсибилизатор SuperNova2, который превосходит SuperNova в экспериментальных условиях данной работы.
«Необходимых показателей нет, — отвечает Дмитрий Горбачев на вопрос, достигнута ли цель работы. — Мы описали мутацию, которая приводит к значительному увеличению фототоксичности и скорости созревания. Но это не предел. Думаю, фототоксичность данного белка можно еще повысить».
Фототоксичность SuperNova2 все еще ниже, чем у KillerRed и KillerRed2. Авторы работы рекомендуют выбирать белок, отталкиваясь от цели исследования, и использовать KillerRed2 с митохондриальной локализацией для экспериментов, требующих гибели клеток, индуцированной светом. Для целевой инактивации клеточных белков лучше использовать SuperNova2, чтобы избежать побочных эффектов, вызванных димеризацией фотосенсибилизатора.
Источник
Gorbachev, D.A. et al. // Genetically Encoded Red Photosensitizers with Enhanced Phototoxicity. // International Journal of Molecular Science. 2020, 21, 8800, published 20 November 2020; DOI: 10.3390/ijms21228800


 Меню
Меню





 Все темы
Все темы





 0
0











